食欲素受体拮抗剂类抗失眠药物的研究进展
于景娴,池里群
北京市海淀区妇幼保健院药剂科,北京 100080
失眠是最常见的睡眠问题之一,长期失眠会严重影响个人的工作和生活。《中国失眠症诊断和治疗指南》(2017 年版)[1]中指出,失眠症是以频繁而持续的入睡困难和(或)睡眠维持困难并导致睡眠感不满意为特征的睡眠障碍。根据病程对其进行分类:病程<3 个月为短期失眠,病程≥3个月为慢性失眠。失眠具有入睡困难、睡眠维持困难或早醒的特征,并对日间功能和整体健康产生显著负面影响。日间功能障碍主要表现为疲劳、情绪低落或激惹、躯体不适、认知障碍等问题。此外,慢性失眠还可能导致工作效率下降、社交孤立[2],并增加精神障碍和心血管疾病等其他疾病的发生风险。研究表明[3-4],通过充分、适当地治疗失眠可改善心理健康和心血管疾病的结局。
目前,临床常用的改善失眠症状的药物主要为镇静催眠药,可分为两类:一类是苯二氮 类药物(benzodiazepine drugs, BZDs),如地西泮、劳拉西泮、艾司唑仑、阿普唑仑等;另一类是非苯二氮 类药物(nonbenzodiazepine drugs, non-BZDs),如唑吡坦、扎来普隆、佐匹克隆、右佐匹克隆等。BZDs存在生理依赖性问题,长期使用后停用会引发戒断症状,在我国被归为二类精神药品管理。此外,长期服用BZDs 还可能导致身体对药物产生耐受性或出现日间困倦、头昏、肌张力减低、跌倒、认知功能减退等不良反应。而non-BZDs 具有与BZDs 类似的催眠疗效,一般不产生日间困倦,且产生药物依赖的风险较传统BZDs 低。但需要注意,non-BZDs 有可能会在突然停药后发生一过性的失眠反弹。实际应用过程中患者往往难以忍受这些不良反应[5-6]。治疗失眠的理想药物是在短期和长期使用中均安全有效的药物,既能改善定量指标(如总睡眠时间、入睡后清醒时间和入睡潜伏期),又能提高睡眠质量、日间功能表现以及整体健康水平的药物[7]。随着人们对生活质量要求的不断提高,开发一种新型改善睡眠和治疗失眠的药物具有重要意义。
食欲素(orexin)是一种在下丘脑外侧区域合成和分泌的促进觉醒的神经肽。食欲素受体(orexin receptor)与食欲素结合,可以发挥调节睡眠-觉醒状态的作用。如果夜间食欲素分泌过多,会导致觉醒系统过于强大,不能顺利切换成睡眠系统,就会出现失眠。如果能够抑制夜间食欲素的活性或阻断食欲素与食欲素受体的结合,就会抑制食欲素的促清醒作用,减少觉醒信号、增加睡意、恢复正常睡眠节奏。食欲素受体拮抗剂在治疗失眠症方面表现出巨大潜力,已成为近期研究的热点之一。
1 食欲素及其受体的发展
1998 年,有2 个独立的研究小组对大鼠下丘脑进行了信使核糖核酸(messenger RNA,mRNA)和蛋白质的研究并有重要发现[8-9],即在大鼠下丘脑中发现了2 种未知的神经肽,分别被称为食欲素A 和B 或下丘脑泌素(hypocretin)1和2[8-9]。2012 年,国际基础和临床药理学联合会(International Union of Basic and Clinical Pharmacology)建议使用“食欲素”一词来描述这些多肽及其受体,并同时保留“下丘脑泌素”(缩写为HCRT)一词来描述其各自的基因和mRNA。HCRT基因可编码一种前体肽,分解成食欲素A和食欲素B 2 种活性肽,并可广泛投射到大脑各个区域,进而调节唤醒、清醒和食欲[10]。食欲素多肽是G 蛋白偶联的食欲素1 型受体(orexin-1 receptor , OX1R)和食欲素2 型受体(OX2R)的配体。食欲素A 以相似效力激活OX1R 和OX2R,而食欲素B 则优先激活OX2R[11]。
2 食欲素受体拮抗剂的发展
食欲素受体拮抗剂根据其结合亲和力可分为选择性OX1R 拮抗剂(selective orexin-1 receptor antagonists,SORA1s)、 选择性OX2R 拮抗剂(selective orexin-2 receptor antagonists,SORA2s)和双重食欲素受体拮抗剂(dual orexin receptor antagonists, DORAs)。OX2R 在睡眠调控中起关键作用,并可与OX1R 协同调节快速眼动(apid eye movement,REM)睡眠[12]。近20年来,国内外医药公司针对食欲素受体研发了几十个化合物,然而对于SORA1s 而言,并没有明显改善失眠的效果[13]。虽然部分SORA2s 在动物实验中显示出强大的催眠作用,但仍需要进一步进行临床研究[14]。由于DORAs 具有良好的抗失眠效果和安全性,在过去10 年里已成为新型抗失眠药物研发的主要方向。本文主要介绍DORAs 中的3 个明星药物,分别为suvorexant、lemborexant 和daridorexant,其已先后在美国上市,但目前在我国均尚未上市。
2.1 Suvorexant
Suvorexant 于2014 年在美国获批用于治疗由于入睡困难和(或)睡眠维持困难而导致的失眠,是首个获批的DORAs[15]。2016 年的一项研究显示[16],suvorexant 能够延长所有睡眠阶段的时长,特别是对REM 睡眠的改善效果较好。其可以使REM 睡眠在整个睡眠周期中所占比例提高达3.9%,且不改变总体睡眠结构,对于睡眠期间功率谱曲线的影响几乎可以忽略不计。2017 年发表的一篇系统综述发现[17],原发性失眠患者应用suvorexant后,在1 个月和3 个月内主观入睡时间和主观睡眠质量方面均有良好改善。2019 年的一项针对非老年(18~64 岁)和老年(≥65 岁)失眠患者为期3 个月的suvorexant 试验结果显示[18],根据年龄调整(非老年/老年患者)的给药剂量分别为40/30mg和20/15mg,且其在失眠严重指数方面改善睡眠程度均优于安慰剂组。
Suvorexant 最常见的不良反应是嗜睡、疲劳。有研究显示,服用suvorexant 20mg 剂量时,嗜睡发生率为5.1%,头痛发生率为6.7%,其他常见的不良反应包括上呼吸道感染、头晕、异常梦境和咳嗽等(>3%)。值得注意的是,嗜睡的发生与所服用的剂量呈正相关,剂量越高则发生率越高[18-19]。Suvorexant 主要通过细胞色素P450 3A(CYP3A)代谢,因此其药动学可能受到CYP3A 调节剂的影响,在使用CYP3A 激活剂或抑制剂时需谨慎[20]。另一项研究显示[21],suvorexant 在男性和女性中均表现出良好的耐受性和有效性,且对于绝经期患者可能将是一种较优的治疗选择。
Suvorexant 在老年人中显示出良好的临床疗效,并且可能对阿尔茨海默病伴失眠者有积极作用,同时具备良好的耐受性和轻微不良反应(以嗜睡最为常见)[22]。而一项对于年轻健康志愿者进行的研究表明[23],患者在服用suvorexant 20mg 或40mg 后的第二天早上驾车时,没有嗜睡的不良反应残留影响,但某些个体确会有影响。在2 型糖尿病患者中,suvorexant 能够改善睡眠质量和与肥胖相关的参数,包括血糖控制。这与对糖尿病模型小鼠进行临床前实验中所得到的数据非常吻合[24]。在接受治疗的高血压和失眠患者中,服用suvorexant 20mg 对白天、夜间或早晨血压都没有整体影响[25]。
相关研究发现[26],suvorexant 可能成为一种改善睡眠障碍、帮助戒断阿片类药物以及减少丁丙诺啡渴望方面的新的治疗方法。但是需要注意药物滥用等问题,包括非法使用或过量使用处方药。一项对健康者娱乐性多药使用进行的研究中发现了suvorexant 有被滥用的潜在风险,但相关研究认为suvorexant 的滥用倾向与唑吡坦相似甚至可能更低[26]。
2.2 Lemborexant
Lemborexant 属于DORAs,分别于2019 年12 月在美国和2020 年1 月在日本获得批准,用于治疗以入睡或保持睡眠困难为主要特征的成人失眠患者。与suvorexant 相比,lemborexant 对食欲素受体的抑制作用更强,且在OX1/2R 上表现出可逆的竞争性拮抗作用。其对于OX2R 的抑制作用明显优于OX1R,并具有较高的选择性,因此能够提供更强的抗失眠效果。同时,其与食欲素受体结合和解离速度快,相关研究显示与[27-28],安慰剂相比,lemborexant 并未影响次日日间功能,且可有效减少次日残留等不良反应。Lemborexant 的推荐剂量为5mg,受个体临床反应及耐药性等影响,其最大剂量可增至10mg,建议在睡前立即服用,并确保至少在计划苏醒时间前7h 服用,可有效减少入睡后觉醒[29]。2021 年的一项荟萃分析[30]比较了不同类别的失眠药(包括lemborexant、suvorexant、唑吡坦、佐匹克隆、右佐匹克隆、曲唑酮、氟硝西泮、艾司唑仑、三唑仑、溴替唑仑、替马西泮和雷美替安)在睡眠质量、入睡时间以及总睡眠时间方面的指标,结果显示lemborexant 可能是最佳的治疗方案。
与苯二氮 类相比,lemborexant 能显著减少相关头晕和姿势不稳的风险,且没有明显的药物相互作用;而对于老年人来说,lemborexant 可能比苯二氮 类药物更安全[30]。需要注意的是,对于那些可能对lemborexant 敏感的患者来说,在考虑到第二天早上驾车时可能出现的认知损伤风险,可能需要减少剂量[31]。Moline 等[28]通过对9 项临床试验数据进行分析,评估了lemborexant 在次日的残留效应,包括清晨的身体稳定性、认知能力、驾驶功能影响、主观困倦和嗜睡情况。结果显示,与安慰剂组相比,lemborexant 并没有明显影响次日白天的功能表现,并且经过长达6 个月的治疗后,使用lemborexant 的患者在第二天早上更加警觉;服用lemborexant 5mg 的患者嗜睡发生率为8.6%,稍高于suvorexant。一项针对日本人群的回顾性研究表明[32],在持续用药6 个月后停药时,因为嗜睡、疲劳和噩梦等原因引起的不适症状可以自行缓解,这可能与该药半衰期较长有关。
2.3 Daridorexant
Daridorexant 作为一种新型高效的DORAs,于2022 年1 月在美国批准上市,其剂量包括25mg和50mg。与安慰剂相比,daridorexant 25mg 和50mg 剂量在1 个月和3 个月时可以改善成人患者(包括老年人)的夜间睡眠和日间状态,能够帮助患者达到与生理睡眠周期相似的睡眠效果,可增加总体睡眠时长,提升睡眠质量,并具有良好的安全性[33-34]。Daridorexant 的体内药动学曲线更优越,其半衰期为5.9~8.8h,更符合人体自然睡眠周期,既能保持夜间睡眠质量,同时又对次日日间功能影响较小;生物利用度高,能够迅速吸收和代谢[35]。Kunz 等[36]进行了为期52 周的研究,设置了安慰剂作为对照组,观察了daridorexant 的治疗安全性、夜间有效性以及对日间功能的影响。研究结果显示,在失眠患者中,服用daridorexant 10mg、25mg和50mg 剂量组均表现出良好的长期安全性和耐受性,没有出现身体依赖、耐受或失眠反弹。有效性分析显示,相较于安慰剂组,daridorexant 50mg剂量组患者临床效果最好,并有助于改善患者的总睡眠时间和日间功能,且该研究结束时未发现相关益处逐渐消退的迹象。
Daridorexant 最常见的不良反应包括头痛和嗜睡,发生率均<3%;头晕和疲劳的发生率均<2%。与安慰剂组相比,服用daridorexant 的患者未表现出日间过度嗜睡[33]。在52 周停止研究治疗后[36],各治疗组的苯二氮 类药物戒断症状问卷(benzodiazepine withdrawal symptom questionnaire,BWSQ)评分相似且均较低,且daridorexant 组和安慰剂组间无统计学差异。在试验结束时,没有患者达到BWSQ 评分>20 分;未观察到剂量依赖性;没有证据表明其有任何与停药相关的症状或者反跳性失眠,提示滥用可能性低[36-37]。
2.4 3 种DORAs 类药物对比
本文主要介绍的3 个DORAs 明星药物均经CYP3A4 代谢,主要通过粪便和尿液排泄,药动学的主要区别在于半衰期不同。3 种DORAs 药品相关情况比较见表1[38]。
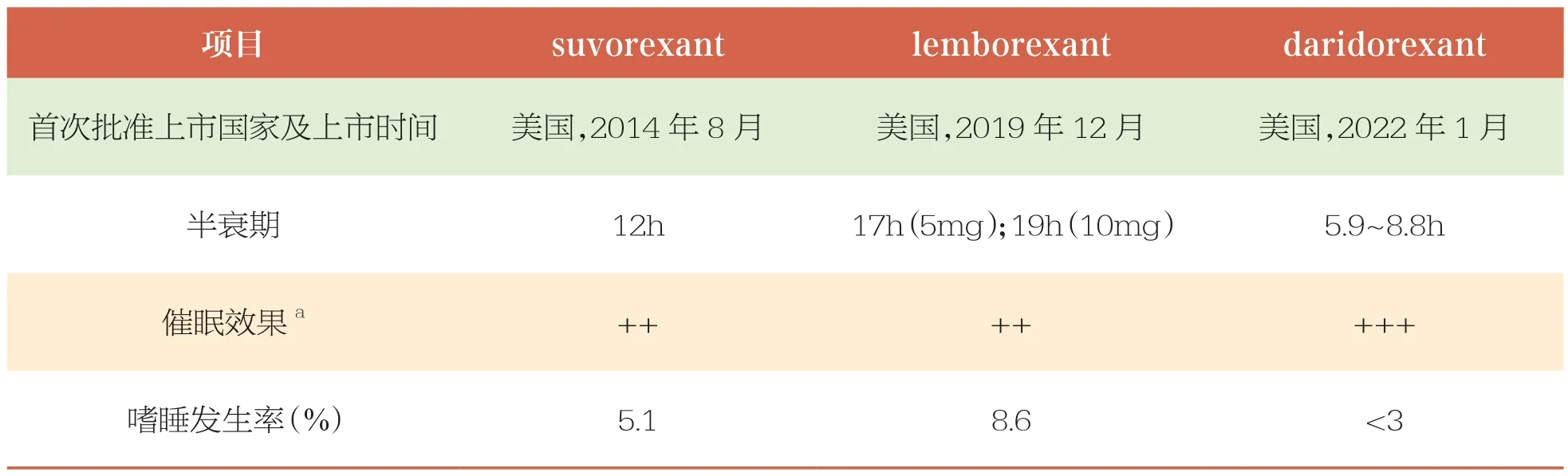
表1 3 种DORAs 药品相关情况比较
3 小结
综上所述,食欲素受体拮抗剂是一种具有很大潜力的治疗失眠的方法,有着广阔的应用前景,为解决睡眠障碍、焦虑症和药物成瘾治疗提供了突破口。作为新一代抗失眠药物,食欲素受体拮抗剂通过独特的机制减弱觉醒信号,从而抑制清醒状态而非诱导镇静,在一定程度上解决了传统镇静催眠药物存在的一些缺点。另外,此类药对次日日间功能影响较小、成瘾性较低,尤其最新上市的daridorexant 能够帮助患者达到与生理睡眠周期相似的睡眠效果,提高睡眠质量。但需要注意的是,目前对于特殊人群,如儿童、妊娠期和哺乳期妇女等,使用该类药物的数据几乎为零,且其应用于失眠患者的长期安全性和有效性仍需开展更多临床前和临床研究。
suvorexant

