人工智能辅助头颈部电子计算机断层扫描血管成像在颅内动脉瘤诊断中的应用
王勇 武汉忠 常燕翔 朱华 夏茜


作者简介:王勇,大学本科,副主任医师,研究方向:神经系统疾病诊断。
通信作者:武汉忠,大学本科,副主任医师,研究方向:神经系统疾病诊断。E-mail:15151099196@163.com
【摘要】目的 分析应用人工智能辅助头颈部电子计算机断层扫描血管成像(CTA)对颅内动脉瘤诊断的准确性,为该疾病的诊治提供参考依据。方法 回顾性分析东台市人民医院在2021年9月至2023年9月期间收治的68例疑似颅内动脉瘤患者的临床资料,所有研究对象均接受头颈CTA、数字减影血管造影(DSA)检查。以DSA为金标准,分析所有疑似颅内动脉瘤患者经人工智能辅助头颈部CTA检查的检出情况、诊断效能,包括阳性例数检出情况、病灶大小(病灶>5 mm、3~5 mm、<3 mm)检出情况。结果 68例研究对象经金标准检查,其中阳性53例,阴性15例,经CTA检查与DSA诊断结果的一致性较好(Kappa=0.708)。53例颅内动脉瘤患者经金标准检查出61个病灶;经CTA检查颅内动脉瘤病灶大小(病灶>5 mm、3~5 mm)与DSA诊断结果的一致性较好(Kappa分别为0.651、0.666,P<0.05);人工智能辅助头颈CTA检查对颅内动脉瘤的诊断特异度、灵敏度及准确度分别为80.00%、92.45%、89.71%,且对
>5 mm、3~5 mm的病灶的诊断灵敏度、准确度均较<3 mm病灶更高(均P<0.05)。结论 在颅内动脉瘤中,人工智能辅助头颈CTA具有良好的诊断价值,尤其是对病灶>5 mm、3~5 mm患者的诊断效能较高,因此,临床可在诊断颅内动脉瘤时运用人工智能辅助头颈CTA的检查结果及其影像学特征,以期提高筛查颅内动脉瘤的准确率。
【关键词】颅内动脉瘤 ; 人工智能 ; 电子计算机断层扫描血管成像 ; 诊断 ; 准确性
【中图分类号】R445【文献标识码】A【文章编号】2096-3718.2024.06.0095.04
DOI:10.3969/j.issn.2096-3718.2024.06.031
颅内动脉瘤是临床中常见的脑血管疾病,多数患者无明显临床表现,少数患者可伴有头痛、麻木等症状。颅内动脉瘤一旦发生破裂,则可引发蛛网膜下腔出血,进而导致患者残疾甚至死亡,故及时发现、诊断至关重要。现阶段,临床诊断颅内动脉瘤主要是以数字减影血管造影(DSA)作为金标准,可有效检出患者疾病情况,但其在应用中存在一定局限性,如会对患者机体造成损伤,从而易影响其后期患者治疗的依从性;耗时较长,易延误患者最佳抢救时机等,从而影响临床使用[1]。随着影像学检查技术的进步,电子计算机断层扫描血管成像(CTA)已逐渐应用于疾病诊断中,且具有操作方便、无创等优势。头颈CTA主要是通过扫描以获取头颈部位图像,进而清晰显示其形态、结构,能够为疾病的临床诊疗提供有效信息,目前头颈CTA诊断结果主要依赖影像科医师的经验,故易存在漏诊、误诊情况[2]。人工智能自2017年以来逐渐被用于辅助头颈CTA检查以诊断颅内动脉瘤,其能够获取更为清晰的影像图像,且病灶观察视野更广泛[3],但现阶段关于其应用价值情况尚未完全明确。基于此,本研究通过选取68例疑似颅内动脉瘤患者进行回顾性分析,旨在探究颅内动脉瘤诊断应用人工智能辅助头颈CTA的准确性,现将研究结果进行如下报道。
1 资料与方法
1.1 一般资料 回顾性分析2021年9月至2023年9月期间东台市人民医院收治的68例疑似颅内动脉瘤患者的临床资料,均开展头颈CTA、DSA检查。以DSA为金标准。所有研究对象年龄35~78岁,平均(53.47±
5.47)岁;男、女性分别为38、30例;BMI 18~25 kg/m2,平均(22.52±0.74) kg/m2。纳入标准:⑴伴有头痛、麻木、缺血性症状等临床表现;⑵存在多发病灶情况;⑶头颈CTA、DSA检查间隔时间短于14 d;⑷非开颅手术、血管内介入栓塞等术后患者。排除标准:⑴伴有恶性肿瘤或精神系统疾病;⑵重要脏器(心、肝等)器质性病变;⑶图像质量差无法进行人工智能处理;⑷对碘对比剂过敏;⑸同期参与其他相关研究。此次研究经东台市人民医院医学伦理委员会批准。
1.2 研究方法 所有研究对象均接受头颈CTA、DSA检查,其中CTA检查具体方法如下:使用CT扫描仪(美国通用电气公司,型号:revolution 256)进行扫描头颈部位,采用迭代重建算法,设置图像层厚(1.0 mm)、矩阵(512×512)、层间距(0.7 mm),以获取CTA图像,进行增强扫描,选择监测点:主动脉弓层面,自动触发扫描:设置触发阈值(100 HU)。静脉注射碘普罗胺注射液(成都倍特药业股份有限公司,国药准字H20233136,规格:100 mL∶62.34 g),经右肘正中注射,40~50 mL/次,注射速度:4.5~5.0 mL/s,而后注入生理盐水(30 mL)。人工智能评价检测图像:使用Cerebral Doc头颈人工智能辅助诊断系统软件(数坤科技头颈血管智能诊断系统V1.0),自动识别、处理头颈CTA图像(使用三维卷积神经网络),得到头颈CTA诊断结果,阳性判定标准参考《颅内动脉瘤影像学判读专家共识》 [4]。
DSA检查具体方法如下:由两名具有中级职称以上影像诊断医师在Philips INTEGRIS 3D-RA工作站上,使用血管造影机(荷兰皇家飞利浦电子公司,型号:
Allura Xper FD20),穿刺置管(经股动脉插管,使用Seldinger技术),常规注射碘普罗胺(双侧颈内动脉、椎动脉血管),得到2D-DSA图像,检查全脑血管(通过旋转DSA),行3D-DSA重建,记录颅内动脉瘤的有无、大小、数量及位置情况。DSA检查阳性判定标准[4]:颅内动脉分叉部的囊袋状瘤样凸起。当医师的诊断结果意见不一致时,由高年资高级职称医師审核或排除。
1.3 观察指标 ⑴人工智能辅助头颈CTA检查对颅内动脉瘤的检出情况,包括阳性例数检出情况、病灶大小(病灶>5 mm、3~5 mm、<3 mm)检出情况。⑵人工智能辅助头颈CTA检查对颅内动脉瘤的诊断效能。其中特异度=[真阴性例数/(假阳性+真阴性)例数]×100%;灵敏度=[真阳性例数/(真阳性+假阴性)例数]×100%;准确度=[(真阳性+真阴性)例数/总例数]×100.00%。⑶典型病例图片分析。
1.4 统计学方法 采用SPSS 26.0统计学软件分析,计数资料以[例(%)]表示,采用χ2检验;应用Kappa检验评价人工智能辅助头颈CTA检查与DSA诊断结果的一致性:<0.4表示一致性差,0.4~0.75表示一致性较好,>0.75表示一致性高。 P<0.05为差异有统计学意义。
2 结果
2.1 人工智能辅助头颈CTA检查对颅内动脉瘤的检出情况 经金标准检查,68例研究对象中阳性53例,阴性15例;经CTA检查与DSA诊断结果的一致性较好(Kappa=0.708)。53例颅内动脉瘤患者经金标准检查出
61个病灶;经CTA检查颅内动脉瘤病灶大小(病灶>5 mm、3~5 mm)与DSA诊断结果的一致性较好(Kappa分别为0.651、0.666,均P<0.05);经CTA检查颅内动脉瘤病灶<3 mm与DSA诊断结果的Kappa值为0.023,P>0.05),见表1、表2。
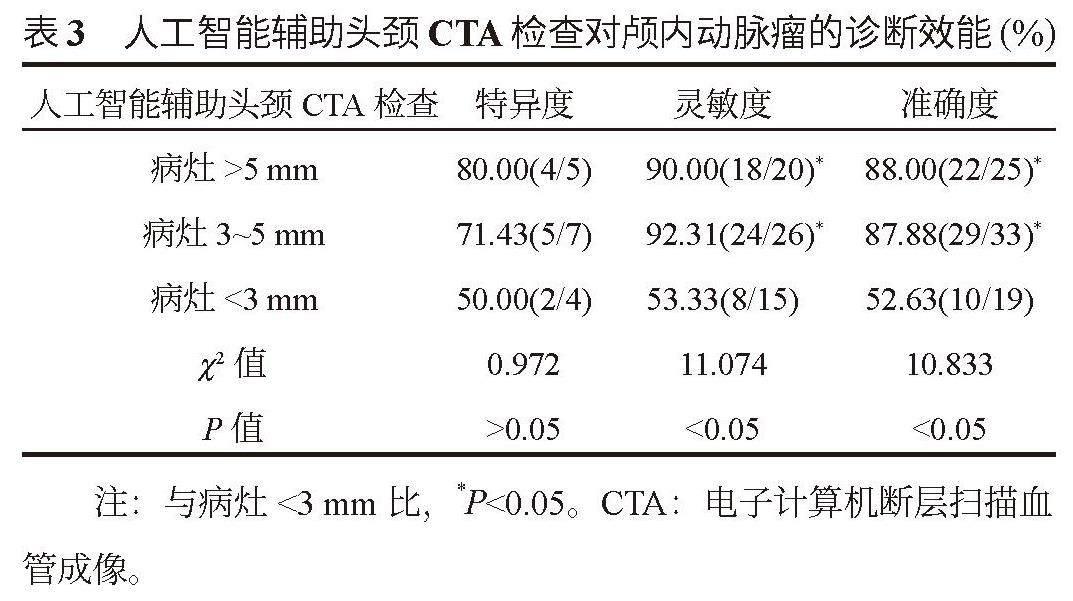
2.2 人工智能辅助头颈CTA检查对颅内动脉瘤的诊断效能 人工智能辅助头颈CTA检查对颅内动脉瘤的诊断特异度、灵敏度及准确度分别为80.00%、92.45%、89.71%,且对>5 mm、3~5 mm的病灶的诊断灵敏度、准确度均较<3 mm病灶更高,差异均有统计学意义(均P<0.05),见表3。
2.3 典型病例图片及详细对应介绍 患者,女性,63岁,因突发头痛、呕吐40 min,送至江苏省东台市人民医院急诊内科就诊,急诊查头颅平扫CT示:蛛网膜下腔出血(环池、小脑天幕、侧裂池密度增高);急诊头颅CTA示基底动脉瘤状突起,图中箭头所示为病灶,提示基底动脉瘤,人工智能自动处理头颅CTA,见图1-A;DSA检查,图中箭头所示为病灶:基底动脉动脉瘤证实基底动脉瘤,见图1-B。
3 讨论
颅内动脉瘤主要是由动脉硬化、感染等因素影响而导致颅内动脉管壁局部异常扩张,并表现为瘤状突出的一种血管壁损害。颅内动脉瘤具有潜在致命性,且预后较差,因此,临床早期快速、精准检出颅内动脉瘤患者,可有助于管理该类患者,且对患者生活质量改善具有重要意义。DSA主要是通过高时间、空间分辨率进行诊断颅内动脉瘤,具有较高的诊断价值,但其属于侵入性操作,可能会对受检者机体造成损伤,从而使得临床应用受到一定限制[5-6]。
随着医学影像学的进步,CTA在疾病诊疗中发挥的作用也随之增加,现已成为多种疾病筛查、诊疗不可或缺的工具。CTA具有无创、快速、操作简单等优势,现已广泛应用于脑血管疾病的诊疗中,但由于其在应用中受主观性(人工测量)的影响,而难以获取病灶的复杂特征,进而使得诊断结果存在差异[7-8]。人工智能是以深度学习计算机算法为基础,可通过快速识别、处理大量的数据信息,并对图像进行自动化分割、提取及分析数据,完整显示颅内动脉瘤和血管情况,进而有助于提高检查的客观性及准确率,因此人工智能辅助头颈CTA检查对颅内动脉瘤具有较高的临床应用价值[9]。
本研究结果显示,68例研究对象经金标准检查,其中阳性53例,阴性15例;经CTA检查与DSA诊断结果的一致性较好(Kappa=0.708)。53例颅内动脉瘤患者經金标准检查出61个病灶 ;经CTA检查颅内动脉瘤病灶大小(病灶>5 mm、3~5 mm)与DSA诊断结果的一致性较好(Kappa分别为0.651、0.666);且人工智能辅助头颈CTA检查对颅内动脉瘤(阳性例数、病灶>5 mm与3~5 mm)的灵敏度、准确度均较高,表明在颅内动脉瘤中,人工智能辅助头颈CTA具有良好的诊断价值,尤其是对病灶>5 mm、3~5 mm患者的诊断效能较高,与胡斌等[10]研究结果基本一致。分析其原因在于,本研究采用人工智能主要是利用三维卷积神经网络进行骨分割和血管分割,能够确保完整识别提取颅内动脉瘤模型,进行精准的瘤体长径和短径测量,尤其是对病灶>5 mm、3~5 mm患者,进而实现“数字化”动脉瘤,获得与金标准结果较好的一致性,可为诊断医生提供更多的可靠依据。但该研究结果存在一定的误诊、漏诊情况,分析其原因可能为,检查时患者的配合度可受多种因素影响(如种类、病情严重程度不同),同时蛛网膜下腔出血(动脉瘤破裂所致)会对影像学征象产生一定程度掩盖,进而对准确诊断疾病造成一定的困难[11-12]。因此,临床可在诊断颅内动脉瘤时运用人工智能辅助头颈CTA的检查结果及其影像学特征,以提高诊断颅内动脉瘤的准确率。同时,临床还建立了颅内动脉瘤临床科研数据库,以收集动脉瘤患者资料全面分析动脉瘤各方面特征,不断修正人工智能并进行外部验证,改进动脉瘤诊断流程,以更智能和自动化的方法简化临床工作中对动脉瘤的检测(量化、报告)、破裂风险及并发症预测、治疗策略选择和复发风险评估,以期能有对人类疾病诊疗的新发现。
综上,在颅内动脉瘤中,人工智能辅助头颈CTA具有良好的诊断价值,尤其是对病灶>5 mm、3~5 mm患者的诊断效能较高,因此,临床可在诊断颅内动脉瘤时运用人工智能辅助头颈CTA的检查结果及其影像学特征,以提高筛查颅内动脉瘤的准确率。但值得注意的是,本研究仍存在一定不足之处,如回顾性研究无法保证全部信息的准确性与可信度,单中心研究等,可能影响数据统计和分析,致使结果存在偏倚。基于此,临床仍有待进一步研究进行验证人工智能辅助头颈部CTA诊断颅内动脉瘤的
准确性。
参考文献
翁海明. 3D-DSA与3D-CTA成像在颅内动脉瘤早期诊断中的应用效果比较[J]. 中国急救医学, 2017, 37(1): 128-129.
林惠岚. 头颈部CTA能谱成像与头颈部DSA对微小动脉瘤筛查及诊治的比较研究[J]. 中西医结合心脑血管病杂志, 2017, 15(15): 1918-1921.
李锐, 阎世鑫, 靳松. 人工智能技术在颅内动脉瘤诊疗中的研究进展[J]. 国际医学放射学杂志, 2021, 44(4): 461-465.
中国医师协会神经介入专业委员会, 中国颅内动脉瘤计划研究组, 张鸿祺, 等. 颅内动脉瘤影像学判读专家共识[J]. 中国脑血管病杂志, 2021, 18(7): 492-504.
邓昊, 韦鑫, 曹闻挺, 等. AI辅助头颈CTA在诊断颅内动脉瘤中的应用[J]. 第三军医大学学报, 2021, 43(12): 1179-1184.
张倩, 姜淼淼, 黄艳, 等. 探讨CT血管造影(CTA)在颅内动脉瘤(IA)诊断中应用[J]. 中国CT和MRI杂志, 2023, 21(4): 1-3.
祁冬, 施彪, 姚传顺, 等. 人工智能对颅内动脉瘤CTA诊断价值初探[J]. 联勤军事医学, 2023, 37(7): 576-580.
梁奕, 柳柏玉, 杨威威, 等. 人工智能在头颈部CTA中的应用价值[J]. 医学影像学杂志, 2022, 32(10): 1824-1826.
王珍, 邱晓明, 叶宇. 人工智能技术在头颈部CT血管成像中的临床应用价值[J]. 临床放射学杂志, 2022, 41(11): 2025-2030.
胡斌, 荐志洁, 张蕴, 等. 基于头颈部CTA的人工智能辅助诊断系统对颅内动脉瘤的应用价值探讨[J].中國数字医学, 2022, 17(1): 33-37, 26.
姜雪, 李王佳, 魏淼, 等. 容积CT数字减影血管造影与人工智能技术对头颈CTA减影效果的比较[J]. 中国医疗设备, 2020, 35(10): 113-116.
武玉良, 朱玉英, 赵孟德, 等. CTA与DSA诊断颅内动脉瘤的临床应用分析[J]. 医学影像学杂志, 2022, 32(5): 858-860.

