海藻酸钠/壳聚糖引导酸蚀离体牙在模拟体液中生成羟基磷灰石晶体的实验研究
韩 凉,张胜楠,朱山成
(1济南市口腔医院,济南 250014;2焦作市第二人民医院)
目前,牙体组织缺损修复所采用的各类异质修复材料无论在结构、性质和组成上都与牙组织相差较远;牙组织与修复材料之间均存在界面问题,现有缺损牙体组织的修复技术均会造成牙体组织的破坏,而上述均为牙本质过敏、边缘微漏、继发龋并发症的重要因素。因此,利用基质模板实现可控性磷灰石晶体生长,仿生合成与天然牙体组织类似结构的生物材料,诱导损伤牙体组织自愈修复已成为口腔医学的一个新的研究热点[1]。近年来,我们对酸蚀离体牙用海藻酸钠/壳聚糖处理后浸入模拟体液(SBF)中,采用扫描电镜(SEM)、X射线衍射仪(XRD)和傅立叶红外光谱仪(FTIR)对处理后离体牙分别进行形貌观察、元素性质确定和谱图测定,旨在为牙体组织损伤的自愈性修复、牙本质过敏症等临床问题提供新的治疗途径。
1 材料与方法
1.1 材料 正畸拔除的完整、无龋的前磨牙(济南市口腔医院东院口腔外科提供)1颗,劈开,超声清洗,4℃下储存于2.5%的戊二醛溶液中,1个月内使用;牙体酸蚀剂(35%磷酸酸蚀剂);海藻酸钠(黏度10 g/L,20 ℃)/(Pa·s)≥0.02),壳聚糖(脱乙酰度92%,MW为2.9×105)。SBF(采用Kukobo配方,按参照文献[2]提供的方法进行SBF的配置,SBF配置完成后使用10 mol/L HCl滴定,将配置完成溶液的 pH值滴定到 7.0);50%、70%、80%、90%、95%、100%梯度乙醇。50 mL聚乙烯塑料离心管;1000 mL聚乙烯塑料烧杯。SEM(S-3400N);XRD;FTIR;磁力搅拌器;恒温水浴箱。
1.2 实验方法 清洗烧杯并消毒,干燥后注入2%海藻酸钠水溶液,缓慢加入25%CaCl2溶液,经过Ca2+-Na+离子交换作用后,再加入1%壳聚糖溶液,制备海藻酸钠/壳聚糖凝胶。将离体牙用酚醛树脂包埋固化,经砂纸打磨,水溶性抛光膏抛光后,用37%磷酸腐蚀牙釉质层1 min。去离子水超声清洗3次自然干燥后将样品置入海藻酸钠/壳聚糖凝胶与1%海藻酸钠水溶液中静置24 h。将表面修饰完成的离体牙放置于已经加入50 mL SBF的离心管内,密封管口后置入37℃恒温水浴箱中孵育,每日定时更换SBF,7 d后取出离体牙。用去离子水反复冲洗,常温下干燥,表面喷金,肉眼及SEM下观察其形貌,剥落覆盖在牙釉质表面形成的晶体,50℃低温干燥后XRD测定生成物晶相,采用KBr压片法在FTIR下测定晶体颗粒谱图。
2 结果
2.1 肉眼观察 于SBF溶液中浸泡7 d后可见离体牙釉质表面布满了白色物质与未浸泡离体牙釉质颜色有明显区别。
2.2 SEM观察SEM照片显示为未经矿化的酸蚀牙釉质表面形成类似蜂巢状凹坑,内无晶体沉积;经过SBF溶液矿化后的牙釉质表面经酸蚀形成的蜂巢状凹坑中有簇状、块状、球状或板状晶体,晶体呈现多样性。
2.3 XRD检测 对SBF溶液中浸泡7 d后覆盖在牙釉质表面形成的晶体进行剥离、对其使用XRD进行分析(图1),可见釉质表面生成的物质在2θ角为25.723°时对应的 D 值为 3.4380;31.536°时对应的D值为2.8026,为羟基磷灰石晶体(HA)的特征峰[3],提示海藻酸/壳聚糖可诱导矿化生成 HA晶体。
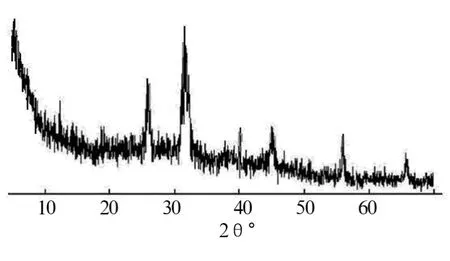
图1 白色晶体的XRD谱
2.4 FTIR检测 FTIR图谱见图2。图2中的3个反射峰 557 cm-1、609 cm-1、1042 cm-1为 HA 晶体中磷酸根振动谱带的3个特征峰,羟基基团的吸收峰表现在1637 cm-1和3442 cm-1处出现的2个反射峰。碳酸根的吸收峰表现在868 cm-1和1421 cm-1出现的反射峰,可见在SBF中生成的晶体为含有碳酸根的 HA[4]。
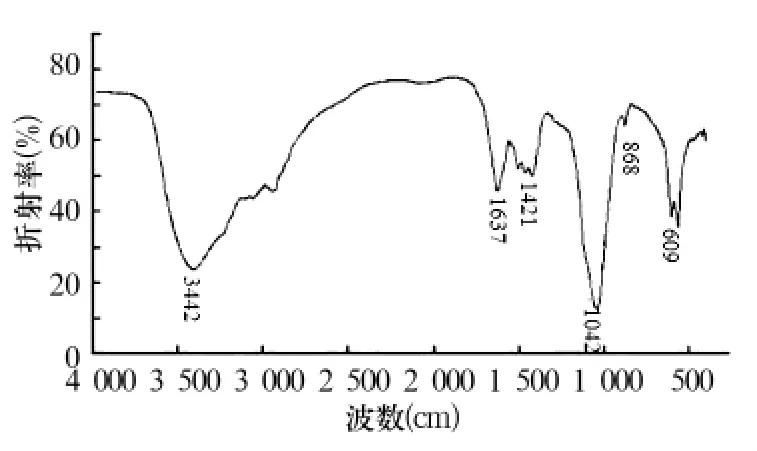
图2 在SBF中浸泡7 d后FTIR图谱
3 讨论
陶瓷、复合树脂、金属等为目前修复牙体组织缺损的主要材料[5,6],但由于其结构组成及生物学特性上与天然牙体组织存在较大差别,加之修复技术对牙体组织造成破坏,修复后易导致修复材料与牙体硬组织之间出现难以用肉眼观察的微小缝隙,而这些缝隙是液体、细菌、分子和离子的通道,可导致活髓牙充填后的术后敏感,充填体边缘着色、松动、脱落、继发龋以及牙髓炎与根尖周炎等一系列临床并发症,已成为口腔临床急待解决的难题[7]。海藻酸钠通过(1-4)糖苷键聚合β-D-甘露糖醛酸(M)和α-L-古罗糖醛酸(G)生成,海藻酸钙凝胶是海藻酸钠通过Ca2+在离子交换作用下置换出Na+而形成的既有弹性又有强度的凝胶样物质。在骨缺损修复领域,海藻酸钙凝胶既可以在骨缺损处形成空间支架结构来诱导仿生矿化又可为骨修复提供适量再生空间[8]。壳聚糖的吡喃环型葡萄糖结构单元中分别含有氨基和醇羟基2个活性基团,这2个活性基团可以黏附和聚集成骨细胞、牙周膜细胞,并加速这些细胞的分化和增殖。
聚电解质复合物是由静电作用将天然聚阳离子物质和天然聚阴离子物质组装成的有序复合体,有诱导人体各组织细胞的分化和增殖的生物性能,因此可作为新型骨引导再生膜的有机模板[9]。本实验通过静电作用将天然聚阳离子物质壳聚糖和天然聚阴离子物质海藻酸钠组装成有序复合体,利用海藻酸钠—壳聚糖中的天然聚阴离子物质的海藻酸钠不断摄取SBF中的Ca2+离子形成结晶矿化中心,再与、OH-等离子根结合,在牙釉质表面诱导生成HA[10]。依据分子仿生矿化原理,对于修复体与牙体之间的缝隙采用牙釉质表面经再矿化生成的磷灰石晶体来堵塞,从而在可能发生微渗漏处建立起一道人工修复体和牙体结构之间的物理屏障,这将为未来解决牙体组织损伤的自愈性修复、牙本质过敏症等临床问题提供新的治疗途径。
[1]张胜楠,唐旭炎,李全利.牙体粘接剂在模拟体液中诱导生成磷灰石晶体[J].安徽医科大学学报,2008,43(6):667-669.
[2]Nemoto R,Nakamura S,Lsobe T,et al.Direct synthesis of hydroxyapatite-silk fibroin nano-composite sol via a mechanochemical route[J].J Sol-Gel Sci Tech,2001,21(6):7-12.
[3]Murphy WL,Mooney DJ.Bioinspired growth of crystallin ecarbonate apatite on iodegradable polymer substrata[J].J Am Chem Soc,2002,124(9):1910-1917.
[4]Hayakawa T,Yoshinari M,Sakae T.Calcium phosphate form ationon the phosphorylated dental bonding agent in electrolyte solution[J].J Oral Rehabil,2004,31(7):67-73.
[5]Hench LL,Polak JM.Third-generation biomedical materials[J].Science,2002,295(5557):1014-1017.
[6]Griffith LG.Emerging design principles in biomaterials and scaffolds for tissue engineering[J].Ann NY Acad Sci,2002,961(6):83-85.
[7]Larson TD.The clinical significance and management of microleakage.Part two[J].Northwest Dent,2005,84(2):15-19.
[8]刘袖洞,于炜婷,王为,等.海藻酸钠和壳聚糖聚电解质微胶囊及其生物医学应用[J].化学进展,2008,20(1):126-139.
[9]Mi FL,Wu YB,Shyu SS,et al.Control of wound infections using a bilayer chitosan wound dressing with sustainable antibiotic delivery[J].J Biomed Mater Res,2002,59(3):438-449.
[10]Shi H,Ratner BD.Template recognition of protein-imprinted polymer surfaces.[J].Biomed Mater Res,2000,49(1):1-11.

