依诺肝素钠中残留N,N-二甲基甲酰胺的测定
王悦,李京,李颖颖,范慧红
(中国食品药品检定研究院,北京 100050)
依诺肝素钠中残留N,N-二甲基甲酰胺的测定
王悦,李京,李颖颖,范慧红△
(中国食品药品检定研究院,北京 100050)
目的 建立依诺肝素钠原料中N,N-二甲基甲酰胺残留的测定方法。方法 采用乙醇作为萃取剂,使依诺肝素钠生成沉淀,N,N-二甲基甲酰胺则溶于乙醇,取上清液直接进样,用气相色谱仪分析。色谱柱为Agilent DB-wax(30m×0.53mm,1.0μm);载气为高纯氮气;流速为3m L/min;采用程序升温的方式;进样口温度为200℃;FID检测器温度为250℃。结果 该方法测得的线性范围为8.8~880μg/mL;定量限为11.6μg/mL;检出限为3.5μg/m L;加样回收率为94.8%,RSD为2.0%。结论 该检测方法方便、快速、准确,避免了样品基质对测定的干扰,可用来控制依诺肝素钠中痕量N,N-二甲基甲酰胺残留。
N,N-二甲基甲酰胺;依诺肝素钠;气相色谱法
低分子肝素(low molecular weight heparin,LMWH)是酶解或化学裂解肝素后得到的产物,其抗血栓作用优于肝素,生物利用度高、出血倾向小,是肝素的第二代产品[1]。根据原料来源、生产工艺[2]、末端结构[3-5]的不同,低分子肝素被分为许多不同的种类,它们的分子量与分子量分布、硫酸化程度、抗凝活性均不相同[6]。不同种类的低分子肝素在其生产过程中会使用到不同的有机溶剂;相同品种的LMWH也会由于不同工艺步骤而使用不同的溶剂,因此应分别控制。
依诺肝素钠是将肝素的苄基酯衍生物进行碱裂解而获得的一种低分子肝素,生产工艺较为复杂,在生产过程中除LWMH常用到的甲醇、乙醇等溶剂外,不同企业根据工艺不同,还会使用二氯甲烷[7]或N,N-二甲基甲酰胺等溶剂。N,N-二甲基甲酰胺属于第二类有机溶剂,需要对其在药品中的残留量进行控制,ICH规定其残留量不得超过0.088%。目前药典项目有关均采用气相色谱法来测定挥发性溶剂的残留量,由于N,N-二甲基甲酰胺的沸点较高(149℃~156℃),不容易充分汽化[8],中国药典明确建议采用直接进样法测定此类沸点较高的溶剂[9]。但依诺肝素钠除溶于水外,不溶于乙醇、乙醚、氯仿等有机溶剂,因此本研究曾尝试采用水溶液直接进样及顶空进样等方式,结果均不理想。考虑到依诺肝素钠不溶于乙醇,而N,N-二甲基甲酰胺可与乙醇互溶的性质,本文建立了乙醇萃取的样品处理方式,对依诺肝素钠原料中残留N,N-二甲基甲酰胺进行定量检查。
1 材料与方法
1.1 仪器与试药 HP 6890 plus气相色谱仪,HP 7683自动进样器,FID检测器,SDG-300氮氢空一体机。
乙醇购自CNW公司,绝对纯;N,N-二甲基甲酰胺购自J&K公司。6批依诺肝素钠原料药分别由杭州九源基因有限公司和深圳天道医药有限公司提供。
1.2 溶液制备
1.2.1 对照品溶液:准确称取N,N-二甲基甲酰胺适量,用乙醇稀释制成880μg/mL的贮备液。精密移取1.0mL置10mL量瓶内,加乙醇稀释至刻度,混匀即得。
1.2.2 供试品溶液:称取供试品1.0 g,置10 m L量瓶内,加2 mL水溶解后,缓慢加入乙醇,边加边振摇并稀释至刻度,混匀。室温下放置至沉淀生成完全后,取上清液放入离心机内10000 r/min离心5 min,取上清液0.45μm滤膜过滤即得。
1.3 色谱条件 色谱柱:AgilentDB-WAX(30m×0.53mm,1.0μm);载气为高纯氮气;升温梯度:起始温度100℃,维持2 min;以5℃/min的速率升至140℃;流速为3mL/min;分流比为10∶1;进样口温度为200℃;FID检测器温度为250℃。
2 结果
2.1 专属性试验 按照1.2.1方法,配制不含N,N-二甲基甲酰胺的阴性溶液,进样1μL,记录色谱图,在N,N-二甲基甲酰胺出峰位置附近无色谱峰干扰。对照品溶液色谱图内,乙醇与N,N-二甲基甲酰胺色谱峰分离度能够符合要求(见图1)。
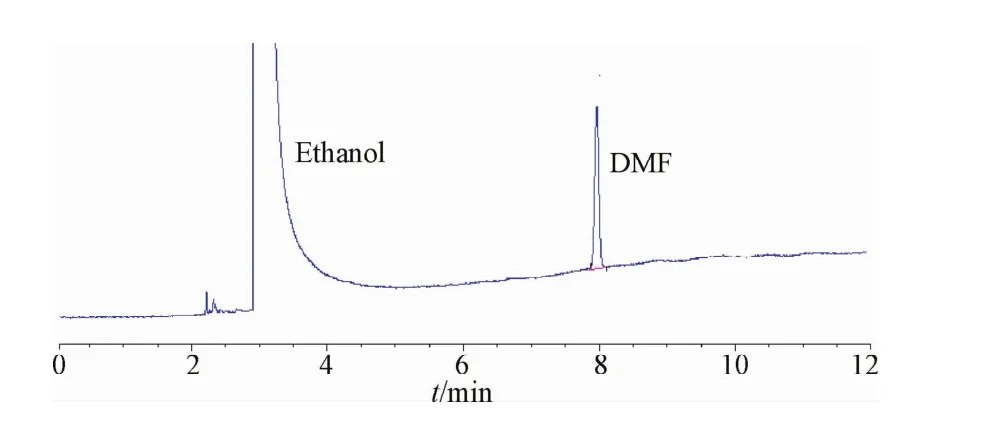
图1 对照品溶液色谱图Fig.1 The chromatography of standard solution
2.2 线性关系、定量限及检测限考察分别精密吸取对照品贮备液 0.1、0.2、0.5、1.0、2.0、5.0、10.0mL,置 10mL量瓶内,加入乙醇稀释至刻度并混匀,得到含N,N-二甲基甲酰胺分别为8.8、17.6、44、88、176、440、880 μg/mL的系列线性溶液。 分别吸取上述线性溶液1μL进样,记录峰面积。以对照品的质量浓度X(μg/mL)为横坐标,峰面积Y为纵坐标进行线性回归,得出N,N-二甲基甲酰的回归方程为Y=0.3254X-0.0575,r=0.9999。取低浓度溶液逐级稀释,以信噪比为3得出检测限为3.5μg/mL;以信噪比为10时得出定量限为11.6μg/mL。
2.3 精密度试验 取对照品溶液1μL,注入气相色谱仪,连续进样6次,记录峰面积,测得的N,N-二甲基甲酰胺峰面积RSD为0.26%,说明仪器精密度良好。
2.4 加样回收率 称取9份已测定含量的样品0.5 g,精密称定,按低、中、高3个浓度分别加入对照品贮备液0.4、0.5、0.6mL,每个浓度平行3份,充分混匀,加入1mL水溶解,缓慢加入乙醇,边加边振摇并稀释至刻度,混匀。室温下放置至沉淀生成完全后,取上清液放入离心机内10000 r/min离心5min,取上清液0.45μm滤膜过滤。分别进样1μL,记录峰面积,计算加样回收率,结果见表1。

表1 加样回收率试验结果Tab.1 Sample recovery test results
2.5 实际样品测定 将6批供试品分别按照1.2.2方法配制。取对照品溶液(图1)和供试品溶液(图2)各1μL进样,记录峰面积,按外标法计算供试品溶液中N,N-二甲基甲酰胺残留量,结果均未检出,可见受试样品工艺中未使用N,N-二甲基甲酰胺作溶剂,或样品中残留量低于检出限。
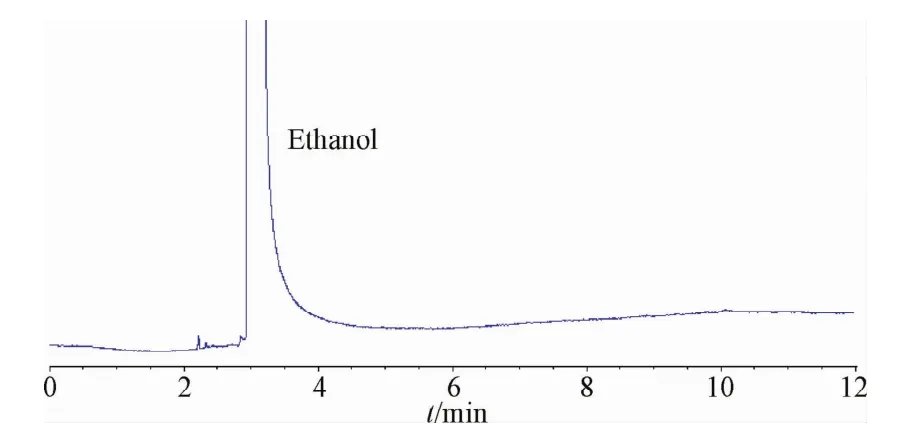
图2 供试品溶液色谱图Fig.2 The chromatography of sample solution
3 讨论
3.1 样品处理方式 依诺肝素钠除溶于水外,几乎不溶于任何有机溶剂,本研究曾采用纯化水作为溶剂,将供试品溶液直接进样,但色谱图中N,N-二甲基甲酰胺色谱峰对称性较差;本研究还曾采用纯化水作为溶剂,顶空进样,结果显示,N,N-二甲基甲酰色谱峰重现性较差,严重影响定量准确度。因此本研究最终选用乙醇萃取样品的方式,先用少量纯水将样品溶解,再加入乙醇使依诺肝素钠形成白色沉淀,而N,N-二甲基甲酰胺与水和乙醇都可互溶,可直接进样进行测定。该方法避免了样品基质对测定的干扰,配制样品过程水的用量较少,得到的色谱峰对称性较好,结果重现性较高。可见,与直接进样及顶空进样方式相比,乙醇萃取后直接进样的方式更有优势[10]。
3.2 色谱柱选择 本研究曾尝试选用中等极性的DB-624毛细管柱进行分离分析,但结果表明溶剂峰与主峰分离度不佳,考虑到N,N-二甲基甲酰胺极性较大,故选用改性聚乙二醇作为固定相的极性毛细管色谱柱DB-wax进行分析,分离度得到较大改善。
3.3 标准讨论 目前国内外药典中仅有欧洲药典(EP)8.0的那屈肝素钙[11]品种里规定了乙醇的检查项目,美国药典(USP)及EP其它种类 LMWH均未在正文中规定[11-13]。我国2006年颁布的依诺肝素钠国家标准YBH06762006中收载了甲醇、乙醇和二氯甲烷的检查项目,然而不同厂家在生产过程中使用的溶剂不同,除通用的甲醇、乙醇外,还会使用二氯甲烷或N,N-二甲基甲酰胺。本研究联合生产实际,在依诺肝素钠新版国家标准的草案中增加了N,N-二甲基甲酰胺的检查项目,并在其和二氯甲烷的检查项后面标注了“如使用”,检验时可根据企业实际使用的溶剂有针对性地进行测定。
[1] 李京,范慧红,徐康森.低分子肝素药用现状及质量标准概况[J].中国生化药物杂志,2004,25(1):53-55.
[2] Rahul G.Ingle,Asyush SA.A world of low molecular weight heparins(LMWHs)enoxaparin as a promising moiety-A review[J].Carbohy Polym,2014,106:148-153.
[3] King JT,DesaiUR.A capillary electrophoreticmethod for fingerprinting low molecular weight heparins[J].Anal.Biochem,2008,380:229-234.
[4] Bianchini P,Mascellani G.Few bicyclic acetals at reducing end of lowmolecular-weight heparins:might they restrict specification of pharmacopoeia? [J].Pharmeur Sci Notes,2005, 2005V22005N1:1-3.
[5] Wang B,Lucinda FB, li Al-Hakim,et al.Characterization of currently marketed heparin products:Analysis of heparin digests by RPIPUHPLC-QTOF-MS [ J].J.Pharm.BioChem Anal, 2012, 67-68:42-50.
[6] 李京,王悦,宋玉娟,等.低分子肝素注射剂质量评价[J].药物分析杂志,2013,33(10):1768-1773.
[7] 马光磊,俞孝珍.顶空气相色谱法检测依诺肝素钠原料药中有机溶剂残留[J].中国药业,2013,22(14):74-75.
[8] 许明哲,邹文博,薛晶,等.顶空气相色谱法测定头孢氨苄原料中的残留N,N-二甲基甲酰胺[J].药物分析杂志,2010,30(10):1876-1878.
[9] 中国药典.2010[S].二部:附录61.
[10] 马志华,赵焕荣,姬胜利.气相色谱法测定依诺肝素钠中N,N-二甲基甲酰胺的残留量[J].求医问药,2012,10(8):333-334.
[11] EP8.0[S].2014:2815-2817,2392-2394,1988-1989,2968,3430.
[12] EP 8.1[S].2014:3749-3750.
[13] USP37 NF32[S].2014:2792-2795.
(编校:吴茜)
Determ ination of residual N,N-dimethylformam ide(DM F)in enoxaparin sodium
WANG Yue,LI Jing,LIYing-ying,FAN Hui-hong△
(National Institute for Food and Drug Control,Beijing 100050,China)
Objective To establish amethod to quantify the residual DMF in enoxaparin sodium.Methods Enoxaparin sodium was precipitated by ethanol,meanwhile the DMFwas soluble,and was analyzed by direct injection.The Agilent DB-wax capillary column(30m×0.53mm,1.0μm)was adopted with high-purity nitrogen as the carrier gas,with a flow rate of3.0mL/min,the injector temperature was 200℃,FID detector temperature was 250℃,and the temperature-programmedmethod wasused.Results The linear range of DMFwas8.8~880μg/mL,the LOQwas11.6μg/mL,the LOD was 3.5μg/mL and the average recoveries(n=9)was94.8%.Conclusion The potential contamination from samplematrix could be avoided by using this sample preparation step.Thismethod is simple and accurate with high sensitivity and good repeatability,which could be used for quality control of trace DMF in enoxaparin sodium.
N,N-dimethylformamide;enoxaparin sodium;gas chromatography
TQ460.72
A
1005-1678(2014)06-0168-03
国家质量监督检验检疫总局公益性行业专项(2012104008-1-16)
王悦,女,助理研究员,研究方向:多糖类药物质量控制;范慧红,通信作者,女,研究员,研究方向:生化药物的质量控制,E-mail:shenghuayaoshi@126.com。

