新生儿红斑狼疮19例临床分析并文献复习
郝冬林,刘 晶,赵 岩,刘秋红,高忠恩
(中国医学科学院 北京协和医学院 北京协和医院风湿免疫科,风湿免疫病学教育部重点实验室,北京 100730)
新生儿红斑狼疮(neonatal lupus erythematosus,NLE)由McCuistion和Schoch[1]于1983年首次报道,系由于系统性红斑狼疮(systemic lupus erythematosus,SLE)或干燥综合征(Sjogren’s syndrome,SS)等结缔组织病母亲体内抗Ro/SSA和抗La/SSB抗体经胎盘传递至胎儿体内而诱导新生儿发生红斑狼疮样皮肤、血液系统、肝脏损害和先天性心脏传导阻滞(congenital heart block,CHB)的一种少见的获得性自身免疫性疾病。现将北京协和医院1990年1月至2013年6月收治的19例NLE患儿临床特点及诊治情况总结如下。
资料和方法
临床资料
回顾性分析1990年1月至2013年6月北京协和医院风湿免疫科和儿科就诊的19例NLE患儿病历资料,详细记录其临床表现、实验室检查(血常规、肝肾功能、自身抗体水平)、心电图、心脏彩超、诊治和随访情况,以及患儿母亲病史、自身抗体水平。抗核抗体(anti-nuclear antibody,ANA)采用间接免疫荧光法检测,抗可提取性核抗原抗体(extractable nuclear antigen,ENA)采用免疫双扩散和印迹法。
NLE诊断标准
诊断参考文献[2],满足下述任何一条标准即可诊断为NLE:(1)新生儿出现CHB,同时伴有母亲或(和)新生儿抗Ro/SSA和(或)抗La/SSB抗体阳性。(2)新生儿出现皮肤科专科医师和(或)组织病理学确定的与NLE相关的皮肤损害,同时伴有新生儿或母亲抗Ro/SSA和(或)抗La/SSB抗体阳性。
结 果
一般情况
19例NLE患儿中胎儿2例,婴儿17例(男婴10例,女婴7例)。2例胎儿分别在孕19周及22周时发
病。所有17例出生婴儿起病时间在出生后1~30 d,胎龄最短为35周+2 d,最长为39周+6 d,平均为(37.4±1.7)周;体重为1 820~3 470 g,平均(2 772±477) g。19例NLE患儿母亲10例为胎次(G)1产次(P)1,5例为G2P1,1例为G3P1,1例为G4P1,1例为G2P0,1例为G1P0,既往均无NLE史。
临床表现
皮肤损害:19例患儿中,15例(78.94%)出现皮肤狼疮损害,出现时间为1~30 d;其中,10例在出生时伴皮疹,余5例分别在出生后第5、7、10、22、30天出现狼疮样皮疹,皮疹多分布于面部、头皮、颈部等易暴露部位,亦出现躯干和四肢等非暴露部位,少数可累及到脚底心。主要表现为高于皮肤,大小不等的圆形、环形或半环形暗红色或鲜红斑,部分中央萎缩,可有鳞屑样变,呈散发或融合成片(图1)。15例患儿皮疹于出生后2~8个月完全消失(表1)。
心脏损害:19例患儿中,10例(52.63%)出现心脏受累;其中,1例动脉导管未闭,7例房间隔缺损,同时伴左房轻度增大者1例,右室增大者1例;1例婴儿心电图提示Ⅲ度房室传导阻滞(atrioventricular block,AVB);1例患儿母亲在孕19周时行胎儿超声心动图发现其Ⅲ度AVB;1例在孕22周时发现心动过缓,心率66次/min(表1)。
血液系统损害:血液系统受累者9例(9/19,47.37%),5例表现为外周血小板计数减少,最低降至68×109/L;4例出现新生儿贫血,最低血红蛋白水平为78 g/L;9例患儿外周血白细胞计数均正常。
肝损害:肝功能异常者5例(5/19,26.32%),天冬氨酸转氨酶(aspartate aminotransferase,AST)为71~183 U/L,丙氨酸转氨酶(alanine transaminase,ALT)为108~159 U/L;胆红素一过性升高者2例(表1)。
中枢神经系统损害:1例患儿在出生27 d出现间断性发作双眼凝视、四肢抽搐(表1)。
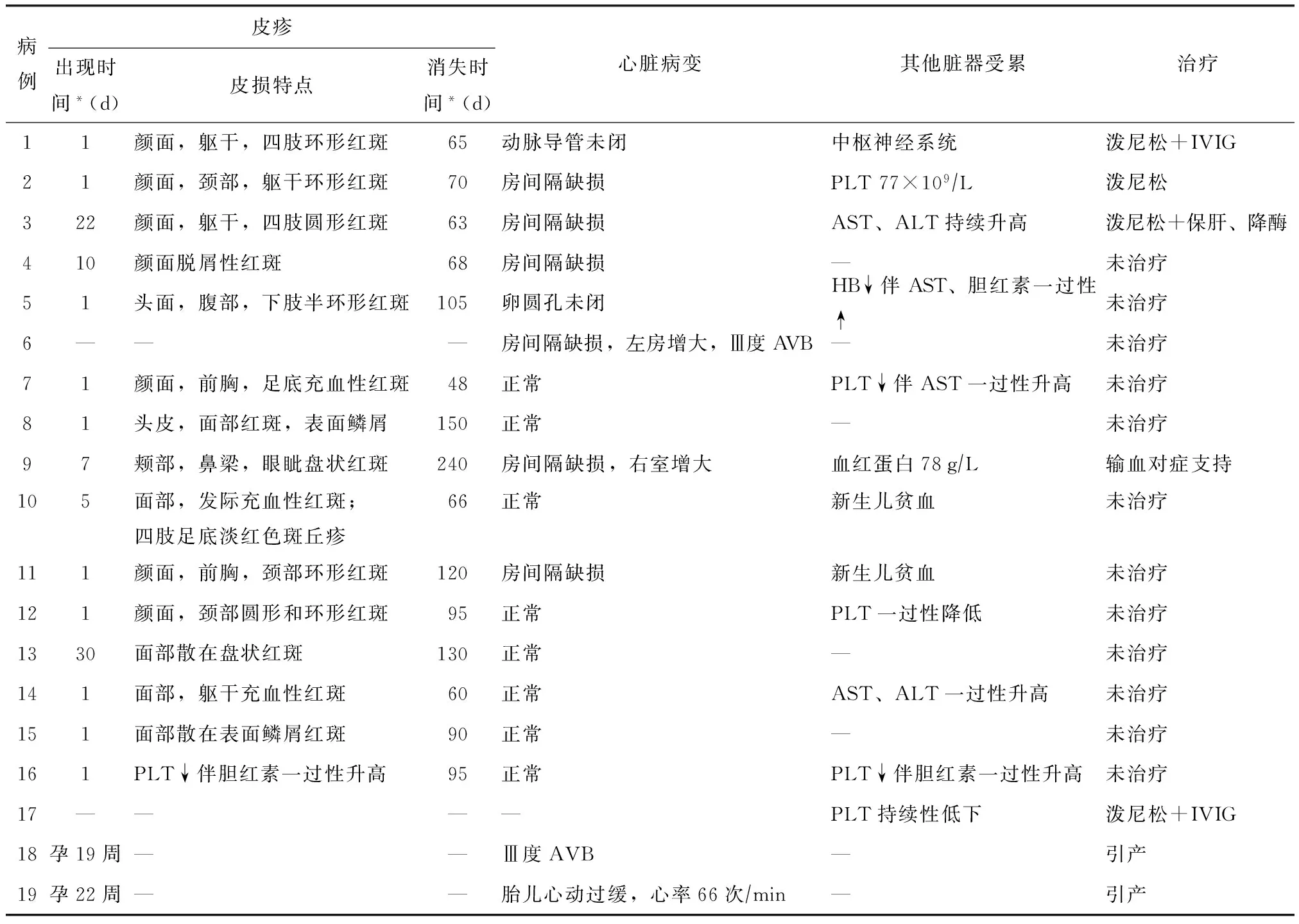
表1 19例新生儿红斑狼疮患儿临床表现及治疗情况
*皮疹出现和消失时间以出生后时间计;AVB:房室传导阻滞;IVIG:静脉用人免疫球蛋白;PLT:血小板计数;ALT:丙氨酸转氨酶;AST:天冬氨酸转氨酶;↑:升高;↓:降低
母婴免疫学指标
所有患儿及其母亲抗核抗体(antinuclear antibody,ANA)均阳性,抗体滴度为1∶160~1∶1 280。患儿母亲抗SSA抗体阳性者19例,抗SSA和抗SSB抗体均阳性者14例,抗SM抗体阳性者4例,抗核糖核蛋白(ribose nuclear protein,RNP)抗体阳性者1例,抗双链DNA(double-stranded DNA,ds-DNA)抗体阳性者4例。患儿抗SSA抗体阳性者19例,抗SSA和抗SSB抗体均阳性者12例,抗SM抗体阳性者3例,抗RNP抗体阳性者1例,抗ds-DNA抗体阳性者2例,抗血小板抗体阳性者1例(例17),所有患儿抗体均在出生后3~10个月消失(表2)。
患儿治疗情况
所有患儿和母亲避免日光曝晒。17例出生患儿中12例未接受治疗。5例患儿接受药物治疗,其中,1例因新生儿贫血(血红蛋白水平78 g/L)给予输血对症支持和口服硫酸亚铁;1例皮疹较重伴外周血小板计数降低予口服泼尼松(2.5 mg,1次/d,共用21 d);1例肝功能持续升高,排除嗜肝病毒感染后加用泼尼松(5 mg,1次/d,逐渐减量,共用5个月)并联合保肝降酶治疗;1例外周血小板持续低下,检查提示血小板抗体阳性,给予静脉应用人免疫球蛋白(400 mg/kg,1次/d,共用5d)联合泼尼松(5 mg,1次/d)治疗,激素逐渐减量,共用5个月;1例中枢神经系统受累患儿给予静脉应用人免疫球蛋白(400 mg/kg,1次/d,共用5 d)联合泼尼松(2.5 mg,3次/d),激素逐渐减量,共治疗6个月(表1)。
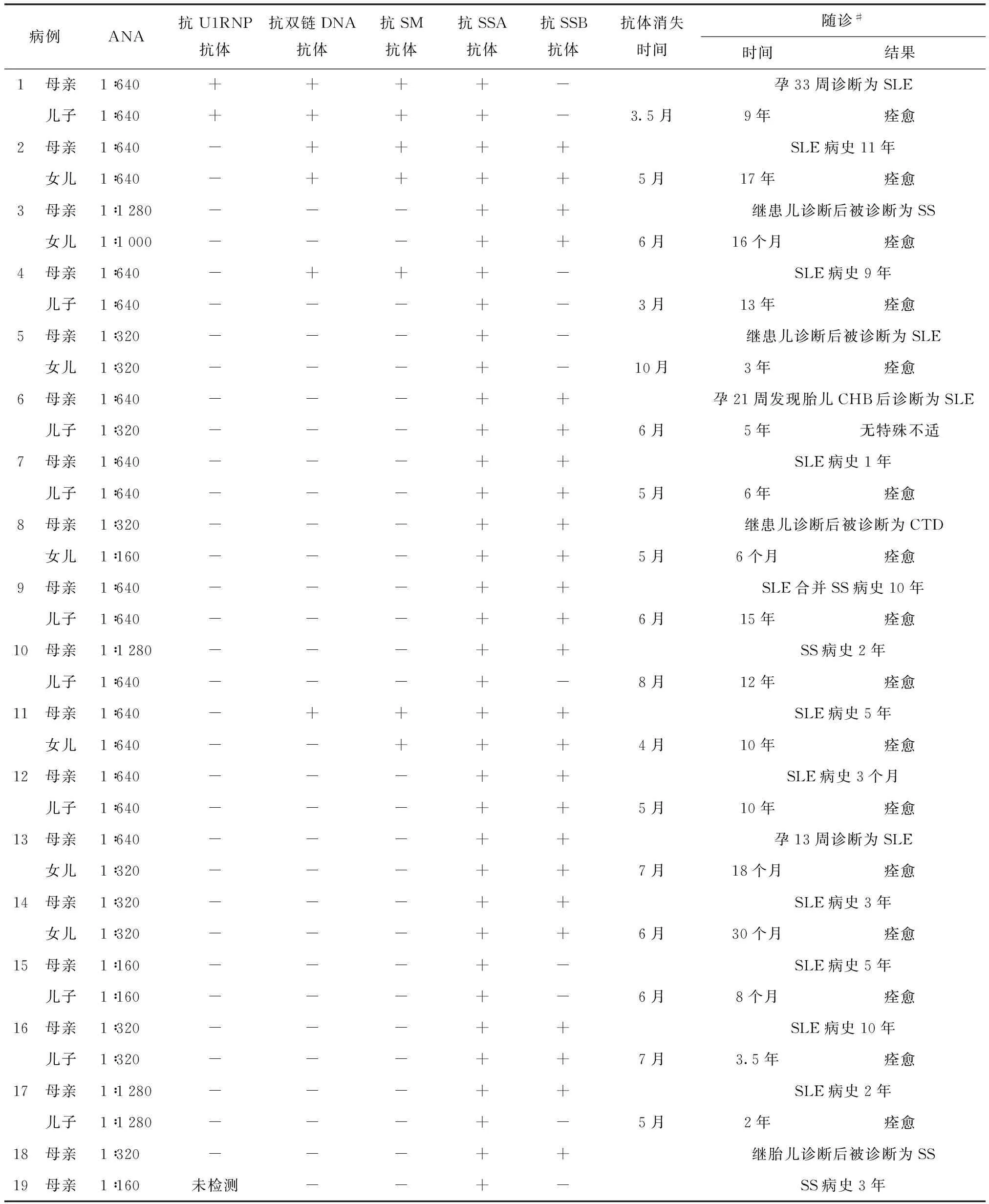
表2 19例新生儿红斑狼疮患儿及其母亲自身抗体特征及随诊情况
RNP:核糖核蛋白;SLE:系统性红斑狼疮;SS:干燥综合征;CHB:先天性心脏传导阻滞;CTD:结缔组织病;引产无胎儿记录;#随诊中母亲情况为怀孕前或孕期状态
母婴随访结果
17例出生患儿随访时间为3个月~17年,患儿全部好转,与正常儿童无异。8例心脏受累患儿在随诊中复查心脏彩超均正常;其中,Ⅲ度AVB患儿,截止投稿日期5岁,未安装心脏起搏器,无特殊不适(表2)。
19例患儿母亲在孕前诊断为系统性红斑狼疮(systemic lupus erythematosus,SLE)者12例,干燥综合征(Sjogren’s syndrome,SS)者2例;2例母亲在孕12周和33周分别出现面部新鲜皮疹、关节炎和蛋白尿增多,考虑为SLE疾病活动,经泼尼松(50 mg,1次/d)和羟氯喹(0.2 g,2次/d)治疗后好转;其余10例母亲孕期持续服用小剂量泼尼松(≤15 mg,1次/d);1例SS母亲孕期未服用任何药物治疗。5例母亲在患儿诊断为NLE后被诊断,其中2例为SS,1例为结缔组织病,服用羟氯喹治疗;2例SLE服用小剂量激素和羟氯喹治疗(表2)。
讨 论
NLE是由于母体所含抗SSA,抗SSB和(或)抗U1RNP抗体经胎盘进入胎儿体内,诱导胎儿或者婴儿发生红斑狼疮样皮疹和(或)心脏房室传导阻滞等临床表现的一种少见的获得性自身免疫性疾病[3]。由McCuistion和Schoch等于1954年首次报道,而国内在20世纪80年代后期开始报道,多见于出生后3个月以内的婴儿。据统计,美国NLE发病率为1/20 000[4],我国对其发病率的统计还未有报道。男女比例为1∶2.3[5],患儿性别无明显差异。
NLE发病机制并不确切,目前认为其发病与母体抗Ro/SSA、抗La/SSB抗体经胎盘进入胎儿体内,形成抗原抗体复合物,诱导胎儿组织损伤的关系最密切[6],也有少数病例显示由母体U1RNP抗体导致[7]。其中抗体Ro靶抗原最重要的是Ro52 KD(相对分子质量52 000)和Ro60 KD(相对分子质量60 000)两种蛋白质,而La抗原中相对分子质量为48 000的蛋白质更具特异性[8]。其他致病机制亦要考虑,如心肌细胞凋亡,自身抗体与心脏组织的交叉反应,T细胞功能失调和抑制性受体,母体微嵌合体,与遗传易感性等因素[9]。本研究患儿及母亲ANA和抗SSA抗体均阳性,但抗SSB抗体母亲14例,患儿11例,且患儿亦存在抗SM抗体和抗ds-DNA抗体阳性,表明母亲除抗SSA、抗SSB抗体及抗U1RNP抗体外,其他抗体亦可通过胎盘传给胎儿,但也并非母体所有抗体都会传给胎儿。
NLE最突出的临床表现是皮肤和心脏损害。国外报道,皮肤损害发生率约为50%,心脏以CHB损害多见,约占30%~50%[6,10]。我国NLE皮疹发生率为77.7%,明显高于国外报道,心脏损害发生率为24.5%[11]。本研究出现皮损者15例,心脏受累者10例且多以心脏结构异常为主,CHB者3例,这可能是由于对抗SSA、抗SSB抗体阳性怀孕母亲监测不足,尤其是胎儿CHB筛查不足,且多数NLE首诊症状为皮疹,因此导致数据与国外文献报道不同。NLE患儿皮疹一般发生在出生时或出生后2个月内,平均在出生后6周发生。本研究10例(66.67%,10/15)在出生时出现皮损,5例在出生30 d内出现。皮疹具有光敏现象,多见于颜面、头皮、躯干、四肢、亦可见于手足心;表现为高出皮面的不规则圆形、环形、半环形红斑,中间色淡,表面有鳞屑。皮肤病理为表皮及真皮连接部位出现退化,血管周围淋巴细胞浸润;直接免疫荧光显示,在角质形成细胞及基底膜周围出现免疫沉积物[6]。多数皮疹未经治疗可自行缓解,偶有皮肤色素沉着。临床研究显示,母体抗SSA和抗SSB抗体在孕12周经胎盘传递到胎儿循环,造成胎儿心脏传导系统免疫损伤,约在孕期18~24周形成CHB[12]。在一些病例中,AVB开始表现为Ⅰ度或Ⅱ度,并最终进展为Ⅲ度[13]。一旦出现Ⅲ度AVB,病变不可逆,60%以上患儿需安装永久性起搏器。本研究中1例Ⅲ度AVB患儿未装起搏器,目前无不适。
除皮肤和心脏病变外,约10%~20%NLE患儿出现血液系统异常,表现为外周血小板、白细胞计数减少及溶血性贫血等;9%可出现肝胆受累,多为黄疸、肝功能异常、高胆红素血症。国内研究显示,94例NLE患儿中血液系统异常者46.8%,出现肝胆损害者31.9%,可单独存在或合并其他脏器损害,但均不严重,多表现为一过性损害[11]。本研究显示,血液系统受累9例(47.37%),5例为外周血小板计数减少,4例为新生儿贫血,发病率高于国内外报道;而出现肝功能异常者5例(26.32%),胆红素一过性升高者2例,皮肤轻度黄染者2例。
NLE与SLE不同,几乎不累及肾脏。国内尚无相关报道,国外文献报道1例NLE出现膜性肾小球肾炎,提示来自母体自身抗体可致新生儿发生肾小球肾炎[14];中枢神经系统受累少见,杨群等[15]报道2例NLE患儿出现中枢神经系统损害,1例表现为睡眠脑电图异常,另1例为脑室周围白质异常,均未予治疗且随访1年后均正常。本研究未见患儿出现肾脏受累;有1例在出生21 d出现四肢抽搐、双眼凝视等症状,经激素和静脉应用人免疫球蛋白好转,1年后随访正常。说明NLE中枢神经系统受累可能是暂时的,可随着年龄增长改善,但需密切随访和观察。
多数NLE患儿预后良好,对于仅有皮肤损害或内脏受累轻者可不予治疗,避光观察即可。内脏损害明显,如外周血小板计数降低、肝功能持续异常、中枢神经系统受累可予以对症支持、短期糖皮质激素和(或)人免疫球蛋白治疗。对于CHB患儿,应先动态观察,然后再决定是否安装永久性起搏器。国外报道,部分母亲在分娩NLE患儿时无症状,后1/3发生自身免疫性疾病。Martin等[16]对49例8岁以上曾患NLE患儿随访发现,6例患儿出现自身免疫性疾病(2例幼年类风湿性关节炎,2例银屑病,1例桥本氏病,1例先天性甲状腺功能不全合并肾病综合征)。本研究5例患儿(26.31%)接受药物治疗,12例(63.15%)仅观察随诊,最终都与正常儿童无异。患儿母亲在分娩前有12例诊断为SLE,2例为SS,5例在婴儿诊断NLE后随诊(2例SS,1例CTD,2例SLE)。故对NLE母子均需要做长期随访。
抗SSA和抗SSB抗体阳性母亲的胎儿的NLE患病率约为1%,可通过服用羟氯喹降低发生率[17]。若既往曾分娩过NLE患儿,妊娠妇女再次分娩NLE患儿的发生率可达25%,通过产前超声检查和胎儿心电图早期发现胎儿是否存在心脏AVB,也可在怀孕8~12周使用人免疫球蛋白(20 g,3~5 d)阻断母亲抗SSA和抗SSB抗体通过胎盘传给胎儿,从而降低CHB发生率[18]。若发现胎儿已出现CHB,要及早联合使用可穿透胎盘、在胎儿体内以活性形式存在被利用的地塞米松和人免疫球蛋白,使部分胎儿AVB恢复正常。但由于地塞米松的潜在不良反应,故不作为常规预防使用。
对于含有抗SSA和(或)抗SSB抗体阳性的母亲,怀孕期间应密切监测胎儿心脏变化,而对于NLE及其母亲都应该长期随访,警惕自身免疫性疾病的发生。
(本文图1见插页Ⅱ)
[1]McCuistion CH,Schoch EP Jr.Possible discoid lupus erythematosus in newborn infant.Report of a case with subsequent development of acute systemic lupus erythematosus in mother[J].Arch Dermatol,1983,119:615- 618.
[2]Lee LA.Cutaneous lupus in infancy and childhood[J].Lupus,2010,19:1112-1117.
[3]Johnson B.Overview of neonatal lupus[J].J Pediatr Health Care,2014,28:331-341.
[4]Buyon JP,Clancy RM.Neonatal lupus syndromes[J].Curr Opin Rheumatol,2003,15:535-541.
[5]Brucato A,Buyon JP,Horsfall AC,et al.Fourth international workshop on neonatal lupus syndr-omes and the RoSSA-LaSSB system[J].Clin Exp Rheumatol,1999,17:130-136.
[6]Boh EE.Neunatal lupus erythematosus[J].Clin Dermatol,2004,22:125-128.
[7]Heelan K,Watson R,Collins SM.Neonatal lupus syndrome associated with ribonucleoprotein antibodies[J].Pediatr Dermatol,2013,30:416- 423.
[8]蒋明,张奉春.风湿病诊断与诊断评价[M].上海:科技术出版社,2004:36-37.
[9]Chang C.The pathogenesis of neonatal autoimmune and autoinflammatory diseases:comprehensive review[J].J Autoimmun,2013,41:100-110.
[10] Lee LA.Transient autoimmunity related to maternal autoantibodies:neonatal lupus[J].Autoim-mun Rev,2005,4:207-213.
[11] 李玲,董光富,韩凤珍,等.新生儿红斑狼疮7例报告并87例文献复习[J].中华儿科杂志,2011,49:146-150.
[12] Garcia S,Campos-de-Carvalho AC.Neonatal lupus syndrome:the heart as a target of the immune system[J].An Acad Bras Cienc,2000,72:83-89.
[13] Buyon JP,Clancy RM.From antibody insult to fibrosis in neonatal lupus-the heart of the matter[J].Arthritis Res Ther,2003,5:266-270.
[14] Lam C,lmundo L,Hirsch D,et al.Glomerulonephritis in a neonate with atypical congenital lupus and toxoplasmosis[J].Pediatr Nephrol,1999,13:850-853.
[15] 杨群,邵肖梅,曹云,等.新生儿狼疮八例分析[J].中华儿科杂志,2008,46:18-21.
[16] Martin V,Lee LA,Askanase AD,et al.Long-term follow up of children with neonatal lupus and their unaffected siblings[J].Arthritis Rheum,2002,46:2377-2383.
[17] Izmirly PM,Kim MY,Llanos C,et al.Evaluation of the risk of anti-SSARo-SSBLa antibody-associated cardiac manifestations of neonatal lupus in fetuses of mothers with systemic lupus erythematosus exposed to hydroxychloroquine[J].Ann Rheum Dis,2010,69:1827-1830.
[18] Brucato A.Prevention of congenital heart block in children of SSA-positive mothers[J].Rheumatology(Oxford),2008,47:35-37.

