移植后糖尿病
谢轲楠 综述 陈劲松 审校
随着手术技术和各种免疫抑制剂的发展,实体器官移植的数量和存活受者数量均逐年提高。器官移植受者的生存时间延长,代谢性疾病(如糖尿病、脂代谢异常、肥胖、代谢综合征等)的发生率也随之升高[1]。对移植受者进行代谢性疾病的管理,目的在于减少患者的发病率和病死率,防止或延缓代谢性疾病相关的心血管疾病发生率和死亡率。
从1964年[2]首次报道肾移植后糖尿病以来,移植后糖尿病(PTDM)的研究不断推进。PTDM是器官移植后常见的并发症,增加受者心血管疾病的发生率和死亡率,并且增加移植器官的丢失[3]。因此,明确PTDM的危险因素、早期诊断、有效管理非常重要。本篇综述将着重介绍PTDM的诊断、危险因素、治疗和管理。
诊 断
2003年,移植后新发糖尿病(NODAT)的首个指南由多个相关领域的专家组成的国际性的专家委员会制订[4]。该指南仅制订了肾移植后NODAT的诊断标准,但也被其他器官移植领域广泛借鉴。该指南参照美国糖尿病协会(ADA)、世界卫生组织(WHO)关于非移植人群的糖尿病诊断标准,定义NODAT的诊断标准:至少1次空腹血糖≥7 mmol/L,随机血糖≥11.1 mmol/L且有症状,或口服葡萄糖耐量试验(OGTT)中2 h血糖≥11.1 mmol/L。
2014年,经过专家委员会讨论,第2个国际指南发表,肾移植受者高血糖的诊断仍沿用ADA制订的糖尿病和糖尿病前期的诊断标准(表1),但对于疾病名称和诊断时机等进行了重大更新[5]。
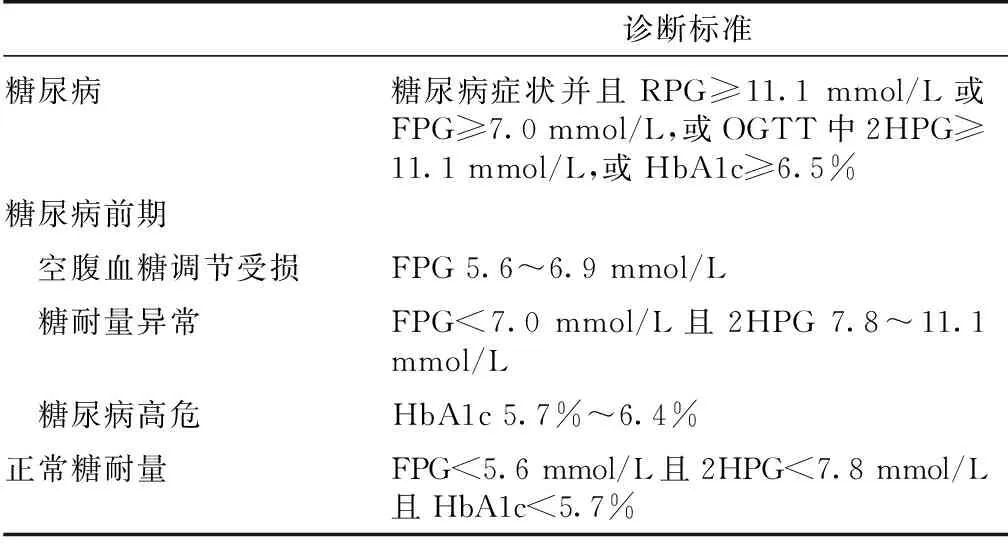
表1 ADA制定的糖尿病和糖尿病前期诊断标准
ADA:美国糖尿病协会;RPG:随机血糖,一天中无论上次进餐时间的任意时刻血糖;FPG:空腹血糖,指至少8 h无热卡摄入;2HPG:餐后2 h血糖;OGTT:口服葡萄糖耐量试验;HbAlc:糖化血红蛋白;糖尿病症状:多尿、多饮和体重减轻
该指南将“移植后新发糖尿病(NODAT)”更名为“移植后糖尿病(PTDM)”。取消“新发”这个冠名,是因为即使很多患者在移植后才诊断为糖尿病,也不能确定糖尿病是移植后新发生的。移植之前糖尿病的诊断与否,很大程度上与不同中心的筛查方法有关。多数中心仅采用空腹血糖和糖化血红蛋白(HbA1c)筛查移植前受者,这两种方法敏感度明显低于OGTT试验。因此,并不能明确移植受者术后出现的糖尿病是否为“新发”,故2014年指南更改为“移植后糖尿病”。
该指南首次提出了诊断PTDM的时间界定。2003年指南并未排除移植早期、仍在住院并接受大剂量糖皮质激素治疗的患者。由于移植早期大剂量使用糖皮质激素且住院期间血糖监测频繁,很多患者出现糖耐量异常或达到糖尿病诊断标准,但随着身体状态改善、运动量增加和糖皮质激素用量减少,这种高血糖状态可恢复正常。因此,新指南建议,推迟PTDM的诊断时间到患者出院之后、状态稳定且免疫抑制方案调整到日常维持剂量时。
此外,是否采用HbA1c作为PTDM的诊断标准。由于移植后早期常见血红细胞计数(RBC)减低,认为在移植后最初12个月,HbA1c不能准确反映血糖升高。专家委员会建议,HbA1c升高(≥6.5%)可作为PTDM的诊断标准,但不应作为移植1年内唯一的实验室诊断标准。
危险因素
PTDM和2型糖尿病(T2DM)的发病机制相似,都与胰岛素抵抗相关,但PTDM还存在由免疫抑制剂造成的胰岛β细胞功能障碍及其移植相关的危险因素(图1)[6]。
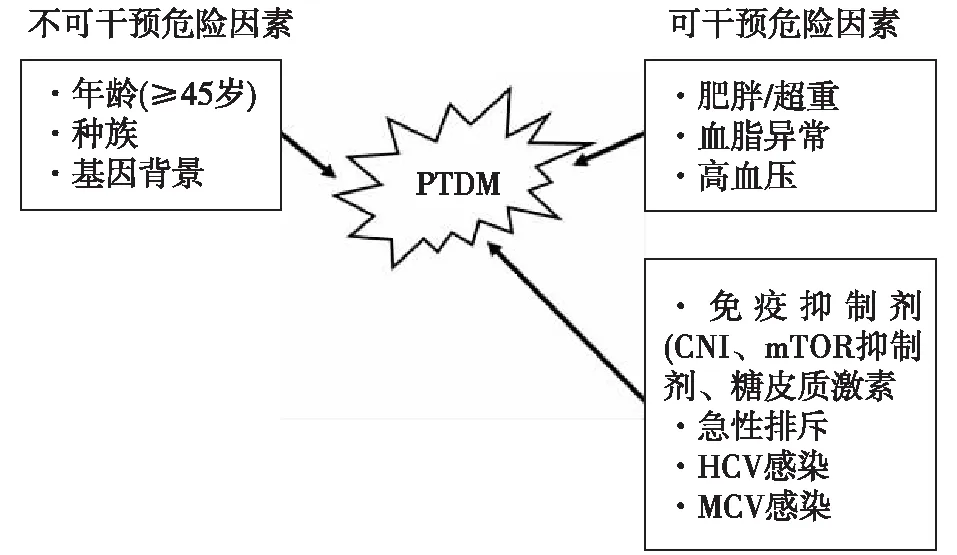
图1 PTDM的危险因素PTDM:移植后糖尿病;CNI:钙调神经磷酸酶抑制剂;mTOR:哺乳动物雷帕霉素靶蛋白;MCV:巨细胞病毒;HCV:丙型肝炎病毒
年龄与T2DM相似,高龄也是PTDM的危险因素,特别是移植时的高龄受者。有研究报道[7],受者年龄>45岁,PTDM发生风险随年龄增加而增加。与18~44岁的受者相比,年龄≥60岁的受者PTDM风险增加160%[8]。高龄不仅增加PTDM风险,还增加PTDM患者血糖控制的难度。
基因背景回顾性研究报道,与无糖尿病家族史患者相比,有糖尿病家族史的患者PTDM发生风险增加7倍。父母中一方患糖尿病的受者,发生PTDM的风险更高[9]。
PTDM的发病率在不同种族人群存在明显差异。美国肾脏病数据系统(URDS)的分析报告显示,与高加索人相比,非裔美国人发生PTDM的相对风险增加68%,西班牙裔增加35%[8]。近期有研究报道,南亚人种比高加索人PTDM发生率高(5年累积发病率 35%vs10%,HR 4.2,95%CI 2.4~8.5)[10]。
除种族差异之外,很多特定基因和单核苷酸多态性(SNP)与PTDM的发生相关。研究发现,导致T2DM的TCF7L2、SLC30A8、HHEX、CDKAL1、CDKM2A/B、KCNQ1基因突变,也与PTDM有关[11]。血管紧张素原基因编码的SNP增加PTDM的风险[12]。钙调神经磷酸酶抑制剂(CNI)的靶基因是活化的T细胞的核因子转录因子,同样也调节胰岛素产生,从而影响服用CNI类药物受者的血糖[13]。有研究发现[14],SLC30A8 rs13266634基因突变与PTDM的易感性有关,该基因编码胰岛β细胞特异性锌转运体8(ZnT-8)。
肥胖肥胖是公认的T2DM危险因素,同样也增加PTDM风险。据报道[15],移植后1年或半年内,患者体重增加10%~20%。体重增长的原因可能为进食增加、运动减少和使用糖皮质激素。除移植后体重增加之外,患者移植前肥胖也是PTDM的一个重要危险因素。有研究发现[15],体质量指数(BMI)≥30 kg/m2,PTDM的发生风险增加73%(P<0.001)。移植后1年BMI>25 kg/m2,PTDM的发生风险与BMI的增加呈平行关系。除体重外,体脂含量的增加会导致外周胰岛素抵抗。一项前瞻性研究报道[16],与没有代谢综合征的患者相比,移植前存在代谢综合征的患者PTDM患病率增加(P<0.001)。
丙型肝炎病毒(HCV)感染HCV感染和PTDM的关联已经在肾移植和肝移植受者中被充分证实[17-18]。具体机制尚未完全明确,可能的危险因素有炎症细胞因子、氧化应激、肝脏的胰岛素抵抗、胰岛β细胞功能障碍。有研究报道[19],慢性丙肝患者,根除HCV感染能够使空腹血糖调节受损(IFG)和T2DM的发生率降低约50%(HR 0.48,95%CI 0.24~0.98,P=0.04)。
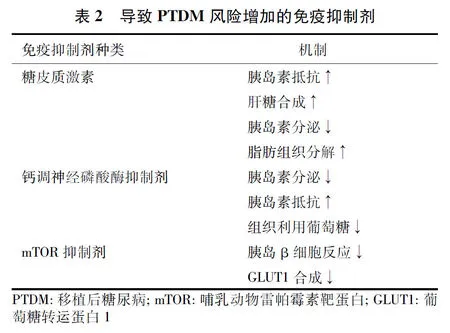
免疫抑制剂实体器官移植受者的免疫抑制治疗是防止排斥反应所必需的。尽管有多种免疫抑制方案可供选择,但目前常用的方案往往包括糖皮质激素、CNI类药物(他克莫司、环孢素)和哺乳动物雷帕霉素靶蛋白(mTOR)抑制剂,均可增加PTDM的风险(表2)。
糖皮质激素升高血糖的机制主要有:刺激肝糖原异生、抑制外周组织对葡萄糖的摄取和利用、增加肝糖原合成,对胰高血糖素、肾上腺素及生长激素的升糖效应有允许和协同作用,降低肾小管对葡萄糖的重吸收等。其升高血糖的作用呈剂量相关性。一项多中心的前瞻性双盲随机对照队列研究显示[20],联合使用霉酚酸酯和他克莫司的受者,早期撤除糖皮质激素(移植7d以内)与持续使用低剂量糖皮质激素(5 mg/d)相比,随访5年后移植肾远期预后和心血管疾病的危险因素相似,但早期撤除糖皮质激素的患者,需要胰岛素治疗的比例低于持续使用低剂量糖皮质激素的患者。另一项多中心研究[21],将联用环孢素、麦考酚钠和巴利昔单抗的肾移植受者,随机分为不使用激素、早期撤除激素(移植7d后)和标准剂量激素(泼尼松5~10 mg/d)3组,发现前两组需要降糖药物治疗的PTDM患者少,且其他激素相关的副作用发生率更低。虽然早期撤除激素或不使用激素对减少高血糖有益,但增加排斥风险。建议根据受者具体情况,权衡糖皮质激素使用的利弊。
CNI类药物具有剂量相关的升高血糖作用[8]。CNI类药物引起胰岛素抵抗,并且具有胰腺毒性,可导致胰岛素分泌下降。此外,有研究报道[22],CNI类药物减少人类脂肪细胞表面葡萄糖转运蛋白4(GLUT4),不依赖胰岛素信号通路方式抑制葡萄糖摄取。既往研究显示[23],他克莫司比环孢素更能加重PTDM进展,将他克莫司切换为环孢素,能够改善PTDM患者的空腹血糖。但上述研究存有争议:该研究中他克莫司的目标浓度较高(10~15 ng/ml),并且只监测了6个月的血糖。
西罗莫司(雷帕霉素)是mTOR抑制剂,也被证实可增加PTDM风险。西罗莫司可抑制胰岛素信号通路和GLUT1合成,并且影响胰岛β细胞的应答[24]。一项美国全国范围的研究显示[25],联合使用西罗莫司和CNI类药物的肾移植受者,PTDM的风险最高(HR 1.66,95%CI,1.42~1.93;环孢素和霉酚酸酯/硫唑嘌呤作为对照)。与他克莫司+霉酚酸酯/硫唑嘌呤相比,西罗莫司+他克莫司的免疫抑制方案使PTDM的风险增加约20%(HR 1.19,95%CI 1.02~1.37),表明西罗莫司是PTDM的独立危险因素。
他汀类降脂药器官移植受者的脂代谢异常发生率较高,他汀类药物是治疗的首选。研究发现[26],他汀类药物增加发生糖尿病的风险。一项Meta分析的结果显示[27],他汀类降脂药使糖尿病的风险增加9%。有研究报道[28-29],他汀类药物与肾移植和肝移植受者IFG和PTDM有关。他汀类药物之中,阿托伐他汀导致PTDM的风险最高(与氟伐他汀相比,HR 2.21,95%CI,1.02~4.76),普伐他汀、氟伐他汀、匹伐他汀是肾移植受者比较安全的降脂药[30]。
治疗和管理
PTDM的管控应开始于移植前对高危患者的筛查、移植后的生活方式指导、血糖监测,并延伸至糖尿病并发症、心血管事件的筛查和干预。移植后代谢性疾病的管理是一个系统性工作,需要内科医师和患者共同参与。
移植前筛查移植前所有患者均应评估糖尿病危险因素,询问糖尿病病史和家族史。反复检测空腹血糖和OGTT,以发现糖耐量异常(IGT)。文献报道[31],IFG和IGT的患者,发生PTDM的风险比正常患者增加2.5倍。PTDM的高危患者,应当调整生活方式。胰岛素抵抗和肥胖的患者,药物首选二甲双胍,可延缓糖尿病的发生。
移植后管理由于大剂量使用糖皮质激素,移植后1周时约66%的患者出现高血糖[32]。在免疫抑制剂调整至维持剂量之前,建议监测血糖。由大剂量糖皮质激素、手术应激、术后疼痛导致的高血糖,推荐使用胰岛素[33]。严格控制血糖有引发低血糖的风险,住院患者建议参考以下目标[33]:监护中患者,随机血糖控制在7.8~10 mmol/L;普通病房患者,空腹血糖<7.8 mmol/L,餐后血糖<10 mmol/L。出院之后,血糖控制目标是空腹血糖5~7.2 mmol/L,餐后≤10 mmol/L。PTDM最易发生在移植后的6个月之内,因此,这段时间需定期严密监测血糖。患者移植之后,应当进行生活方式指导。
药物治疗选择降糖药和调整免疫抑制方案,需注意移植肾功能和药物的相互作用。根据ADA指南,PTDM治疗主要参考T2DM。但与T2DM相比,PTDM有其特殊性:患者同时服用免疫抑制剂,需注意药物的相互作用、在治疗中需评估和观察移植器官功能和排斥风险。应当针对患者和移植物情况,进行个体化治疗。
调整免疫抑制剂 PTDM或糖尿病前状态的受者,需注意抗排斥药物的减量和调整。关于免疫抑制剂的选择,并无明确的指南和推荐。免疫抑制剂需要个体化调整,关键是平衡高血糖和排斥的风险[5]。
口服降糖药 多种类型的口服降糖药可用于PTDM的治疗(表3)[6]。不同药物的作用机制和特点不同,需根据情况运用。还需指出的是,部分药物代谢途径和抗排斥药的代谢途径相似,需注意药物的相互作用,监测血糖和免疫抑制剂药物浓度。
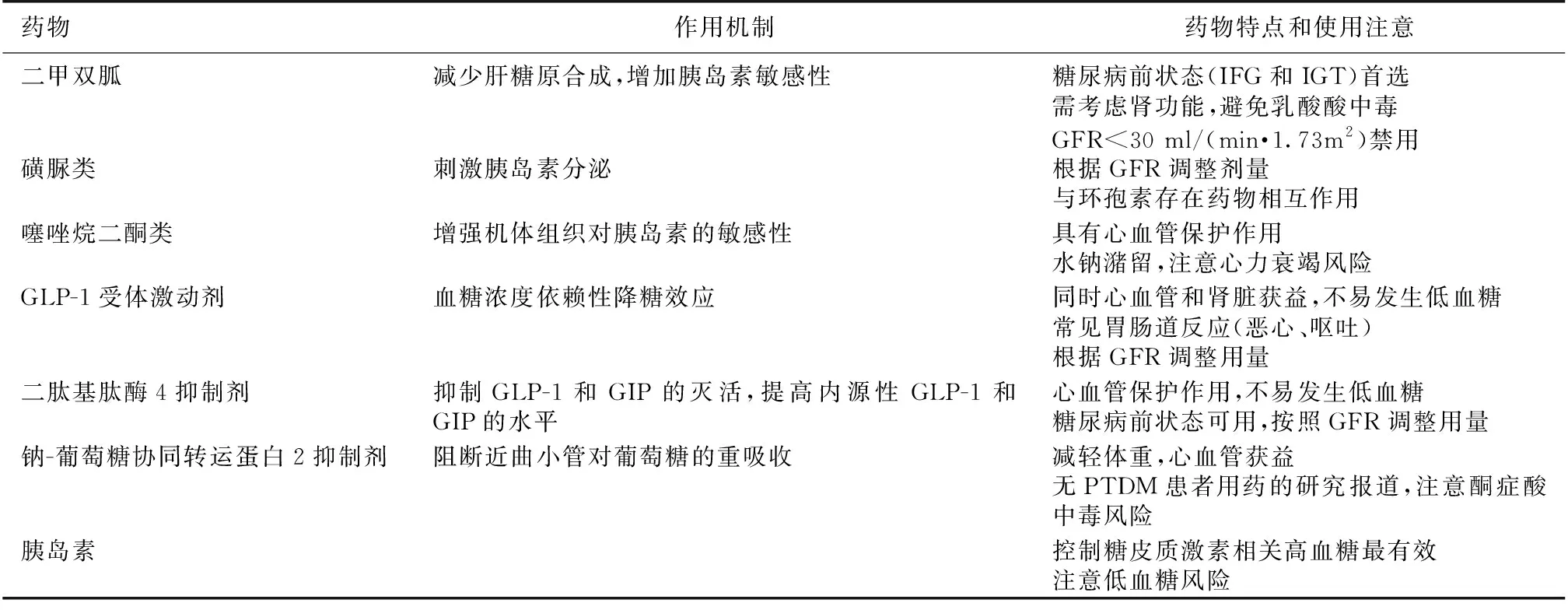
表3 PTDM的降糖药物[6]
PTDM:移植后糖尿病;IFG:空腹血糖调节受损;IGT:糖耐量异常;GLP-1:胰高血糖素样肽1;GFR:肾小球滤过率;GIP:葡萄糖依赖性促胰岛素分泌多肽
胰岛素 胰岛素对糖皮质激素导致的糖尿病最有效,且无需根据肾功能调整剂量。近期有随机、对照的临床研究报道[34],早期的基础胰岛素治疗(晚间血糖≥7.8 mmol/L即开始基础胰岛素治疗),能保护胰岛β细胞功能,将PTDM的风险降低73%。PTDM的治疗可选用胰岛素标准方案:基础胰岛素、基础+餐前胰岛素或混合方案。
小结:PTDM是实体器官移植后常见的并发症,增加心血管疾病的发生率和死亡率,并且增加移植物丢失率。移植前应当仔细评估PTDM的危险因素,包括高龄、基因背景、肥胖、HCV感染等。免疫抑制方案的选择方面,要平衡高血糖和排斥反应的利弊。所有的移植受者均应监测血糖。早期诊断、合理管理是治疗PTDM的关键。高危患者和已经诊断PTDM的患者,都应进行生活方式干预,包括饮食调整和锻炼。PTDM的管理与T2DM相似,但需考虑移植器官功能和药物的相互作用。
1 Bloom RD,Crutchlow MF.New-onset diabetes mellitus in the kidney recipient:diagnosis and management strategies.Clin J Am Soc Nephrol,2008,3 Suppl 2:S38-48.
2 Starzl TE,Marchioro TL,Rifkind D,et al.Factors in successful renal transplantation.Surgery,1964,56:296-318.
3 Wauters RP,Cosio FG,Suarez FML,et al.Cardiovascular consequences of new-onset hyperglycemia after kidney transplantation.Transplantation,2012,94(4):377-382.
4 Davidson J,Wilkinson A,Dantal J,et al.New-onset diabetes after transplantation:2003 International consensus guidelines.Proceedings of an international expert panel meeting.Barcelona,Spain,19 February 2003.Transplantation,2003,75(10 Suppl):SS3-24.
5 Sharif A,Hecking M,de Vries AP,et al.Proceedings from an international consensus meeting on posttransplantation diabetes mellitus:recommendations and future directions.Am J Transplant,2014,14(9):1992-2000.
6 Han E,Kim MS,Kim YS,et al.Risk assessment and management of post-transplant diabetes mellitus.Metabolism,2016,65(10):1559-1569.
7 Boudreaux JP,McHugh L,Canafax DM,et al.The impact of cyclosporine and combination immunosuppression on the incidence of posttransplant diabetes in renal allograft recipients.Transplantation,1987,44(3):376-381.
8 Kasiske BL,Snyder JJ,Gilbertson D,et al.Diabetes mellitus after kidney transplantation in the United States.Am J Transplant,2003,3(2):178-185.
9 Chakkera HA,Hanson RL,Raza SM,et al.Pilot study:association of traditional and genetic risk factors and new-onset diabetes mellitus following kidney transplantation.Transplant Proc,2009,41(10):4172-4177.
10 Peracha J,Nath J,Ready A,et al.Risk of post-transplantation diabetes mellitus is greater in South Asian versus Caucasian kidney allograft recipients.Transpl Int,2016,29(6):727-739.
11 Lee YH,Kang ES,Kim SH,et al.Association between polymorphisms in SLC30A8,HHEX,CDKN2A/B,IGF2BP2,FTO,WFS1,CDKAL1,KCNQ1 and type 2 diabetes in the Korean population.J Hum Genet,2008,53(11-12):991-998.
12 Tarnowski M,Suczanowska-Gabowska S,Pawlik A,et al.Genetic factors in pathogenesis of diabetes mellitus after kidney transplantation.Ther Clin Risk Manag,2017,13:439-446.
13 Sr L,Moon JY,Lee SH,et al.Angiotensinogen polymorphisms and post-transplantation diabetes mellitus in Korean renal transplant subjects.Kidney Blood Press Res,2013,37(2-3):95-102.
14 Khan IA,Jahan P,Hasan Q,et al.Validation of the association of TCF7L2 and SLC30A8 gene polymorphisms with post-transplant diabetes mellitus in Asian Indian population.Intractable Rare Dis Res,2015,4(2):87-92.
15 el-Agroudy AE,Wafa EW,Gheith OE,et al.Weight gain after renal transplantation is a risk factor for patient and graft outcome.Transplantation,2004,77(9):1381-1385.
16 Porrini E,Delgado P,Bigo C,et al.Impact of metabolic syndrome on graft function and survival after cadaveric renal transplantation.Am J Kidney Dis,2006,48(1):134-142.
17 Fabrizi F,Martin P,Dixit V,et al.Post-transplant diabetes mellitus and HCV seropositive status after renal transplantation:meta-analysis of clinical studies.Am J Transplant,2005,5(10):2433-2440.
18 Saliba F,Lakehal M,Pageaux GP,et al.Risk factors for new-onset diabetes mellitus following liver transplantation and impact of hepatitis C infection :an observational multicenter study.Liver Transpl,2007,13(1):136-144.
19 Simó R,Lecube A,Genescà J,et al.Sustained virological response correlates with reduction in the incidence of glucose abnormalities in patients with chronic hepatitis C virus infection.Diabetes Care,2006,29(11):2462-2466.
20 Woodle ES,First MR,Pirsch J,et al.A prospective,randomized,double-blind,placebo-controlled multicenter trial comparing early (7 day) corticosteroid cessation versus long-term,low-dose corticosteroid therapy.Ann Surg,2008,248(4):564-577.
21 Vincenti F,Schena FP,Paraskevas S,et al.A randomized,multicenter study of steroid avoidance,early steroid withdrawal or standard steroid therapy in kidney transplant recipients.Am J Transplant,2008,8(2):307-316.
22 Pereira MJ,Palming J,Rizell M,et al.Cyclosporine A and tacrolimus reduce the amount of GLUT4 at the cell surface in human adipocytes:increased endocytosis as a potential mechanism for the diabetogenic effects of immunosuppressive agents.J Clin Endocrinol Metab,2014,99(10):E1885-1894.
23 Rathi M,Rajkumar V,Rao N,et al.Conversion from tacrolimus to cyclosporine in patients with new-onset diabetes after renal transplant:an open-label randomized prospective pilot study.Transplant Proc,2015,47(4):1158-1161.
24 Pereira MJ,Palming J,Rizell M,et al.mTOR inhibition with rapamycin causes impaired insulin signalling and glucose uptake in human subcutaneous and omental adipocytes.Mol Cell Endocrinol,2012,355(1):96-105.
25 Johnston O,Rose CL,Webster AC,et al.Sirolimus is associated with new-onset diabetes in kidney transplant recipients.J Am Soc Nephrol,2008,19(7):1411-1418.
26 Ridker PM,Pradhan A,MacFadyen JG,et al.Cardiovascular benefits and diabetes risks of statin therapy in primary prevention:an analysis from the JUPITER trial.Lancet,2012,380(9841):565-571.
27 Preiss D,Seshasai SR,Welsh P,et al.Risk of incident diabetes with intensive-dose compared with moderate-dose statin therapy:a meta-analysis.JAMA,2011,305(24):2556-2564.
28 Choe EY,Wang HJ,Kwon O,et al.HMG CoA reductase inhibitor treatment induces dysglycemia in renal allograft recipients.Transplantation,2014,97(4):419-425.
29 Cho Y,Lee MJ,Choe EY,et al.Statin therapy is associated with the development of new-onset diabetes after transplantation in liver recipients with high fasting plasma glucose levels.Liver Transpl,2014,20(5):557-563.
30 Riella LV,Gabardi S,Chandraker A.Dyslipidemia and its therapeutic challenges in renal transplantation.Am J Transplant,2012,12(8):1975-1982.
31 Iida S,Ishida H,Tokumoto T,et al.New-onset diabetes after transplantation in tacrolimus-treated,living kidney transplantation:long-term impact and utility of the pre-transplant OGTT.Int Urol Nephrol,2010,42(4):935-945.
32 Cosio FG,Kudva Y,van der Velde M,et al.New onset hyperglycemia and diabetes are associated with increased cardiovascular risk after kidney transplantation.Kidney Int,2005,67(6):2415-2421.
33 Shivaswamy V,Boerner B,Larsen J.Post-Transplant Diabetes Mellitus:Causes,Treatment,and Impact on Outcomes.Endocr Rev,2016,37(1):37-61.
34 Hecking M,Haidinger M,Döller D,et al.Early basal insulin therapy decreases new-onset diabetes after renal transplantation.J Am Soc Nephrol,2012,23(4):739-749.

