抗人表皮生长因子受体2单克隆及双特异性抗体在进展期胃癌中的研究进展
胡珊,杨继元
长江大学附属第一医院肿瘤科,湖北 荆州4340000
胃癌的发病率虽然呈现稳步下降的趋势,但其仍是世界上常见和致命的肿瘤之一。流行病学研究显示,胃癌的发病率位居世界第五位,是全球第三大恶性肿瘤死亡的原因,仅次于肺癌和结直肠癌[1]。胃癌通常由于缺乏早期特异性症状而被延误诊断,多数患者确诊时已处于晚期阶段,5 年生存率较低;转移性胃癌患者的中位生存期不足1年[2]。人表皮生长因子受体2(human epidermal growth fac‐tor receptor 2,HER2,也称Neu)属于受体酪氨酸激酶家族,该家族包括4 个成员:HER1[也称表皮生长因子受体(epidermal growth factor receptor,EGFR)]、HER2、HER3 和HER4[3]。HER2 是一种185 kD 的跨膜糖蛋白,包含胞外配体结合域、跨膜域和具有酪氨酸激酶活性的胞内域[4]。HER2 通过异源二聚体和酪氨酸激酶的自磷酸化介导信号转导,激活下游通路,调节细胞增殖、分化和肿瘤发生过程中的信号转导[5]。因此,HER2 被认为是理想的抗肿瘤治疗靶点。本文总结了抗HER2 单克隆及双特异性抗体在进展期胃癌中的研究进展。
1 抗HER2 单克隆抗体
1.1 曲妥珠单抗(trastuzumab)
曲妥珠单抗是美国食品药品管理局(FDA)批准上市的第一种重组DNA 衍生人源化单克隆抗体,对HER2 二聚体具有良好的抑制作用,能够阻断配体活性信号的相关转导途径[6]。TOGA 研究是一项随机、开放、多中心Ⅲ期临床试验,首次对比了曲妥珠单抗联合卡培他滨或5-氟尿嘧啶+顺铂(XP/FP)方案与单纯化疗在HER2 阳性胃癌中的治疗效果,奠定了曲妥珠单抗在HER2 阳性胃癌一线治疗中的基础地位,胃癌治疗真正开启靶向治疗时代。该研究共纳入3807 例进展期胃癌和胃食管结合部腺癌患者,所有患者均进行了HER2 检测,其中,594 例HER2 阳性胃癌和胃食管结合部腺癌患者被随机分为单纯化疗组(接受XP/FP 方案,n=296)和曲妥珠单抗联合化疗组(接受曲妥珠单抗+XP/FP 方案,n=298),结果显示,曲妥珠单抗联合化疗较单纯化疗能明显改善患者的各项疗效指标,患者的总生存期(overall survival,OS)为13.8 个月,中位无进展生存期(progression-free survival,PFS)为6.7 个月,中位肿瘤进展时间(time of tumor pro‐gression,TTP)为7.1 个月,均明显长于接受单纯化疗患者的11.1、5.5、5.6 个月(P<0.01)[7]。HELOISE试验比较了曲妥珠单抗联合化疗一线治疗HER2 阳性晚期胃癌的两种剂量方案:曲妥珠单抗的起始剂量为8 mg/kg,其中一组的维持剂量为6 mg/kg,每3周1 次;另一组为10 mg/kg,每3 周1 次。该试验的主要研究目的是找到曲妥珠单抗的最优使用剂量和方法,主要终点是OS,次要研究终点是PFS、客观缓解率(objective response rate,ORR)、安全性等;结果显示,低剂量曲妥珠单抗组和高剂量曲妥珠单抗组患者的中位OS 分别为12.5 个月和10.6 个月(HR=1.24,P=0.24),中位PFS 分别为5.7 个月和5.6 个月,两组的安全性相似,提示一线使用高剂量曲妥珠单抗维持剂量并不能延长HER2 阳性胃癌患者的OS 或PFS[8]。此外,曲妥珠单抗一线治疗进展后的HER2 阳性胃癌患者能否继续使用曲妥珠单抗治疗?2018 年,美国临床肿瘤学会(American Society of Clinical Oncology,ASCO)会议报告了Ⅱ期WJOG7112G(T-ACT)的试验结果,该研究共纳入了91 例铂类和氟尿嘧啶类联合曲妥珠单抗治疗进展的患者,二线随机接受紫杉醇联合曲妥珠单抗和紫杉醇单药治疗,结果显示,两组患者的中位PFS 期为3.68 个月和3.19 个月(HR=0.91,P=0.33),中位OS 期为10.20 个月和9.95 个月(HR=1.23,P=0.20),ORR 为33.3%和31.6%(P=1.00),疾病控制率为61.5%和71.1%(P=0.47),两组患者的安全性相似,提示HER2 阳性胃癌患者在疾病进展后持续使用曲妥珠单抗并不能延长PFS 期[9]。
1.2 帕妥珠单抗(pertuzumab)
帕妥珠单抗是新一代人源化单克隆抗体,主要与HER2 受体胞外结构域Ⅱ区结合,同时可阻断HER3,与曲妥珠单抗联用可发挥协同作用,能够更全面地阻断HER2 信号转导,从而提高临床疗效,改善预后[10]。基于CLEOPATRA 研究的结果[11],2015年美国国立综合癌症网络(National Comprehen‐sive Cancer Network,NCCN)指南将帕妥珠单抗联合曲妥珠单抗和紫杉醇类化疗作为雌激素受体阴性、孕激素受体阴性和HER2 阳性的复发或Ⅳ期乳腺癌全身治疗的首选方案[12]。因此,帕妥珠单抗在HER2 阳性胃癌患者中的疗效令人期待。JACOB(NCT01774786)是一项双盲、安慰剂对照的随机多中心Ⅲ期试验,旨在评估帕妥珠单抗+曲妥珠单抗+化疗在HER2 阳性晚期胃癌及胃食管结合部癌中的疗效和安全性,并探讨在目前曲妥珠单抗加化疗的一线治疗方案上加用帕妥珠单抗的临床价值。该研究共纳入780 例初治HER2阳性转移性胃癌或胃食管结合部癌患者,患者被随机分配接受帕妥珠单抗840 mg(n=388)或安慰剂(n=392)联合曲妥珠单抗和化疗,主要终点是OS,次要终点是PFS、ORR、缓解持续时间(dura‐tion of response,DOR)、临床获益率(clinical bene‐fit rate,CBR)及安全性指标;结果显示,两组患者的中位OS 分别为17.5 个月和14.2 个月(HR=0.84,P=0.057),尽管帕妥珠单抗组患者的OS 较安慰剂组延长3.3 个月,但差异无统计学意义(P>0.05);两组患者的中位PFS 分别为8.5 个月和7.0 个月(HR=0.73,P<0.01);ORR 分别为56.7%和48.3%,DOR 分 别 为10.2 个 月 和8.4 个 月,CBR 分 别 为84.6%和81.3%[13]。虽然JACOB 研究显示了阴性结果,但在目前仍不能完全否定帕妥珠单抗在HER2阳性胃癌中的作用。
1.3 马格妥昔单抗(margetuximab/MGAH22)
马格妥昔单抗是一种Fc 片段优化的靶向HER2 的单克隆抗体,马格妥昔单抗具有与曲妥珠单抗相似的HER2 结合和抗增殖的作用,同时其优化的Fc 结构域可以增强抗体依赖性细胞介导的细胞毒性作用(antibody dependent cell mediated cyto‐toxicity,ADCC),提高了对肿瘤细胞的杀伤力[14]。基于一项临床Ⅰb/Ⅱ期研究(NCT02689284),目前正在进行一项关于马格妥昔单抗的临床Ⅱ/Ⅲ期研究MAHOGANY(NCT04082364),其旨在评估马格妥昔单抗联合免疫检查点抑制剂、联合或不联合化疗用于一线治疗HER2 阳性胃癌或胃食管结合部癌患者的临床效果,该研究分为2 个队列,队列A 为单臂研究,旨在评估马格妥昔单抗联合尚在研究阶段的抗PD-1 单克隆抗体MGA012 在HER2 阳性和PD-L1 阳性胃癌患者中的治疗效果;队列B 为随机试验,旨在评估在HER2 阳性胃癌患者(无论PD-L1 表达情况如何)中马格妥昔单抗联合抗PD-1单克隆抗体(MGA012 或MGD013)及化疗与曲妥珠单抗联合化疗的标准治疗方案的疗效,主要终点是OS,该项研究正在进行,未来靶向治疗联合免疫治疗可能成为更有效的治疗方案。
1.4 1E11
1E11 是一种抗HER2 人源化单克隆抗体,与曲妥珠单抗靶向的表位不同,其可以与Ⅳ亚区结合。有研究表明,1E11 联合曲妥珠单抗能增强HER2 过表达胃癌细胞系的抗肿瘤作用[15]。因此,对HER2过表达的胃癌患者而言,1E11 和曲妥珠单抗联合应用可能成为一种新型有效的抗体治疗方案。
2 抗体药物偶联物(antibody-drugconjugate,ADC)
2.1 T-DM1
T-DM1 是一种新兴的抗体和细胞毒药物偶联物,由曲妥珠单抗和细胞毒类药物美坦辛衍生物DM1 偶联而成[16-17]。GATSBY 研究(NCT01641939)是一项随机、开放、多中心Ⅱ/Ⅲ期研究,比较了T-DM1与标准紫杉烷类药物治疗进展的HER2 阳性局部晚期或转移性胃癌或胃食管结合部腺癌患者的临床效果,该研究共纳入345 例一线氟尿类加铂类治疗期间或之后进展的患者,随机分为T-DM1 治疗组(n=228)或TAX 治疗组(n=117);主要终点是OS;结果显示,两组患者的中位OS 为7.9 个月和8.6 个月(HR=1.15,P=0.86);两组患者的中位PFS为2.7 个月和2.9 个月;T-DM1 治疗组3 级及以上不良反应的发生率低于TAX 治疗组(60%vs70%),两组死亡相关不良反应的发生率相似;研究还显示,在既往接受过治疗的HER2 阳性晚期胃癌患者中,T-DM1 并不优于TAX,目前这类患者中,治疗选择仍然有限[16]。但是,GATSBY 研究失败原因亦可能是一线化疗后HER2 状态发生变化,而该研究中患者入组时未重新进行HER2 检测。因此,期待关于T-DM1 的进一步研究。
2.2 DS-8201a
DS-8201a 是人源化抗HER2 靶向抗体曲妥珠单抗与DNA 双螺旋拓扑异构酶Ⅰ抑制剂依沙替康衍生物组成的抗体-药物结合物[18]。一项Ⅰ期临床研究分析了DS-8201a 在既往接受过HER2 靶向标准治疗无效肿瘤患者治疗中的安全性,结果显示,DS-8201a 对HER2 低表达的胃癌患者仍具有抗肿瘤活性,并对T-DM1 耐药的肿瘤亦显示出抗肿瘤活性[19]。2018 年1 月ASCO 中公布了一项Ⅰ期胃癌临床研究数据,该研究共纳入45 例胃癌或者胃食管交界腺癌患者,其中,44 例患者曾接受过曲妥珠单抗治疗,24 例患者曾接受过伊立替康化疗,12例患者接受过5 次以上的抗肿瘤治疗。该研究分为两部分试验,第一部分试验共4 例患者,其中,3例患者的DS-8201a 给药剂量为5.4 mg/kg,1 例患者的DS-8201a 给药剂量为6.4 mg/kg,均静脉注射,每3 周1 次;第二部分试验共41 例患者,其中,17 例患者的DS-8201a 给药剂量为5.4 mg/kg,24 例患者的DS-8201a 的给药剂量为6.4 mg/kg,均静脉注射,每3 周1 次。结果显示,第二部分试验41 例患者的中位的PFS 为5.8 个月,中位DOR 为7.0 个月,ORR为45.5%(20/44),DCR 为81.8%(36/44);常见不良反应包括贫血、血小板减少、白细胞减少、中性粒细胞减少、恶心、食欲减退、呕吐、腹泻和发热,提示DS-8201a 对于既往接受过HER2 靶向治疗或化疗的HER2 阳性胃癌患者具有抗肿瘤的作用[20]。一项Ⅱ期研究DESTINY-Gastric02(NCT04014075)正在进行中,旨在探索DS-8201 治疗HER2 阳性的不可切除或转移性胃癌患者的疗效和安全性。
2.3 RC48
RC48 是中国自主研发的新型抗体偶联药物,是由人源化抗HER2 单克隆抗体与一甲基瑞奥西汀E(monomethyl auristatin E,MMAE)结合的抗体-药物偶联药物。一项开放、多中心、单臂、非随机Ⅱ期研究(NCT03507166)评估了RC48 用于HER2阳性局部晚期或转移性尿路上皮癌治疗的临床效果,初步显示治疗效果较好,具有一定的临床意义。另一项Ⅰ期研究(NCT02881138)结果显示RC48 治疗晚期胃癌的效果尚可。目前,RC48 治疗二线治疗失败的HER2 阳性晚期胃癌的Ⅱ期临床试验(NCT03556345)正在开展。
2.4 其他抗体药物结合物
XMT-1522 与传统抗HER2 单抗药物不同,其选择了一种全新的抗原表位作为识别位点,使其对HER2 的识别能力显著提高。临床前研究显示,XMT-1522 对HER2 阳性的耐T-DM1 的胃癌细胞仍有效[21]。一项关于XMT-1522 的Ⅰb 期临床试验(NCT02952729)正在进行中。SYD985 是由曲妥珠单抗和合成的duocarmycin 类似物组成的抗体-药物偶联药物。Menderes 等[22]的研究表明,SYD985的效果优于T-DM1,且对低表达HER2 细胞具有细胞毒性。MM-302 是一种曲妥珠单抗偶联聚乙二醇脂质体多柔比星的靶向-化疗药物偶联物,既有抗HER2 阳性细胞的靶向性,又有抗肿瘤作用,理论上具备减毒增效的作用[23-28]。(表1)
3 抗HER2 双特异性抗体
3.1 ZW25
ZW25 是一种靶向HER2 的新型双特异性抗体,靶点包括曲妥珠单抗结合位点和帕妥珠单抗结合位点[29]。在一项关于评估ZW25 对HER2 阳性晚期实体肿瘤患者安全性和有效性的Ⅰ期试验(NCT02892123)中,大多数接受药物治疗的患者为胃食管癌或结直肠癌患者,客观反应率为41%,且有轻微的不良反应[30]。目前,关于ZW25 联合化疗的Ⅱ期临床试验(NCT03929666)正在进行,旨在探讨ZW25 联合化疗治疗HER2 阳性胃食管腺癌的安全性、耐受性和抗肿瘤活性。2019年,ESMO报告了ZW25的最新临床数据,客观有效率为41%(14/34),疾病稳定率为38%(13/34),疾病进展率为21%(7/34),74%(25/34)的患者的目标病灶直径有所缩小,中位PFS 为6.21 个月;另外,ZW25 具有良好的耐受性,所有与治疗相关的不良反应均为1 级或2 级,未发现与治疗相关的严重不良反应[31]。上述数据证明ZW25 在HER2 阳性实体肿瘤中已展现出很好的临床活性,支持其进一步的临床发展。
3.2 Ertumaxomab
Ertumaxomab 可以同时靶向肿瘤细胞上的HER2 和T 细胞上的CD3,并通过其Fc 片段激活免疫细胞,发挥ADCC 的作用[32]。Diermeier-Daucher等[33]的研究表明,Ertumaxomab 的抗肿瘤作用主要依赖于免疫介导机制,因此,对于HER2 低表达或HER2 高表达但对曲妥珠单抗耐药的肿瘤患者,Er‐tumaxomab 可能是一种有希望的治疗方法。Haense 等[34]研究发现,在经批准的抗HER2 药物治疗的疾病(乳腺癌、胃癌)中,Ertumaxomab 可以作为一种超越标准疗法的新的个性化治疗方法。
3.3 MM-111
MM-111 是一种可同时靶向HER2 和HER3 的双特异性抗体,通过阻断heregulin(HRG)与HER3的结合,进而阻断HER3 的下游信号通路[35]。Zhang 等[36]的研究发现,HRG 降低了曲妥珠单抗和紫杉醇的活性,但在有HRG 存在的胃癌细胞中,MM-111 仍保持活性。因此,MM-111、曲妥珠单抗和紫杉醇联合应用可能是治疗HER2 阳性胃癌的理想药物。随后,2016 年,ASCO 年会公布了紫杉醇、曲妥珠单抗加或不加MM-111 用于HER2 阳性的晚期胃癌患者治疗的Ⅱ期研究(NCT01774851)结果,发现MM-111 并不能延长HER2 阳性晚期胃癌患者的OS 和PFS[37]。(表2)
4 小结与展望
综上所述,曲妥珠单抗被认为是目前治疗HER2 阳性晚期胃癌的典型药物。然而,曲妥珠单抗的耐药性是一个关键的限制性因素。HER2 靶向抗体药物结合物及双特异性抗体在临床前研究中对HER2 阳性耐药恶性肿瘤患者显示出较好的疗效。单克隆抗体和双特异性抗体对HER2 阳性肿瘤的治疗是安全、可行的。包括单克隆抗体和双特异性抗体在内的HER2 靶向治疗药物在治疗HER2 阳性进展期胃癌中起着至关重要的作用,但仍需要更多的临床研究对其有效性进行评估。

表1 已完成的抗HER2 抗体临床试验
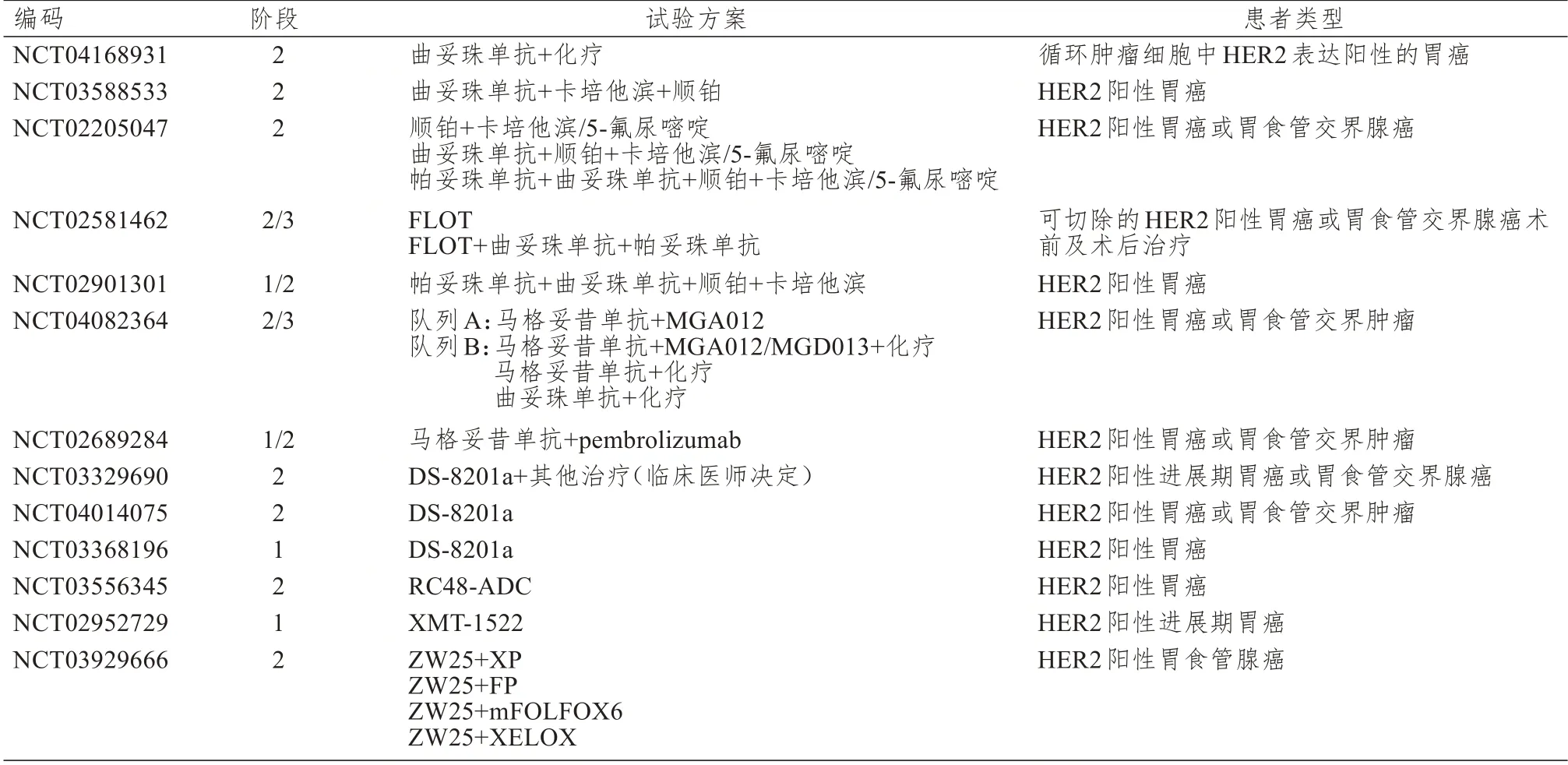
表2 正在进行的抗HER2 抗体临床试验

