老年胃癌术后放化疗胰腺所受剂量对内外分泌功能的影响
吕博,陈迪,高洪波,焦玉新,邱健健,郑向鹏
复旦大学附属华东医院放疗科,上海,200040
全球老龄化人口正以惊人的速度增长。胃癌是全球发病率第四的恶性肿瘤,在我国其发病率和死亡率均居恶性肿瘤第二位,60~74 岁其发病率为最高峰[1]。随着人口老龄化的趋势,60 岁及以上的老年胃癌患者越来越多。INT0116 试验奠定了同步放化疗在局部晚期胃癌根治术后辅助治疗中的地位,基于5-FU 的辅助同步放化疗已成为根治术后高危胃癌患者的标准治疗[2]。随着人类寿命的延长,老年胃癌患者会在术后实行同步放化疗,放疗相关毒副反应逐步成为研究热点。放疗计划制定时常规会对肝脏、双侧肾脏、小肠、脊髓等危及器官进行剂量限制[3-4]。由于胰腺特殊的解剖位置,横卧于腹腔,紧贴胃的下方,患者在放疗期间,胰腺不可避免的会受到照射,但目前并没有一个明确的胰腺放疗剂量限制的相关规定[5]。胰腺代表着代谢活跃的器官,具有摄取和分解基本营养成分的能力,老年患者随着年龄的增长,胰腺形态的变化以及分泌功能的下降会逐渐体现[6],因此放化疗期间老年患者胰腺的限量更值得探讨。
胰腺是本身兼有内分泌和外分泌功能的腺体,外分泌腺由腺泡和腺管组成,腺泡分泌胰液,腺管为胰液排除管道,胰液中含有碳酸氢钠、脂肪酶、淀粉酶等。胰液通过胰腺管排入十二指肠,发挥消化蛋白质、脂肪和糖的作用[7]。内分泌腺由大小不等的胰岛细胞团构成,可分泌胰高血糖素、胰岛素、胰多肽等影响血糖的控制、胃肠运动的抑制和胰液的分泌等。所以当胰腺受到损伤时,其内外分泌功能会受到影响,进而会导致患者体重减轻、脂肪泄、消化功能紊乱和营养不良,并加大了糖尿病的风险[8-10]。
本研究通过检测老年胃癌患者胰腺内外分泌功能相关的各项指标变化,分析胰腺放疗剂量体积参数与指标变化的关系,探索预防胰腺放疗相关损伤所需要的剂量限制。
1 资料与方法
1.1 一般资料 前瞻性选取2017年3月—2019年7月间在复旦大学附属华东医院接受胃癌根治术后辅助放化疗的老年患者。纳入标准:年龄≥60 岁;(2)KPS评分≥70 分;(3)胃镜下病理证实的胃腺癌;(4)患者均施行胃癌D1 或D2 根治术(R0 切除),术后分期为IIA 期-IIIC 期(AJCC 8 th);(5)无远处转移;(6)无既往恶性肿瘤病史;(7)无术前放疗史,无严重的造血功能、心、肺、肝、肾功能异常和免疫缺陷等放化疗禁忌;以上均符合予以入组。排除标准:(1)直接侵犯胰腺的T4;(2)胰腺切除史;符合其一则予以排除。
1.2 研究方法
1.2.1 放疗 所有患者均采用IMRT 6MV X 线直线加速器常规分割照射。治疗前均行CT 定位,采取仰卧位,平躺于真空塑形垫上,双侧上肢上举至于额定,强化螺旋CT 扫描,3 mm/层,扫描范围:上界至胸廓入口,下界至腹主动脉分叉处,CT 定位图像传输至Varian Eclipse 计划系统,随后医师进行靶区及危及器官勾画。胃癌术后临床靶区(clinical target volume,CTV) 包括术后瘤床、部分残胃及周围淋巴引流区,淋巴引流区域主要包括贲门旁、胃左动脉、胃大弯、胃小弯、脾门、肝门、胰十二脂肠淋巴结等区域,下界至左肾静脉下缘。在CTV 的基础上外放0.5~1 cm获得计划靶区(planning target volume,PTV)。总处方剂量45 Gy,1.8 Gy/次,95%等剂量线包绕PTV;肺V20<20%,V5<60%,肺平均剂量<16~18 Gy;心脏V30<46%,平均剂量<26 Gy;小肠V45 <195 mL,Dmax<50 Gy;脊髓最大剂量<45 Gy;肾脏V15<50%,平均剂量<16 Gy;肝脏平均剂量<23 Gy。运用剂量体积直方图来对靶区剂量分布和正常组织或器官受量进行评价。
1.2.2 化疗 同步口服替吉奥胶囊(维康达/鲁南,批准文号为: 国药准字H20080802)化疗,40 mg/m2,2 次/d,放疗日(周一至周五)口服,共25 d。当患者出现4 级粒细胞下降、血小板下降或3 级及以上非血液学毒性时,化疗剂量较前一次剂量减少25%,当患者出现2 次4 级粒细胞下降、血小板下降或3 级及以上非血液学毒性时,终止化疗。化疗推迟时间不应超过2 周,否则终止化疗。
1.2.3 各项检测指标评估及随访 所有患者均在(放疗前、放疗后3 个月、放疗后个6月)行晨起空腹肘部静脉血液检测,检测项目分别为:胰岛素、C 肽、糖化白蛋白、糖化血红蛋白、淀粉酶、脂肪酶等。制定放疗计划时勾划正常组织胰腺并记录DVH 数据(如胰腺V5、V10、V15、V20、V25、V30、V35、V40、V45),平均胰腺剂量;最高及最低胰腺剂量等。治疗期间,患者每周进行随访,治疗结束后2年内每3 个月随访,2年后每半年随访。随访终点为患者死亡。
1.3 统计学分析 采用SPSS 24.0 统计软件进行统计学分析。连续性资料治疗前后采用均数+标准差(±s) 进行比较,运用ROC 曲线分析胰腺受照剂量体积参数在胰腺分泌功能损伤的价值。以<0.05 为差异有统计学意义。
2 结果
2.1 患者基本情况 共纳入30 例胃腺癌术后患者,年龄60~81 岁,平均(66.6±6.2)岁,其中男性24 例,女性6 例;实行D1 根治术3 例,D2 根治术27 例;IIB 期、IIIA 期、IIIB 期及IIIC 期患者分别为5、8、10 及7 例(TNM 分期参照AJCC 8 th)。随访截止时间2019年12月31日,中位随访时间:18 个月,1、2年生存率分别为90%,75%。见表1。
2.2 治疗情况 仅1 例患者因3 级非血液学毒性终止放化疗,其余所有患者均顺利完成放疗,放疗剂量45 Gy,1.8 Gy/次,完成率98%。27 例患者完成同步口服替吉奥化疗,完成率94%,其中2 例3 度粒细胞减少中途停药,1 例因非血液学毒性停药。
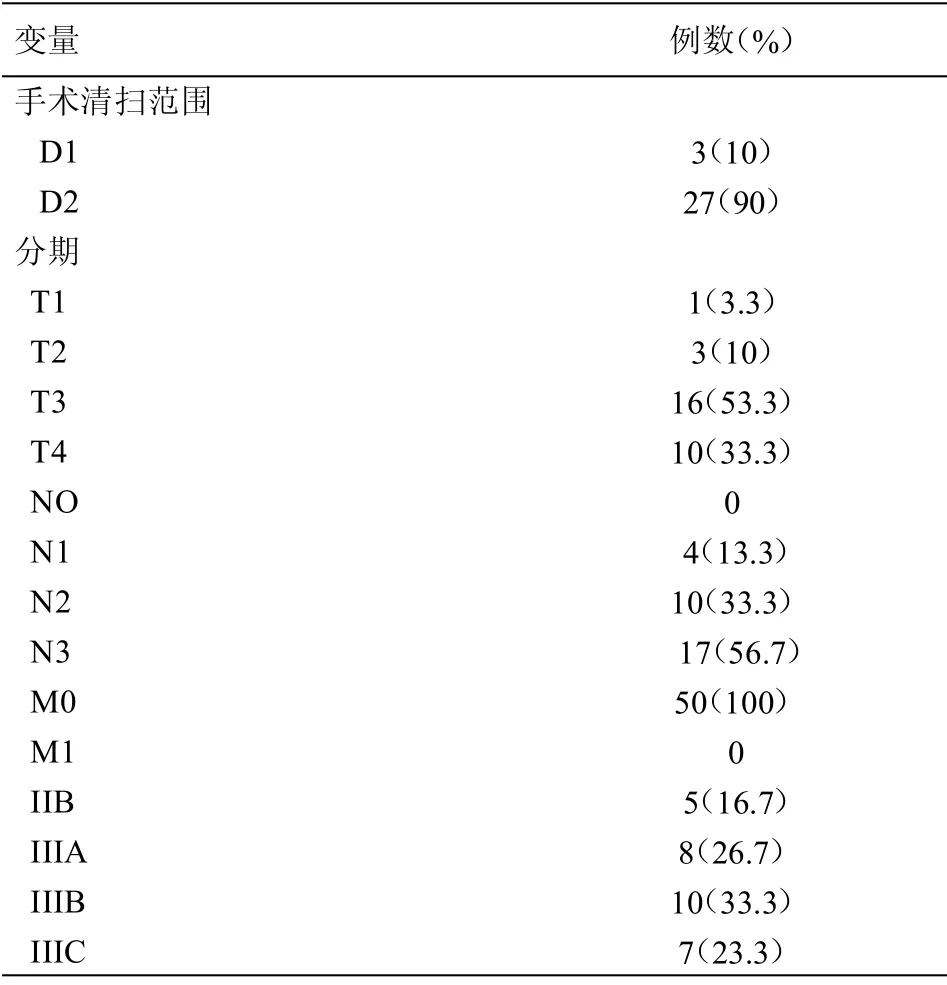
表1 入组患者基本情况
2.3 各项检测指标变化 所有患者于放疗前检测空腹血糖、糖化白蛋白及糖化血红蛋白较放疗后3 个月和放疗后6 个月,均无统计学意义。放疗后3 个月检测胰岛素、C 肽、淀粉酶、脂肪酶较放疗前均出现了下降,<0.05。淀粉酶、脂肪酶于放疗后6 个月仍然持续下降,差异具有统计学意义,而胰岛素、C 肽、并未观察到持续下降,见表2和表3。所有患者胰腺受照剂量体积参数如胰腺受照平均剂量、最小剂量、最大剂量见表4。各项内外分泌功能相关检测指标中脂肪酶的下降最为明显,尤其是大部分患者脂肪酶下降至初始水平的1/3 以下,将所有患者根据脂肪酶下降至是否低于初始水平的1/3 进行分组,经ROC 曲线分析得出胰腺V45 具有最佳预测价值(AUC=0.864,95%0.716~0.992,=0.001),切点值(cut-off)为V45<50%(敏感性84.6%,特异性82.4%)。见表5。
3 讨论
表2 放疗前与放疗后3 个月各项指标变化(±s)

表2 放疗前与放疗后3 个月各项指标变化(±s)
检验指标 放疗前 放疗后3 个月images/BZ_136_2147_443_2169_467.png血糖(mmol/L)胰岛素(mIU/mL)C 肽(ng/mL)淀粉酶(U/mL)脂肪酶(U/mL)糖化白蛋白糖化白蛋白(%)糖化血红蛋白(%)5.11±0.56 7.46±1.74 1.75±0.75 69.89±15.41 36.07±17.32 261.23±55.86 15.20±2.88 5.59±0.67 5.18±0.58 6.51±1.43 1.32±0.69 51.92±16.49 14.17±6.70 268.98±50.98 15.75±2.16 5.42±0.62 0.581 0.000 0.000 0.000 0.000 0.313 0.169 0.132
表3 放疗后3 个月与放疗后6 个月各项指标变化(±s)
检验指标 放疗后3 个月 放疗后6 个月images/BZ_136_2147_1095_2169_1119.png血糖(mmol/L)胰岛素(mIU/mL)C 肽(ng/mL)淀粉酶(U/mL)脂肪酶(U/mL)糖化白蛋白糖化白蛋白(%)糖化血红蛋白(%)5.18±0.58 6.51±1.43 1.32±0.69 51.92±16.49 14.17±6.70 268.98±50.98 15.75±2.16 5.42±0.62 5.36±0.56 6.38±2.33 1.16±0.51 45.51±12.19 11.15±5.92 269.53±43.15 15.92±2.69 5.46±0.87 0.161 0.673 0.106 0.023 0.018 0.867 0.610 0.665
表4 入组患者胰腺受照剂量体积参数(±s)
参数 剂量/体积胰腺受照平均剂量(cGy)胰腺受照平均剂量(cGy)胰腺受照平均剂量(cGy)胰腺V5 (%)胰腺V10 (%)胰腺V15 (%)胰腺V20 (%)胰腺V25 (%)胰腺V30 (%)胰腺V35 (%)胰腺V40 (%)胰腺V45 (%)4075±635 1731±1069 4746±113 95.6±9.7 94.5±11.2 93.5±12.2 92.7±13.4 91.1±15.1 88.5±16.7 83.4±18.1 75.4±19.4 57.2±22.3

表5 入组患者胰腺受照剂量体积参数ROC 曲线分析
有研究显示老年患者胰腺术后并发症更为严重[11],患者≥65 岁与65 岁以下的患者相比,术后并发症更多(62.6%32.4%,<0.001)以及更高的术后死亡率(5.5%0.9%,<0.001)。虽然胰腺功能下降是胰腺外科手术后的常见临床表现,但仍是一个未被全面研究的话题。因此,关于胰腺放疗相关损伤的研究也相对较少[12]。胰腺术后功能不全的相关研究显示接受术后辅助放疗的患者更有可能在术后出现内分泌功能不全(54%34%,=0.048)。接受放疗的患者与未接受放疗的患者相比,术后内分泌不足的风险为1.9,并且围手术期的其他因素与术后内分泌不足无关[13]。这可能与放疗诱发胰腺纤维化有关,已在部分接受过放疗的儿童肿瘤患者中的长期幸存者的相关研究中得以证明[14],但少有在老年患者中的研究,胰腺癌患者的预期寿命短,相比之下胃癌患者术后更长的生存期可以为我们提供研究晚期不良反应的机会。文献中有关放疗相关胰腺组织损伤的数据主要基于动物研究或腹部放射治疗小儿实体瘤或血液系统恶性肿瘤患者骨髓移植前的全身放射治疗(TBI)相关研究。胰腺的腺泡细胞对辐射损伤的敏感性比胰岛细胞高得多,辐射损伤的病理生理学主要是由于慢性血管损伤,最终导致纤维化和腺体萎缩。腹部放射治疗后的糖尿病尚未明确阐明腹部放疗与致糖尿病作用的关系。但很明显,胰腺暴露于放射线会引起糖尿病,而引起糖尿病的最常见原因是 细胞损伤[15]。也有一些研究表明,胰腺受照后慢性增加的炎性细胞因子水平起着关键作用,从而影响胰岛素的分泌[16]。
Ahmadu-Suka 等[17]通过25 Gy 术中放疗(IORT)实验用狗后,发生胰腺外分泌功能不全。尸检评估发现放疗后胰腺组织萎缩,在腺泡细胞上观察到放射损伤的组织病理学证据。有胰腺纤维化和血管及导管损伤,显示出剂量反应关系。然而,胰岛细胞病变并不明显。外分泌型胰腺功能不全和糖尿病可能是25 Gy或更高剂量IORT 的潜在晚期并发症。Pieroni 等[18]研究在6 周内给予实验用狗的胰腺接受了40 Gy 等效照射,这是最常用于治疗上腹部恶性肿瘤的剂量。镜下可见胰腺弥漫性间质纤维化,照射后腺泡细胞数量明显减少。尽管外分泌功能降低,但对内分泌功能影响不大。部分霍奇金病或精原细胞瘤患者腹部放疗后出现了慢性胰腺炎,中位观察期为7年,总剂量为36 Gy 至40.5 Gy。大多数患者患有胰腺疼痛,脂肪泻和糖尿病[19]。另外一项研究发现胃癌的辅助放化疗会导致 细胞功能和胰岛素分泌能力下降,治疗后6 个月,胰岛素,C 肽和HOMA-Beta 水平相应下降[20]。外分泌胰腺类似于腮腺,腮腺平均剂量是口干症的最佳预测指标。通过类推,可以预期该参数将适合于估计辐射对胰腺的损害风险,但是没有报告详细的剂量-体积分析,因为几乎整个胰腺都位于高剂量范围内。建议将平均剂量保持尽可能低的水平[21]。有研究表明大于65 岁的老年胃癌患者,其胰腺外分泌功能的下降更加明显,放疗后胰腺的损伤风险可能更高[21]。近期相关研究表明既往接受过术后辅助放疗的胃癌患者中,伴有肌肉减少症的患者OS 较差,V46 可能是肌肉减少症的独立危险因素[22]。也有研究指出胰腺放疗相关损伤可能是胃肠道放射毒性的一部分。通过大鼠模型评估了胃肠道放疗相关毒性和胰腺损伤的器官间相关性[23]。
所有这些前瞻性动物和回顾性人类数据分析均表明,放射线对胰腺内分泌和外分泌功能具有一定毒性。在本研究中,胰腺照射对老年患者的内外分泌功能的影响进行了研究,包括在腹部照射前以及腹部照射后3 个月至半年内测量空腹血糖、糖化白蛋白、糖化血红蛋白、胰岛素、C 肽、脂肪酶、淀粉酶的水平。其中空腹血糖、糖化白蛋白及糖化血红蛋白较与初始水平相比,研究结束时无差异。胰岛素、C 肽、淀粉酶、脂肪酶较治疗前均出现了下降,尽管内分泌胰腺储备有所减少,但没有一个患者出现明显的糖尿病,因为糖尿病的发展需要数年时间,并且有必要消耗所有胰岛细胞储备。这些患者应接受较长时间的随访,并应常规评估是否患有糖尿病。但是在接受辅助放疗的老年胃癌患者中,因糖尿病并发症导致的死亡风险可能会增加。外分泌功能方面的影响主要体现在脂肪酶在治疗前后的明显下降,尤其是大部分65 周岁以上患者放疗后脂肪酶下降至初始水平的1/3 以下,可能是影响预后的预测因子。当然,本研究也存在一些缺陷,如样本量较少,在本研究的基础上,随后开展的多中心前瞻性随机对照研究能够得出更可靠的结论,为老年胃癌术后患者提供更为优选的放疗方案。
胃癌术后放化疗的老年患者当中,胰腺的损伤主要表现为内分泌及外分泌功能的影响。外分泌功能的变化尤为明显,本研究建议将胰腺设为腹部放疗的危及器官,并加以剂量限值,推荐V45<50%,从而降低胰腺放疗相关的损伤风险,并可能改善接受辅助放化疗的胃癌患者的生存率。

