腹腔镜手术与传统开腹手术对直肠癌患者术后感染和免疫功能的影响
涂清卫
本研究比较了腹腔镜手术与传统开腹术对直肠癌患者术后感染和免疫功能的影响,现报告如下。
1 资料与方法
1.1 一般资料
按治疗方式分组60例直肠癌患者。入选标准:①各患者均满足《NCCN 结直肠癌诊治指南》[1]中直肠癌判定标准;②均满足手术指征;③均自行签字同意治疗方式。排除标准:①病灶出现远处转移者;②消化道出血者;③腹部手术史者;④合并感染症状者;⑤合并其他恶性肿瘤者;⑥肝肾等功能异常者。对照组:病灶距肛缘5.6~7.2 cm,平均为(6.5±0.4)cm,年龄42~81岁,平均为(65.2±1.1)岁,女性11例、男性19例;研究组:病灶距肛缘5.7~7.3 cm,平均为(6.8±0.5)cm,年龄41~82岁,平均为(65.8±1.2)岁,女性12例、男性18例。2组基本资料差异小(P>0.05)。
1.2 方法
研究组30例患者用腹腔镜手术治疗,全麻,截石位,消毒铺巾,控制腹部压力为10~12 mmHg,脐上端做直径10 mm观察孔,再在脐水平两侧2 cm部位与腹直肌外缘建立直径大约为5 mm的操作孔,并在两边麦氏点部位建直径为12 mm、5 mm的操作孔。在腹腔镜协助下观察病灶位置、与附近关系、病灶大小等,用聚合物夹或钛夹高位夹断肠系膜根部血管,游离肠系膜和肠段,清除附近淋巴结和系膜血管根部。
对照组30例患者用传统开腹手术治疗。全麻,取截石位,消毒铺巾,在患者腹部正中部位做大约15 cm的切口,逐层进入腹部,探查病灶,明确病灶位置、病灶有无转移、病灶浸润深度等,在肠系膜和肠组织之间做钝性分离处理,用丝线在病灶远端部位做结扎,冲洗直肠腔,术中保护盆腔自主神经和输尿管,采用吻合器实施超低位或低位结肠-肛管吻合。
1.3 指标判定
术后记录患者感染状况,包含泌尿系感染、腹腔感染、切口感染等。
术前、术后1周时抽取患者空腹静脉血液5 ml,用2 500 r/min的转速做离心处理,分离上清,用酶联免疫吸附法测定其免疫功能指标,包含干扰素γ(IFN-γ)、白细胞介素10(IL-10)、白细胞介素-2(IL-2)。
1.4 统计学方法
2 结果
2.1 术后感染率
研究组术后感染率为3.33%(1/30),低于对照组的30.00%(9/30)(P<0.05),见表1。
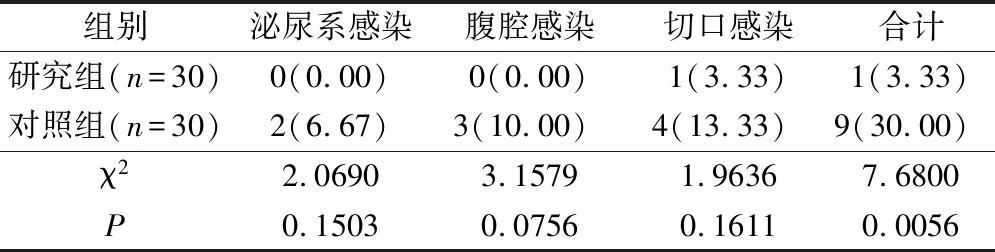
表1 术后感染率比较(例,%)
2.2 免疫功能
术前免疫功能指标差异小(P>0.05),术后1周时,研究组IFN-γ、IL-2低于对照组,IL-10高于对照组(P<0.05),见表2。
3 讨论
直肠癌病灶位置主要在直肠乙状结肠与齿状线两者的交界部位,发病后主要表现为排便梗阻、便血、脓血便等,主要采用手术方式治疗。按照其病灶位置、患者意愿、病情程度等因素选择手术方式,常用方式为传统开腹手术和腹腔镜手术。传统开腹手术视野清晰,可更为彻底地暴露病灶,操作更方便,但手术切口较大,过长时间暴露创面,术中、术后应激反应强烈,术后恢复速度缓慢,进而干扰到整体治疗疗效。因此,近年临床在选择手术方式时,多偏向于腹腔镜手术方式,其原因为,腹腔镜创伤小,术中建立操作孔,缩短了手术切口和手术视野暴露时间,疼痛轻微,且对腹壁神经损伤性也低,有利于术后恢复,但操作较为复杂,对操作者技术要求较高。
手术治疗直肠癌术后较为常见的一种并发症则为感染。本研究中采用2种手术方式进行治疗,结果显示,研究组感染率低于对照组,笔者认为出现此结果的原因与腹腔镜切口小、手术视野暴露范围小、创伤小等优势有关。此外,从免疫功能上来看,研究组IFN-γ、IL-2低于对照组,IL-10高于对照组,表明腹腔镜手术对直肠癌患者免疫功能的影响较小。IL-2指标高低可用来评估机体免疫功能激活状态。IL-10为抗炎因子,此可用来评估机体有无感染症状,IFN-γ可调节机体免疫功能[2],因此,通过考核以上3种免疫指标,也可评估机体免疫状态。

表2 比较免疫功能
综上,临床治疗直肠癌,可首选腹腔镜手术,相比于传统开腹手术,其术后感染更低,患者免疫功能更良好。

