CdS/Poly(MMA-co-MAA)复合材料的一步光化学法制备及其光催化性能研究
黄臻洵
(韩山师范学院 化学与环境工程学院,广东 潮州 521041)
CdS是一种常见的、传统的半导体光催化材料,其室温下禁带宽度为2.42 eV,为典型的Ⅱ—Ⅵ族直接带隙半导体化合物[1],在环境污染的治理中占有非常重要的地位[2-3].然而,一般金属硫化物半导体的主要缺点都在于其光激发下的腐蚀过程,而量子化的金属半导体相对于一般粒子更容易被光腐蚀[4].由于CdS本身的光腐蚀现象,在环境污染治理中会带来二次污染.因此,要应用CdS治理环境污染,必须先提高其稳定性.将CdS与聚合物通过适当方式复合制备复合材料,可改变材料的结构与组成,有利于提高材料的光稳定性.
近年来,半导体纳米粒子/有机物复合材料正在成为一个新兴的极富生命力的研究领域,引起众多研究者的广泛关注.张轶楠[5]通过溶剂热法,以含羧基聚芳醚酮聚合物为稳定剂,利用原位合成法制备了一系列聚芳醚酮/CdS纳米复合材料.朱佳[6]等通过原位自由基聚合法制得PMMA/CdS复合材料.廖勇勤[7]等利用超声辐照制备PMMA/TiO2、PMMA/SiO2纳米复合材料.随着纳米技术的发展,光化学合成技术也开始渗透到纳米领域,并已形成了一些成熟的制备方法.光化学是材料合成的一项重要技术,主要是通过物质吸收光子,形成激发态分子,进而发生相关的化学反应而生成特定材料的一种方法.相应于热化学,光化学有如下特点:(1)光是一种非常特殊的生态学上清洁的“试剂”;(2)光化学反应条件一般比热化学要温和;(3)光化学反应能提供安全的工业生产环境,因为反应基本上在室温或低于室温下进行;(4)在常规合成中,可通过一步光化学反应大大缩短合成路线;(5)该类反应只受光的控制,可通过光路的控制而体现材料合成的灵活性,这将为材料的器件化、局部化修饰、材料的功能化及廉价合成提供有效的工具[4].Ichimura等[8]用CdSO4和Na2S2O3为原料,按一定的比例将这两种物质溶解成溶液,在紫外灯的照射下,利用光化学反应在玻璃衬底生成CdS薄膜.黄玉英[4]等以二硫化碳为硫源,醋酸镉为镉源,甲醇为溶剂,加入苯乙烯单体,在紫外灯辐照下一步法原位聚合生成了CdS/聚苯乙烯复合物.
相关研究发现,无机半导体材料(如ZnO,Fe2O3,TiO2,CdS)在紫外光照射下可引发单体聚合制备聚合物[9-13].例如Hoffman等[12]用ZnO和CdS量子点分别引发甲基丙烯酸甲酯和苯乙烯聚制备聚甲基丙烯酸甲酯和聚苯乙烯;Song等[13]利用纳米TiO2引发苯乙烯聚合得到聚苯乙烯.这些无疑为聚合物/无机半导体复合材料的制备提供了一条新思路.然而,研究中无机半导体和聚合物的合成都是分步进行的,操作复杂.因此,以上述思路为基础,寻找合适方法以简便制备聚合物/无机半导体复合材料仍是材料科学领域中的一个挑战.
考虑到半导体引发效率与其材料尺度有关,相比于一般纳米材料,半导体量子点具有更高的引发效率,故在CdS生成同时引发单体聚合具有较高可行性.基于此,本文以CdSO4、Na2S2O3、甲基丙烯酸甲酯(MMA)和甲基丙烯酸(MAA)为原料,通过紫外光照射在溶液内部生成CdS,并同步引发MMA 和MAA 共聚,从而一步合成CdS/Poly(MMA-co-MAA)复合物,采用X 射线衍射仪、红外光谱仪、热重分析仪和台式扫描电子显微镜对材料的结构和组成进行表征,并以亚甲基蓝为目标降解物,在紫外光和可见光下对材料光催化活性及光腐蚀效应进行研究.
1 实验
1.1 实验原料
硫酸镉(3CdSO4·8H2O,AR),天津市福晨化学试剂厂;硫代硫酸钠(Na2S2O3·5H2O,AR),西陇化工股份有限公司;甲基丙烯酸甲酯(MMA,AR),上海阿拉丁试剂有限公司;甲基丙烯酸(MAA,AR),天津市科密欧化学试剂有限公司;无水乙醇(99.5%),广州化学试剂厂;亚甲基蓝(MB,AR),上海三爱思试剂有限公司.
1.2 CdS和CdS/Poly(MMA-co-MAA)复合材料的制备
1.2.1 CdS的制备
称取0.155 g 的Na2S2O3·5H2O 和0.962 g 的3CdSO4·8H2O 于150 mL 烧杯中,加入50 mL 去离子水,搅拌,使固体完全溶解,在磁力搅拌下,将体系置于波长为254 nm的8 W紫外灯下光照反应12 h.反应完毕,将制得的产物离心分离,并用去离子水洗涤3次,最后将产物烘干,待用.
1.2.2 CdS/Poly(MMA-co-MAA)复合材料的制备
将0.155 gNa2S2O3·5H2O、0.962 g3CdSO4·8H2O、50 mL 去离 子水、0.128 g 甲基丙烯酸甲酯(MMA)和0.014 g甲基丙烯酸(MAA)混合于锥形瓶中,在暗处先搅拌12 h,使单体充分分散于水溶液中形成单体液滴,在磁力搅拌下,采用波长为254 nm的8 W紫外灯光照反应12 h.反应完毕,将制得的样品离心,用无水乙醇洗涤2次,去离子水洗涤3次,最后将产物烘干,待用.
1.3 测试与表征
1.3.1 结构及组成表征
样品的晶型结构分析使用X 射线衍射谱图(XRD):X-射线衍射仪(D8ADVANCE),以CuKα 0.154 2 nm 作为射线源;样品表面官能基团分析使用傅里叶红外光谱图(FTIR):红外分光光度计(Bruker,Vector-22),采用KBr 压片法;样品的热失重率采用热失重分析图(TGA):热失重分析仪(NETZSCH,209F1),测试条件为在空气气氛下以20° C/min的升温速率从40° C加热至560 °C;样品的形貌使用台式扫描电子显微镜(TM3030)观察.
1.3.2 光催化性能测试
光催化活性测试以亚甲基蓝(MB)(3×10-5mol/L)为目标降解物,光源分别选用8 W 254 nm的紫外灯和300 W Xenon 灯(可见光光源),具体操作如下:
紫外光光催化性能测试:将0.02 g 催化剂样品和150 mLMB加入250 mL烧杯中,先在黑暗条件下搅拌10 min 以达到MB 的吸附平衡(即为光催化反应的初始浓度C0),之后开始进行光照降解实验,每隔20 min取样5 mL,离心后取上层清液,用紫外可见分光光度计在波长665 nm 下测定不同降解时间的吸光度值求降解率,总时间为3 h.
可见光光催化性能测试:将0.02 g 催化剂样品和150 mLMB 加入带冷却装置的光催化反应器中,通循环水保持温度恒定,先在黑暗条件下搅拌10 min 以达到MB 的吸附平衡(即为光催化反应的初始浓度C0),之后开始进行光照降解实验,每隔20 min 取样5 mL,离心后取上层清液,用紫外可见分光光度计在波长665 nm 下测定不同降解时间的吸光度值求降解率,总时间为3 h.
1.3.3 光腐蚀分析
光催化性能测试结束后,将剩下的溶液离心后取1 mL 上层清液配成100 mL 溶液,用原子吸收光度计(AAS)测定溶液中Cd2+的浓度,以此确定光腐蚀的程度.
2 结果与讨论
2.1 CdS/Poly(MMA-co-MAA)复合材料的结构与组成表征
2.1.1 XRD表征分析
图1 为CdS/Poly(MMA-co-MAA)复合材料的XRD 图.在样品的XRD 图谱上出现了2θ=26.72°(111),43.5°(220)和51.4°(311)3 个明显的特征衍射峰,与立方晶相的CdS 标准谱图相同,说明复合材料含有CdS,为立方晶型的CdS.峰位为26.72°、43.5°、51.4°的峰值分别为具体峰值,峰值较高,且有宽化现象,说明CdS的结晶程度较好,且粒子粒径较小,表面积比较大.
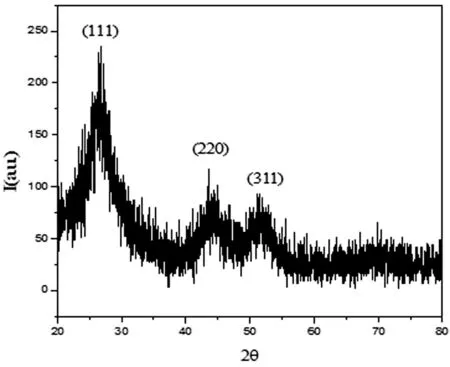
图1 CdS/Poly(MMA-co-MAA)复合材料的XRD图
2.1.2 FTIR与TGA表征分析
图2为CdS/Poly(MMA-co-MAA)复合材料的FTIR 光谱图.在谱图上可清晰观察到在波数为3 437 cm-1、1 732 cm-1和1 045cm-1处有三个特征吸收峰,3 437 cm-1吸收峰对应O-H基团,来源于吸附水,而1 732 cm-1和1 045 cm-1吸收峰分别对应C=O和C-O基团,据此可以判断复合材料中存在羧基及酯基,这表明复合材料中可能含有Poly(MMA-co-MAA).

图2 CdS/Poly(MMA-co-MAA)复合材料的FTIR图
为进一步证明复合材料中含有聚合物,对复合材料进行热失重分析,图3 为CdS/Poly(MMA-co-MAA)复合材料在空气气氛下的热失重曲线.从图中可以看出,复合材料在300 ℃前的失重约为4.84%,该部分为材料物理吸附水的脱附及光化学反应产物S单质的分解;从300 ℃之后出现一个明显失重区,直到550 ℃质量基本不变,该部分失重约为10.56%,这是由于聚合物受热分解引起的.结合FTIR结果,可以证明复合材料中含有Poly(MMA-co-MAA).
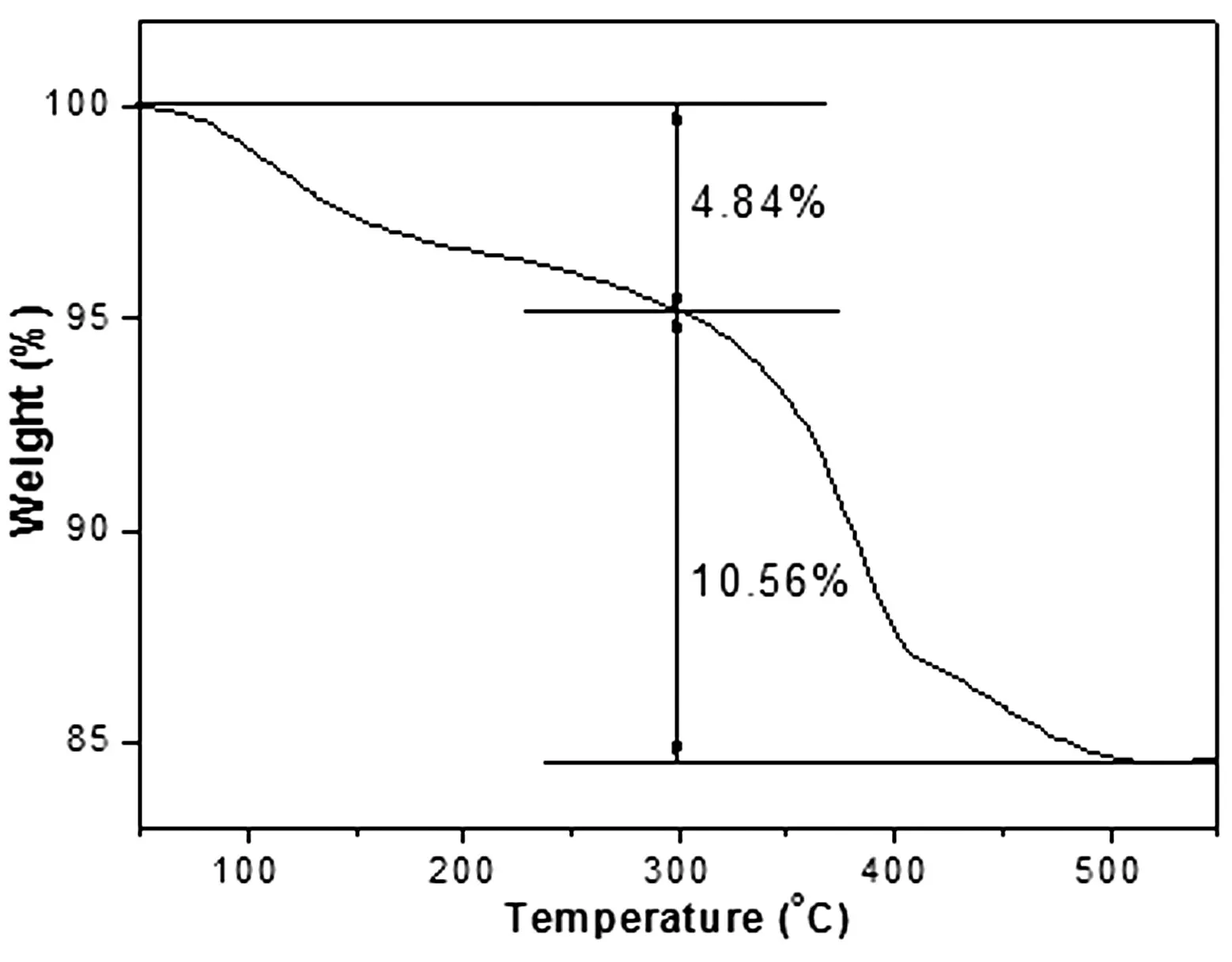
图3 CdS/Poly(MMA-co-MAA)复合材料的TGA图
2.2 CdS/Poly(MMA-co-MAA)复合材料生成机理
为探讨CdS/Poly(MMA-co-MAA)复合材料的生成机理,本研究设计了四个对比实验,反应前驱体分别为(a)MMA 和MAA,(b)CdSO4、MMA 和MAA,(c)Na2S2O3、MMA 和MAA,(d)CdSO4、Na2S2O3、MMA和MAA,均以水相作为反应体系,并采用波长为254 nm的8 w紫外灯照射12 h,实验结果现象如图4所示.从图中可以清楚看到,反应结束后,配方(a)和(b)的反应体系基本澄清透明,配方(c)的锥形瓶底有极少量的淡黄色沉淀物,配方(d)的反应体系出现大量黄色物质.以上实验现象表明,在实验条件下,配方(a)和(b)可能没有发生反应或反应很慢以致观察不到明显现象,而配方(c)和(d)有化学反应发生.

图4 不同反应物反应结果照片
根据该实验现象,结合前述对复合材料的结构组成表征,我们推测CdS/Poly(MMA-co-MAA)复合材料的生成机理如下:反应物在搅拌作用下,单体分散于水溶液中形成单体液滴,在紫外光的照射下,CdSO4和Na2S2O3首先发生如下所示的(1)-(4)的反应生成CdS,而生成的CdS将附着于单体液滴表面,并引发促使MMA和MAA在紫外光下共聚,从而生成CdS/Poly(MMA-co-MAA)复合材料.这与相关研究[12]中提到CdS量子点在紫外光照射下可分别引发MMA及St等单体聚合制备PMMA和PS的观点相符合.

2.3 光催化性能分析
图5和图6是空白样、纯CdS和CdS/P(MMA-co-MAA)复合材料分别在8 W紫外灯和300 W氙灯下降解亚甲基蓝(MB)的光催化降解率图.从图中可以看出,无论是在紫外光下还是在可见光下,CdS/P(MMA-co-MAA)复合材料都表现出较高的光催化活性:如图5所示,经过8 w紫外光180 min光催化后,以CdS/P(MMA-co-MAA)复合材料作为光催化剂,亚甲基蓝的降解率达到了72%,而以纯CdS作为光催化剂时,亚甲基蓝的降解率仅为59%;如图6所示,尽管经过300 w氙灯的可见光180 min光催化后,以CdS/P(MMA-co-MAA)复合材料和纯CdS作为光催化剂,亚甲基蓝的降解率相当,分别为89%和87%,但是以CdS/P(MMA-co-MAA)复合材料作为光催化剂,亚甲基蓝的降解速率明显加快.

图5 样品在8 w紫外灯下的光催化降解MB的降解率图

图6 样品在300 w氙灯下(可见光)的光催化降解MB的降解率图
光催化活性的差别是由于光催化剂比表面积的不同引起的.图7 为纯CdS 和CdS/P(MMA-co-MAA)复合物的SEM照片.如图所示,纯CdS颗粒粒径较大,分散不均匀,粒子间存在团聚现象;而CdS/P(PMMA-co-MAA)复合材料颗粒粒径较小,分散较为均匀,具有较大的比表面积,因此光催化活性较大.

图7 样品的SEM图
2.4 光腐蚀效应分析
表1是纯CdS和CdS/P(MMA-co-MAA)复合材料分别在紫外光和可见光下光催化降解MB后取样在原子火焰分光光度计上测得在光催化过程样品的光腐蚀数据.从表1 中可以看出,在紫外灯照射下,以纯CdS和CdS/P(MMA-co-MAA)复合材料为光催化剂,经过3 h的光催化降解MB后,溶液中Cd2+分别为3.095 mg 和1.054 mg;而在可见光下以纯CdS 和CdS/P(MMA-co-MAA) 复 合材料作为光催化剂在可见光下降解MB,溶液中Cd2+分别为7.938 mg和3.849 mg.上述数据表明,不管是在紫外光还是在可见光下,CdS/P(MMA-co-MAA)复合材料的光催化降解液中Cd2+浓度均低于纯CdS.前述TG 结果表明,CdS/P(MMA-co-MAA)复合物中CdS的质量分数高达84.6%,因此材料组成不是两种光催化剂降解MB后溶液中Cd2+含量不同的主要原因,而是由于CdS/P(MMA-co-MAA)复合物中羧基对Cd2+有配位螯合作用,使光腐蚀产生的Cd2+固定在材料上,从而降低了溶液中Cd2+的含量.
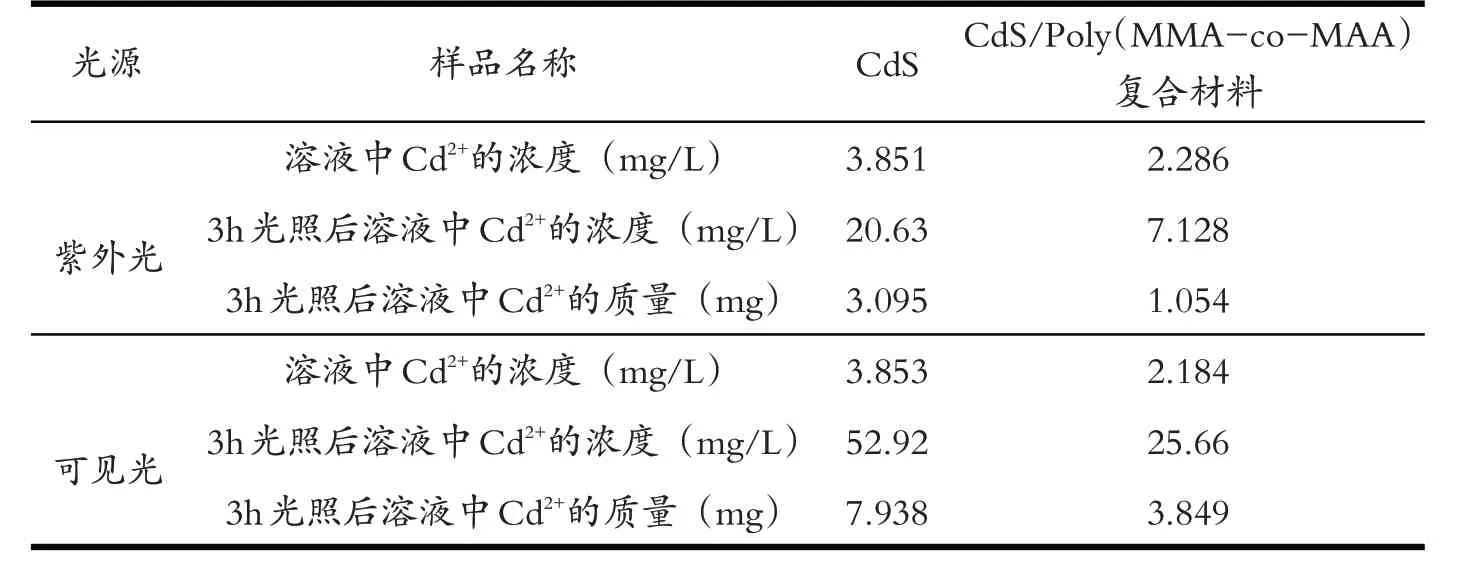
表1 样品光催化反应时光腐蚀数据
3 结论
本研究以硫酸镉、硫代硫酸钠、甲基丙烯酸甲酯和甲基丙烯酸为前驱体,通过光化学一步法合成了CdS/Poly(MMA-co-MAA)复合材料,经XRD、FTIR和TGA表征确定了材料的结构与组成.研究发现,无论是在紫外光下还是在可见光下,相比于纯CdS,CdS/Poly(MMA-co-MAA)复合材料在降解亚甲基蓝时都表现出较高的光催化活性,而且由于P(MMA-co-MAA)中羧基的存在,有效地降低了CdS在光催化降解亚甲基蓝过程中的光腐蚀情况.

