地下水污染识别与溯源指示因子研究进展
王会霞, 史浙明, 姜永海, 廉新颖, 杨 昱, 冯 帆, 贾永锋*
1.中国环境科学研究院 ,环境基准与风险评估国家重点实验室, 北京 100012 2.中国地质大学(北京) 水资源与环境学院, 北京 100083 3.中国环境科学研究院, 国家环境保护地下水污染模拟与控制重点实验室, 北京 100012
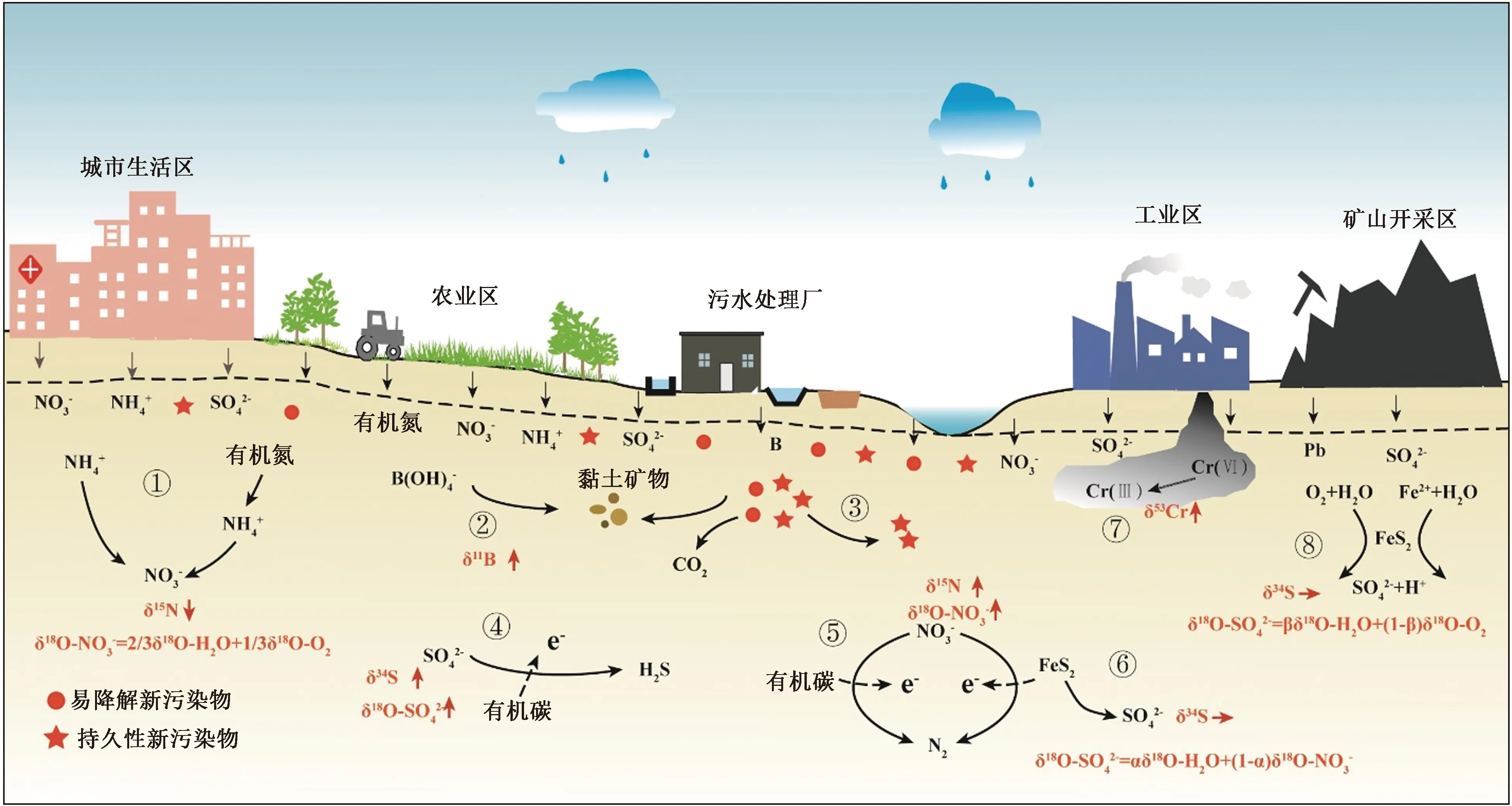
注: ①硝化作用(人为输入的氨氮和有机氮转化成地下水中NO3-,造成NO3-浓度升高,δ15N-NO3-值升高);②硼的吸附作用(人为输入的硼在迁移过程中被黏土吸附,剩余的δ11B升高);③新污染物的吸附、降解与迁移(易降解的污染物在迁移过程中被吸附降解;持久性污染物在地下水中逐渐积累);④硫酸盐还原作用(在还原环境中,发生细菌的硫酸盐还原作用,导致地下水中SO42-浓度减少,δ34S-SO42-和δ18O-SO42-值升高);⑤异养反硝化作用(多数情况下,有机碳参与的反硝化作用,使地下水中NO3-浓度降低,δ15N-SO42-和δ18O-SO42-值升高);⑥自养反硝化作用(以黄铁矿为例,还原性黄铁矿参与到反硝化过程中,造成NO3-浓度降低,δ15N-NO3-和δ18O-NO3-值升高,而SO42-浓度升高,其δ34S-SO42-值不变,δ18O-SO42-值取决于参与此过程的氧源);⑦铬的还原作用〔Cr(Ⅵ)还原成Cr(Ⅲ),使得水体中剩余Cr(Ⅵ)的δ53Cr升高〕;⑧硫化物的氧化作用(氧化环境中,还原性硫化物转化成SO42-,其δ34S-SO42-值保持稳定). 图1 地下水典型污染物迁移转化过程中同位素含量变化特征示意Fig.1 Schematic diagram of isotope value change during the mobilization and transformation of typical pollutants in groundwater
地下水作为重要的饮用水源,其水质问题一直受到人们高度关注[1]. 含水层赋存于地下,一旦被污染,其修复治理难度大、成本高,源头防控是地下水污染修复治理的关键[2],因此查明污染来源对于制定含水层保护策略至关重要[3]. 地下水污染识别采用的技术手段主要包括地球化学足迹法[4]、数理统计法和模型优化法[5]. 数理统计法利用一定的地质统计方法寻求源汇之间数值上的联系[6],通常需要足够的数据量,统计结果有时并不能代表实际情况[7];模型优化法考虑实际场地水文地质条件,主要通过溶质运移模型反演污染的来源,是点状污染源造成的污染场地溯源的有力手段,如石化场地、垃圾填埋场等;地球化学足迹法是利用地球化学指纹或者同位素指纹获取污染源信息的溯源方法[8],相比于统计分析和模型优化对数据量和场地资料的要求,它主要关注具有源特异性的指标,分析潜在污染源与地下水之间的关系,实现快速识别与准确溯源的目的. 因此,该文总结归纳了目前常用于地下水污染溯源的污染指示因子,重点分析其在不同场景下单独及联合应用的情况,并对其发展前景进行展望,以期为地下水污染溯源工作提供参考依据.
1 稳定同位素指示因子
稳定同位素是识别地下水污染物来源最常用的工具[4]. 通常利用稳定同位素作为溯源的指示因子有以下两方面要求[9]:①潜在各污染源之间存在可识别的同位素值差异;②同位素特征在环境中保守,即几乎不发生分馏作用,或者其分馏作用可以被识别. 因此,在筛选利用同位素指示因子溯源的同时,物理、化学及生物过程会产生同位素分馏的物理、化学分馏(见图1),因此应尽可能地区分这些过程带来的影响.
1.1 硝酸盐同位素
硝酸盐污染是浅层地下水中最常见的污染[10],主要来源于合成化肥、粪肥、污水、大气沉降、土壤氮、化粪池及垃圾填埋场[11-14]. 不同来源的硝酸盐,其硝酸盐氮同位素(15N-NO3-)比值存在差异[15],可以根据不同来源的同位素特征值识别污染来源较为单一的地下水污染. 但是15N-NO3-本身存在2个问题:①不同来源的15N-NO3-之间存在着重叠[16-17],大气氮与硝酸盐化肥、氨肥和降水、土壤氮以及部分粪肥和污水的15N-NO3-存在重叠;②硝酸盐在地下水环境中受到硝化、反硝化作用的影响,其15N-NO3-发生改变[18-19]. 这些问题都可能造成对污染来源的误判. 因此,当地下水中可能存在多种污染来源时,单纯利用15N-NO3-并不能作为硝酸盐来源的准确依据[16,20-22].
硝酸盐氧同位素(18O-NO3-)的加入可以为污染来源提供更多的证据[23]. 大气氮、硝酸盐化肥与其他污染源的18O-NO3-典型值范围存在明显差异[24-25],其受控于硝酸盐形成过程中利用的氧同位素特征值. 硝酸盐肥料在其合成过程中利用大气中的氧气(δ18O-O2约为23.5‰)和氮气产生硝酸盐,且生产过程中几乎不发生同位素分馏,因此其氧同位素比值接近大气氧气的同位素特征值[23]. 而其他氮源(氨肥或有机氮)通过硝化作用产生硝酸盐,其氧同位素组成主要受该过程中涉及的氧源同位素组成控制. 硝化过程仅从溶解的大气氧气(δ18O-O2为23.5‰)中吸收了一个氧原子,而从水(δ18O-H2O为-25‰~4‰)中吸收了另外2个氧原子[9,26-29],因此,相比于硝酸盐合成肥料,硝化产生的硝酸盐的18O-NO3-值更低. 另一个影响同位素溯源的因素是反硝化过程. 在厌氧环境下微生物介导的反硝化过程中,随着硝酸盐浓度的减少,δ15N-NO3-、δ18O-NO3-值增加且二者之间存在线性关系[28],比率大致介于1.3~2.1之间[30-31],由此可作为反硝化过程的证据. 图2列举了2个案例中地下水中的同位素比值,其中圆点表示非洲喀拉哈里地区[32]地下水中的硝酸盐同位素的特征值,三角形代表韩国济州岛地区[33]2个含水层中硝酸盐同位素的特征. 其中Ghanzi和Gobabis地区的地下水受到动物粪便与化粪池的影响,Serowe地区同位素值在土壤氮的范围内,表明主要受到天然来源的硝酸盐影响[32]. 韩国济州岛地区不透水层上、下某含水层中的同位素特征表明,地下水中升高的硝酸盐主要来源于合成肥料,另外,浅层含水层中溶解氧含量表明部分地点处于厌氧环境,同位素特征表明可能存在反硝化作用[33]. 硝酸盐同位素难以区分粪肥与污水来源[16-17],在实际应用中需借助其他溯源手段.
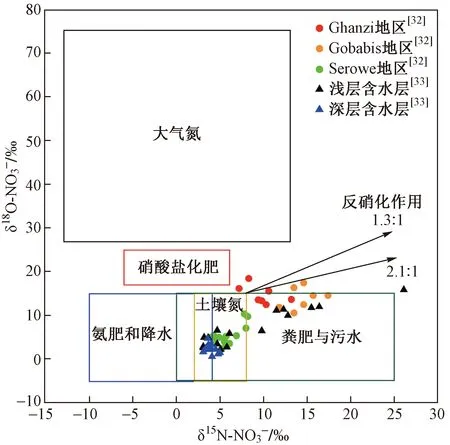
图2 各种硝酸盐来源的δ15N-NO3-和δ18O-NO3-的典型值Fig.2 Typical 15N and 18O values of various nitrate sources
1.2 硫酸盐同位素
硫酸盐是地下水中常见的无机污染组分,其天然的来源途径包括含水层中蒸发岩的溶解和硫化物的氧化,而含硫酸的工业废水排放、酸性矿井排水、化肥的施用以及城市生活污水排放等是主要的人为污染源[34]. 在地球化学循环过程中,除硫酸盐的微生物还原作用外,其他物理化学过程几乎不会产生显著的硫同位素分馏作用[35-37]. 硫酸盐还原作用只会在厌氧且氧化还原电位(Eh)为显著负值的情况下发生[38]. 氧同位素比值(δ18O-SO42-)具有与其成因相关的同位素特征,即取决于形成硫酸盐的氧源同位素特征[17],可以辅助识别由此产生的影响. 在此过程中,随着硫酸盐浓度的降低,δ34S-SO42-值增加,δ18O-SO42-值也随之增加[39-40],且δ34S-SO42-与δ18O-SO42-具有良好的线性相关性,其比值接近1∶1.4[39]. 如图3所示,分别选取了A、B、C、D、E 5个区域的地下水,其中A区和B区[41]为西班牙南部某一流域的地下水,A区地下水主要受合成化肥和污水的影响,而B区主要受到含水层内石膏溶解的影响;C区与D区[42]选自城市地区的地下水,C区地下水主要受化粪池的影响,D区受该区内农业施用化肥及污水中清洁剂的影响;E区[43]地下水中硫酸盐主要源于硫化物的氧化. 众多的研究证明了硫酸盐同位素对不同污染源具有较好的指示作用,对研究区各潜在硫酸盐来源的同位素情况掌握有助于提高指示精度.
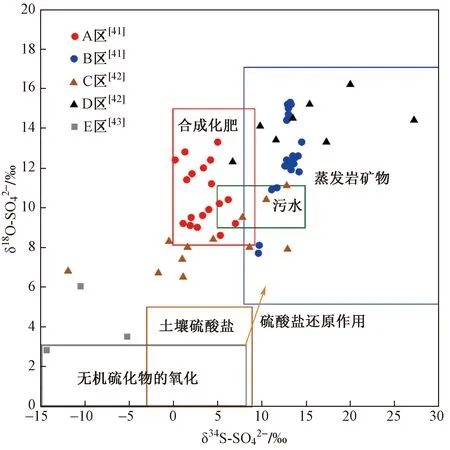
图3 各种硫酸盐来源的δ34S-SO42-和δ18O-SO42-的典型值Fig.3 Typical 34S-SO42- and 18O-SO42- values from various sulfate sources
1.3 硼同位素
硼在地下水中的存在形式主要为含氧化合物(硼酸与硼酸根离子),无价态变化且不参加氧化还原化学反应[44]. 天然地下水中硼的含量一般较低,但是受到卤水、海水入侵以及硼酸盐矿物溶解的影响,地下水中硼的含量会升高,特别是硼化合物在人类生活中的广泛应用(常用于清洁用品中),使得来自污水、垃圾渗滤液、农业径流等的硼可能污染地下水[45-46].
硼的2种稳定同位素10B和11B之间存在较大的相对质量差,导致易产生同位素分馏[47]. 硼同位素分馏主要由同位素平衡交换反应产生,动力学分馏效应较小[47]. 人为来源的硼在生产过程中几乎不发生同位素分馏[4,48],并且污水常用的生物法处理中既不能去除硼也不改变硼同位素的组成[47]. 有研究[49]表明,黏土矿物的吸附作用可使硼同位素产生20‰的变化(见图4). 在图4中,非海相钠硼酸盐、钙硼酸盐和污水的硼同位素特征值范围跨度较小. 海水入侵和污水影响造成的硼同位素值存在显著差异[44]. 如果污染源与地下水的硼同位素值存在显著差异(如5%以上),则可识别污染物的低混合程度影响[44]. 硼同位素对于各污染源较小比例的混合作用具有较强的敏感性. 相对于硼浓度受稀释作用的影响,硼同位素在地下水中表现更为保守,通常可以保留数十年[50],但低硼含量淡水中,δ11B值的测量精度可能限制其在污染溯源中的应用.
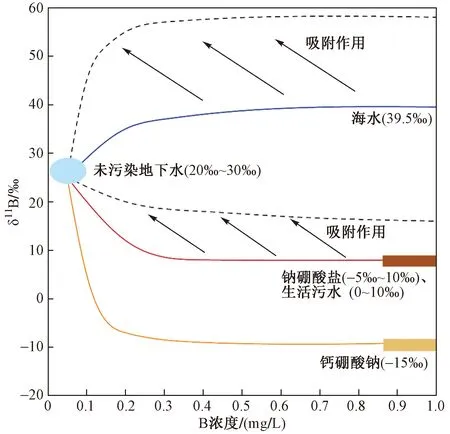
注: 参考Vengosh等[49],有改动. 图4 未受污染地下水与污染源之间δ11B-B混合曲线Fig.4 The δ11B-B mixing lines between uncontaminated boron in groundwater and other pollution sources
1.4 其他稳定同位素
金属稳定同位素是目前非传统稳定同位素的发展前沿. 随着测量技术的进步,铅同位素、铬同位素逐渐应用到环境污染识别中,成为识别特定重金属污染来源的有力工具[51]. 环境中有4种稳定的铅同位素,即204Pb、206Pb、207Pb和208Pb,一般用207Pb/206Pb、208Pb/206Pb 同位素比值的形式表示. 铅同位素质量大,同位素之间的相对质量差较小,在环境地球物理化学过程中难以发生明显的同位素分馏,并且已被证明在工业生产过程中也不会产生明显的同位素分馏[51],因此铅同位素可以较完好地保存其物源和成因的同位素特征. 这种特性使铅同位素在环境示踪中得到广泛应用. Grezzi等[52]利用铅同位素特征结合浓度数据,追踪土壤和地下水污染的来源和程度,结果表明城市化地区表面的土壤中铅同位素组成主要受机动车等人为影响. 与铅同位素类似,铬同位素间原子质量相对差别很小,生产活动中的铬同位素组成难以因外界条件发生改变[4]. 进入环境之后,铬同位素的分馏机制与硫同位素一样,主要是含氧阴离子的还原作用[53]. 在还原条件下,地下水中的Cr(Ⅵ)转化成Cr(Ⅲ),使得水体中剩余Cr(Ⅵ)的δ53Cr相对于污染源逐渐偏正. 例如,Kanagaraj等[53]利用铬同位素比值有效区分出地下水中铬污染的原因,发现相比于地质成因的地下水,制革厂污水及其附近的地下水中δ53Cr明显偏高. 同时,利用铬同位素对水体氧化还原条件较强的敏感性,可以根据Cr(Ⅵ)同位素组成指示其在水环境中的衰减程度. 另外,随着高分辨率色谱-同位素比值质谱技术的不断发展,有机单体同位素分析技术(CSIA)日趋成熟,为有机污染物的来源判识和污染过程示踪提供了有力工具[54]. 该技术目前可应用于有机物中碳、氢、氮、氧、氯、溴稳定同位素测试[55],可有效地识别地下水中有机污染物的衰减程度.
2 地球化学指示因子
某些具有源特异性的地球化学指标可以作为特定污染来源的示踪剂. 其中,合成有机污染物是地下水污染识别的重要指标,且能提供特定污染源的信息,具有广阔的利用前景.
2.1 卤化物
地下水中Cl-、Br-、I-属于保守的阴离子[56-57],在地下水迁移的过程中与环境介质的相互作用非常小[56],天然条件下,地下水中发生的物理过程(稀释、蒸发、混合等)可以改变它们的绝对浓度,但不会显著改变地下水的Cl/Br[58]. 各种污染来源的Cl/Br与Cl浓度的关系如图5所示. 图5中各端元之间的连线表示端元之间的混合作用,通过地下水中Cl/Br与Cl浓度的分布关系,可以大致判断其污染来源. 以以色列Dan地区为例,受污染的地下水受到生活污水和加勒比海水的影响,其Cl浓度升高,Cl/Br满足二者混合的结果[58]. 除Cl/Br外,I/Na与Br浓度的关系也可用于地下水中硝酸盐与盐度的溯源中. Panno等[59]描述了7种Na和Cl的自然和人为来源(包括农药、化粪池污水、动物粪便、垃圾填埋场渗滤液、海水、盆地深层盐水和道路除冰剂),并且发现在I/Na与Br浓度的关系中,碘化物的富集在降水中最大,其次是未污染的土壤水、地下水及垃圾渗滤液,进而为追踪地下水中可能的Na+和Cl-输入来源提供证据.
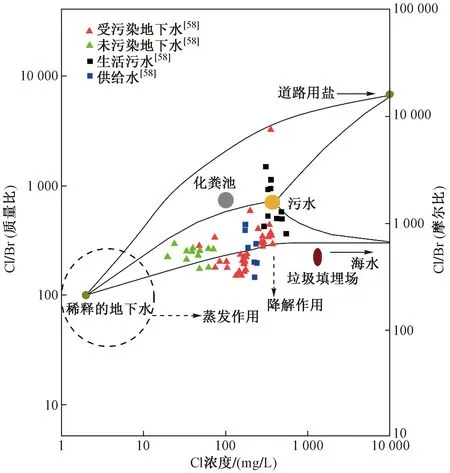
图5 Cl浓度与Cl/Br关系揭示的地下水污染来源Fig.5 The groundwater pollution sources induced by relationship between Cl/Br ratio and Cl concentrations
2.2 稀土元素
随着稀土元素消耗量的增长,环境中稀土元素数量呈现增加的趋势. 天然条件下,不同地下水中稀土元素的含量可能有所不同,但其分配模式基本一致,即标准化后的分配线近乎是一条平直的线. 受到污染的地下水,由于外在物源的输入,会影响其稀土元素的含量及分配模式[60]. 稀土元素钆(Gd)为磁共振成像中造影剂的主要成分. Gd/Gd*(Gd*为Gd的天然背景值)是衡量钆异常的指标,其值大于1,定义为正异常,表明环境中钆输入,研究发现这种正异常通常是人为输入造成的,如污水排放、垃圾填埋场渗滤等.
近年来,土壤、地表水、地下水环境中钆的正异常行为越来越显著. 钆异常被用于人为污染进入地下水环境中的有效示踪[61]. 钆络合物在人体内不经代谢直接排出体外[62],并且无法被污水处理厂处理,说明钆络合物既不吸附,又不共沉淀,也不与有机或无机颗粒状污水进行离子交换[63-64]. 进入环境中的钆络合物主要存在溶液中[65],并且在环境中的保守性较好,因此钆在水体中相对于其他稀土元素异常富集,表现出稀土元素分配模式与浓度的异常. 此外,据Kulaksiz等[66]报道,稀土元素镧(La)和钐(Sm)也被发现可用于识别莱茵河水是否受到工业污染. 对于地下水中更为精准的污染来源识别,有待进一步开展对稀土元素在环境中性质的研究.
2.3 新污染物
随着分析方法与技术的不断提高,环境中众多微量(浓度在ng/L~μg/L之间)且潜在危害难以估量的新污染物检出愈加频繁[67-69]. 这些新污染物主要为药品及个人护理品(PPCPs)、人造甜味剂、农药、消毒副产品等[70]. 与自然中大量存在的、非人为的背景指标(如主要离子)相比,地下水中一旦发现此类污染物,表明存在外来的人为输入,因此具有更显著地识别地下水污染的灵敏度[71]. 理想的溯源指示因子要求满足保守性及低检出限[72-73]. 保守性意味着新污染物是持久的,即具有抵抗生物降解、吸附及转化的能力[74],地下水中污染物含量基本不会损失,表现为持久地存在于地下水环境中[73]. 目前,应用最多的新污染物主要是药品及个人护理品和人造甜味剂,常见新污染物的环境检测浓度、用途和持久性特点如表1所示.

表1 新污染物溯源适用性
2.3.1药品及个人护理品
药品及个人护理品应用于地下水污染来源示踪前景广阔[89-90]. 地下水环境中检测出的持久性药品及个人护理品主要有卡马西平[91-92]、克罗米通[93-94]、普利米酮[73]、阿替洛尔[95]. 卡马西平是世界范围内使用量较大的药品及个人护理品的典型代表[93,96]. 并且在污水处理厂的各种物理化学过程中性质稳定,在污水处理厂二级处理的去除率极低(约为52%±3%)[95]. 进入环境中,由于其亲水性较强(lgKOW为2.45),不易被土壤介质吸附[93,96-97],且其他生物地球化学过程对其在环境中的影响较小,因此在地下水环境中相对其他PPCPs检出率和浓度较高. 与卡马西平类似,克罗米通也表现出环境持久性,其二级去除率为22%±20%[95],亲水性强(lgKOW为2.73),不易被吸附,因此可以作为污水中持久的指示因子. 另外,抗生素如磺胺甲恶唑也能在数千米的距离和数十年的时间尺度上持续存在[88],并已被用作地下水中的协同示踪剂[73].
药品及个人护理品类中某些易降解的污染物也被发现存在于区域性地下水环境中,如污水管网不发达或者不完善的化粪池分布多的地区,污染物通过污水泄漏和溢流等方式进入地下水中[98-99]. 这类污染物主要有咖啡因、布洛芬及对乙酰基酚. 咖啡因最早用来识别未处理污水的污染影响[84,100-102],其在污水处理厂的处理过程中去除率高达99%[100],对乙酰基酚在污水中浓度可达数百ppb[103],但经污水处理厂后迅速降至低于检出水平[89]. 因此如果在地下水中发现此类易降解的新污染物,表明地下水在近期受到了未经处理的污水影响. 易降解的污染物并不会单独存在于地下水中,将易降解的新污染物与同源的保守性指示因子相结合,考虑易降解污染物的衰减常数,可以估算污染发生的时间尺度.
2.3.2人造甜味剂
某些人造甜味剂被证明在地下水环境中具有持久性,并且与大多数新污染物相比,它们的生物及化学活性差[98-99]. 乙磺胺和三氯蔗糖是2种人造甜味剂,最常用于食品和饮料的生产中. 乙磺胺和三氯蔗糖在常规废水处理过程中化学稳定性好,去除率低[102,104-105],二者同时表现出相对较低的土壤吸附能力(lgKOW分别为-1.33和-1.0),并且在地下水环境中具有显著的持久性[103],浓度最高可达分别为33和24 μg/L[23]. 在自然pH条件下为亲水性离子化合物,具有极强的流动性. 在有机质丰富的有氧环境中,污染羽边缘位置存在三氯蔗糖的缓慢衰减[104]. Robertson等[105]发现在众多地下水环境中,三氯蔗糖可持续存在几个月到几年时间,可用于追踪受到病原体威胁的近期污染[105].
人造甜味剂甜蜜素和糖精经过污水处理厂处理之后,几乎全部被去除. 据Van-Stempvoort等[32]的研究,甜蜜素和糖精也经常在水环境中被检出,二者的浓度分别高达0.98和10.3 μg/L. Roy等[106]发现,垃圾渗滤液影响的地下水中糖精的检测浓度相比污水处理厂出水影响的地下水低,这为区分这2种污染源提供了可能.
3 指示因子的应用
理想的地下水污染溯源是仅利用一种或尽可能少的指示因子解决污染来源问题,但由于地下水受不同污染源的影响(见图1),导致污染物种类繁多、污染途径难辨. 各指示因子均存在自身局限性(见表2),多种指示因子联合使用显得尤为必要.

表2 地下水污染溯源关键指示因子
3.1 指示因子在不同场景下的溯源应用
硝酸盐与硫酸盐污染是地下水中常见的无机污染,特别在受农业面源影响的区域. 稳定同位素指示因子是示踪此类污染来源最常用的手段. 通过查明潜在污染来源的同位素特征,对比分析同位素特征以判断污染来源,甚至可以借助混合模型定量污染源的贡献率[107]. 环境同位素(如δ87Sr、δD-δ18O等)与描述地下水年龄的指标(如3H、14C、4He、CFC)常用于辅助识别地下水中污染的来源[24,107-108]. 此外,研究[109]表明,通过将硝酸盐和硫酸盐同位素耦合,还可以证明反硝化作用与黄铁矿氧化之间的联系. 地下水中硝酸盐的反硝化过程主要由两类细菌主导[110],一类是由异氧细菌利用有机化合物能量发生的反硝化作用;另一类是自养细菌从无机化合物的氧化(如硫化物的矿化)中获取能量从而产生反硝化过程. 对于可能存在第二类反硝化作用的地下水中,往往涉及硝酸盐与硫酸盐的连锁反应,这类反硝化过程通常由黄铁矿氧化引起,导致SO42-浓度增加和NO3-浓度减少,同时,δ15N-NO3-和δ18O-NO3-值增加,δ34S-SO42-和δ18O-SO42-与硫酸盐形成的物源一致,即基本不变. 利用这种关系,Otero等[109]证明了硝酸盐污染的地下水中反硝化过程的发生与含水层中黄铁矿的氧化有关.
硼同位素在示踪海水入侵、生活污水入渗以及填埋垃圾渗滤液影响等方面都取得了成功应用. Bassett等[111]研究表明,利用硼与硼同位素能够有效地区分得克萨斯州伊帕索地区处理过的污水与作为灌溉水的天然盐水对地下水的影响. Nigro等[46]利用硼同位素与氚对城市垃圾填埋场的地下水进行表征,结果显示未受污染的地下水中硼同位素比值为19.31‰,而受到污染的地下水中为4.37‰~9.41‰. 污水和粪肥来源的硝酸盐同位素比值存在重叠,导致硝酸盐同位素难以区分这两类污染来源,而硼同位素是硝酸盐的共同迁移体且在硝酸盐的转化过程(硝化、反硝化作用)中几乎不发生同位素分馏[112]. 污水和化肥中的δ11B值相对较低,通常为-6‰~13‰[112-114];粪肥中的δ11B值相对较高,其范围为7‰~42‰[47,114-115]. 因此,对于可能存在污水与粪肥污染的地下水,硼同位素与硝酸盐同位素的联合使用是硝酸盐来源识别的有用工具[113-114].
Cl/Br常用于农业地区或者沿海地区地下水硝酸盐和盐度来源的示踪. 在农业生产地区,Cl/Br与Cl浓度的变化往往能够弥补同位素溯源的信息不足问题[24]. 众多学者开展了不同土地利用下Cl/Br变化的研究,如Koh等[108]利用Cl/Br相对NO3-浓度的变化识别不同土地利用类型(自然区、果园、稻田及住宅区)对地下水质量的影响,效果好于稳定硝酸盐同位素,二者也可结合使用. Pastén-Zapata等[116]将硝酸盐氮氧稳定同位素及不同卤化物比值(Cl/Br-Cl、I/Na-Br)应用于墨西哥农业生产地区,查明了不同土地利用类型(农业用地、住宅用地、灌丛与草地)下硝酸盐污染来源及其转化情况,发现在此研究区I/Na对Br浓度关系图是非常有效的工具,可以实现肥料、污水和垃圾填埋3种污染来源之间的有效识别.
对于污水处理厂、化粪池、垃圾填埋场等点源造成的地下水污染,人为输入的污染物是最直接的污染指示因子. 稀土元素钆异常的应用是最为常见的,钆异常具有追踪污水的潜力. 由于钆异常行为对污染指示作用的认识还不完善,大多数的研究将钆异常与其他指示因子(如硼同位素)结合使用. 持久性新污染物对来自污水处理厂[23,115,117]、化粪池、垃圾填埋场的污染输入有良好的示踪作用. 通常认为单个示踪剂难以明确污水对地下水的影响[118]. 联合多种持久性的新污染物(如三氯蔗糖和卡马西平[119]),进一步纳入证据权重的方法,增强对污染来源的识别. Van-Stempvoort等[73]通过调查加拿大Jasper与Barrie地区地下水中多种人造甜味剂、药品及个人护理品含量,发现安赛蜜是一种普遍存在的保守性污水指示因子,利用其他新污染物与安赛蜜的比值发现,Jasper场地受到单一污染源的影响(普里米酮、卡马西平与安赛蜜的比值均在污染羽内表现一致),而Barrie场地由多种污水混合影响(磺胺甲恶唑、卡马西平、普里米酮与安赛蜜的比值均在污染羽内表现不一致). 然而,抗降解性使持久性污染物无法区分未处理的和处理过的污水. 研究发现,持久性与易降解污染物的组合可有效地解决这一问题[79,91,99,102-103,120],并且通过对污染物降解半衰期的研究,可以估算受未处理污水的影响时间. Currens等[89]利用与未经处理的人类排泄物有关的对乙酰氨基酚与保守性三氯蔗糖的比率(ACE/SUC)确定受污染水体中未经处理污水的年龄信息,并利用三氯蔗糖的绝对浓度估计在污染较轻水体中稀释的程度.
与单个的面源、点源污染不同,由多种污染源共同控制的区域(如城市周边环境),往往存在近期与历史污染、点源与面源污染,各种复杂的污染来源使污染的识别与溯源更为困难. 解决这一问题可使用针对特定污染源的示踪剂(如新污染物),结合更常规的示踪剂(如稳定同位素和主要离子),提供更多的示踪信息[70,81,93]. 这种“共同示踪剂”兼具传统示踪剂溯源信息全面、适用性强的特点,又满足对潜在特定污染源的精准识别,解决了传统示踪剂在各污染源之间指标浓度和(或)同位素比值重叠带来的溯源困难. Mccance等[70]联合使用稳定同位素(δ2H-H2O、δ18O-H2O、δ15N-NO3-、δ18O-NO3-和δ13C-DIC),表征停留时间的放射性同位素(3H和14C),以及卡马西平、西玛津和磺胺甲基恶唑,区分了澳大利亚污水处理厂周围多种潜在的污染源. 然而,迄今为止只有少数研究尝试将新污染物与传统的方法相结合[23,121],主要是由于缺乏一致的检测和分析方法来评估新污染物[92]. 未来这种“共同示踪剂”的组合可能变得更加普遍,为研究混合源环境中污染源提供新的手段.
3.2 指示因子与其他溯源方法的联合使用
由稳定同位素和地球化学指标构成的污染源指示因子体系适用于解决面源污染、点源污染以及多种污染源造成的地下水污染溯源问题. 考虑到更为复杂的污染状况以及溯源的其他要求,如识别污染的位置与时间等,将指示因子与其他方法结合使用变得尤为重要,有助于全面认识污染过程[56]. 稳定同位素在此方面的应用发展较为完善,关于新污染物指标与其他方法的结合是较为新颖的方法. Rona等[122]利用卡马西平和氯化物作为示踪剂,结合地下水三维运移模型模拟污水回灌引起的地下水污染. Stefania等[123]以意大利某垃圾填埋场影响的地下水为研究对象,将4种人造甜味剂(糖精、甜蜜素、安赛蜜、三氯蔗糖)与其他水化学数据结合作为统计分析的对象,利用多元统计分析划分地下水污染的类型,并进一步利用人工甜味剂、粒子跟踪与运移模型实现了对新、老垃圾填埋场2种潜在污染源的鉴定. 此外,微生物指标是指示粪便污染常用的指标,大肠杆菌、埃希式杆菌和肠球菌是典型的粪便污染指示菌[124]. 虽然在适宜的条件下,这些微生物会在水体中繁殖,导致微生物指标的浓度超过指定水平,对分析造成干扰,但是由于这种方法简单、方便,仍然广泛用作辅助指标. 某些研究将其作为特定污染源的指示因子,来探究其他指示因子的适用性. 如Sauvé等[96]发现在城市周边的雨水、溪流收集系统中人为示踪剂与粪大肠菌群普遍存在,表明高度城市化城市环境中的雨水收集系统被下水道广泛污染,并且人为示踪剂咖啡因与粪大肠菌群的相关性较好,认为咖啡因有潜力被用作该地区污染的化学指标. 而Preziosi等[125]则将微生物数据与水文地球化学、同位素数据结合起来,以揭示自然和人为污染源对垃圾填埋场周边地下水的影响.
总之,目前虽然地球化学指纹方法可以通过多种指示因子联合使用解决污染识别与溯源的问题,并且某些新污染物组合也可以实现对污染位置与时间的界定,但是对于越来越复杂的污染过程,结合数学统计分析与模型优化的方法仍是目前较为经济、可靠的选择.
4 结论与展望
a) 目前稳定同位素是应用最成熟的指示因子,适用于面源污染及局部的点源污染,但同位素特征值重叠以及潜在的同位素分馏给污染源的识别带来了不确定性.
b) 相比于稳定同位素,保守性质的地球化学因子(如Cl、Br等)可以指示特定源的污染贡献,借助不同源之间的差异可实现污染的识别诊断. 源特异性的人为输入污染物(如钆、新污染物)成为近年来研究的热点,但在多种污染源共同作用下实现准确识别也存在一定难度.
c) 多种指示因子的联合使用是解决实际溯源问题最常用的手段,可减少不确定性,并有助于发现单一指示因子无法识别的潜在污染源和污染过程. 指示因子的选择应综合考虑潜在污染源特征,选择适合当前潜在污染源的指示因子搭配使用,必要时结合数学统计分析与模型优化手段.
d)指示因子的研究还存在诸多挑战. 对于稳定同位素来说,有机单体同位素分析技术的改进以及金属稳定同位素测试精度的提升,将有望实现对地下水中有机污染以及金属污染物来源与转化过程的示踪,从而实现场地污染的精准识别. 另外,伴随新污染物在地下水中迁移转化的过程以及分析检测技术的成熟,将有助于发现更多特异性的指示因子.

