黄芪有效成分抗动脉粥样硬化机制研究进展
王丽娜,张磊,戴霞✉
(1.山东中医药大学,山东 济南 250355;2.山东中医药大学附属医院,山东 济南 250011)
动脉粥样硬化(atherosclerosis,AS)是一种慢性进行性动脉血管炎症性疾病,在规范应用他汀类等降脂药物并初见成效的当下,仍是造成心脑血管疾病发病率和病死率升高的主要原因[1]。因此,探索一种新的补充甚至是替代疗法是目前抗AS 研究的核心目标。中医学以其多通路、多靶点的治疗特点在AS治疗中备受青睐。根据发病部位及症状的不同,通常将AS归属于“胸痹”“中风”“脉痹”“头痛”“眩晕”等范畴,以本虚标实立论,其中本虚以气虚为主,而标实以血瘀为先[2],故临床治疗AS常用益气活血法[3]。黄芪素有“十方八芪”之称,被誉为“补气圣药”。黄芪在《本草经集注》中被记载具有“逐五藏间恶血、益气”之用,《本草纲目》谓其:“益元气,二也……排脓止痛,活血生血,内托阴疽,为疮家圣药,五也……”,以上均说明黄芪本身具有益气活血之效。另有研究发现,黄芪是中医临床治疗AS 的核心药物之一[4]。现代药理学研究表明,黄芪及其成分具有多种生物活性,如调节血脂、免疫调节、抗氧化、抗炎、抗病毒等[5−6],被广泛应用于心血管、内分泌、免疫及肿瘤等领域。另外,有研究指出黄芪能从保护血管内皮、抗氧化应激、抑制炎症反应等方面干预AS[3,7]。因此,通过梳理近几年国内外相关文献,本文基于AS 的病理特点,从参与AS 的主要细胞的角度对黄芪主要有效成分抗AS的机制进行综述,以期为黄芪等中药干预AS的研究及临床应用提供一定的参考。
1 具有抗AS作用的黄芪有效成分
黄芪为豆科黄耆属植物,根部入药,以蒙古黄芪和膜荚黄芪两种基源为主[8]。从现代药理学角度出发,中药发挥疗效主要依靠其核心成分,即有效成分。通过文献检索发现,黄芪有效成分包括黄芪多糖、黄芪甲苷、黄芪黄酮类,其中黄酮类还包括槲皮素、山柰酚、芒柄花黄素等。现将黄芪有效成分抗AS 的研究总结如下,结果见表1~表3。

表1 黄芪多糖抗AS研究

表2 黄芪甲苷抗AS研究

续表2
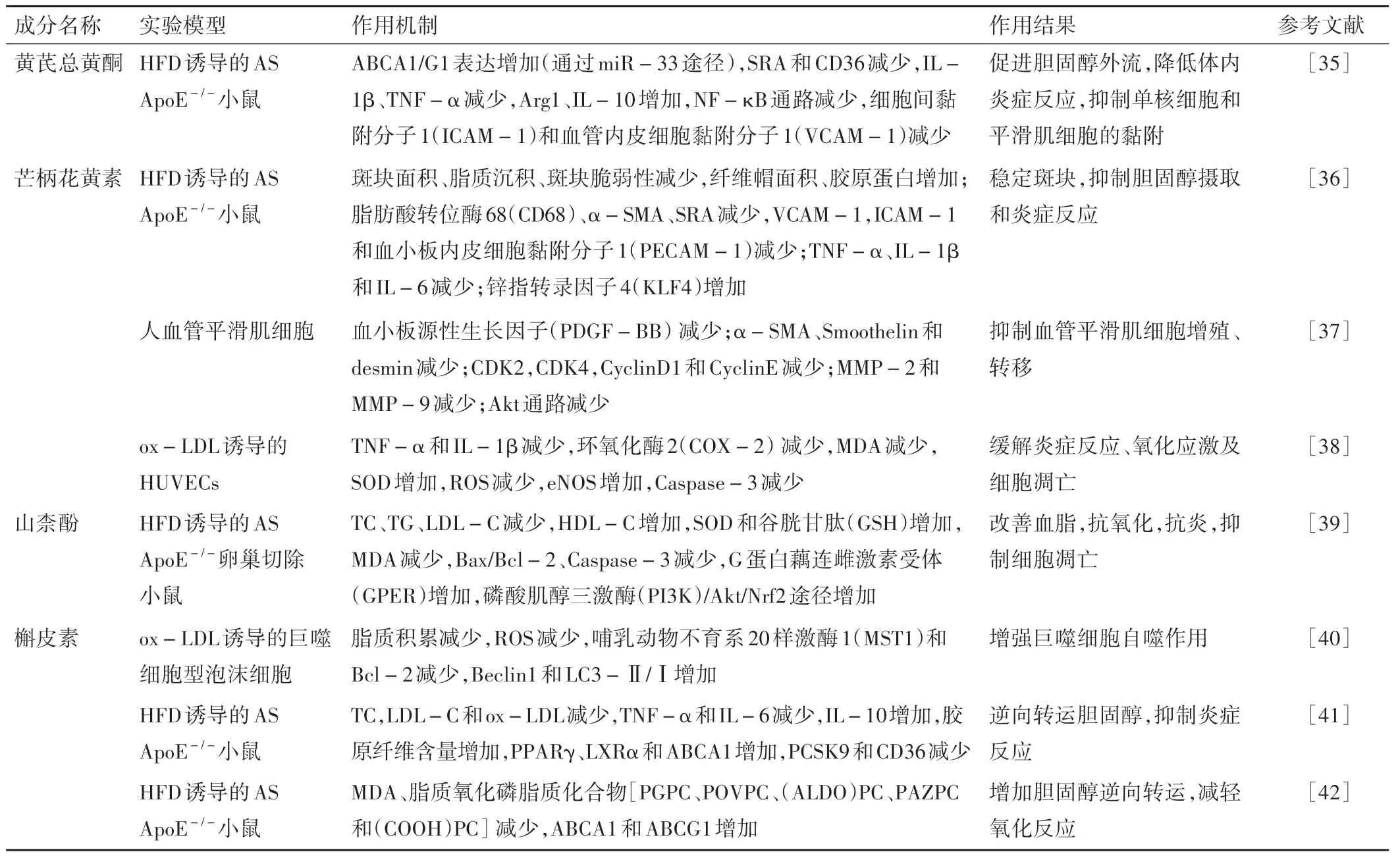
表3 黄芪黄酮类抗AS研究
2 黄芪有效成分抗AS作用机制
2.1 保护血管内皮细胞
2.1.1 抑制炎症反应
在抑制炎症反应过程中,主要通过调控相关炎症信号因子的表达来改善内皮细胞损伤。NF-κB 是参与炎症反应的重要核转录因子之一,通过下调NF-κB信号通路来减轻AS炎症,已成为目前中药有效成分抗AS 研究的热点角度[43],黄芪多个成分可通过此通路抑制炎症反应[32,44−45]。TLR4是NF-κB的上游信号,槲皮素可以通过减弱内皮细胞中的TLR/NF-κB 信号通路来抑制ox-LDL 诱导的内皮白细胞黏附,并减少高脂饮食诱导的AS 大鼠炎症反应,从而有效保护内皮细胞。CD40 信号与AS 的炎症反应密切相关,该信号可在ox-LDL、TNF-α 等刺激下上调于内皮细胞内的表达量[46]。研究发现,黄芪甲苷能够抑制内皮细胞中的CD40 信号,从而降低其下游炎症因子TNF-α、sVACM-1、IL-6 和IL-8 的含量,显示出良好的抗炎特性[23]。另外,NF-κB 又可促使NLRP3 炎症小体形成[47],NLRP3炎症小体基因的沉默可减慢小鼠AS的进展[48],而黄芪甲苷具有下调NLRP3蛋白表达的作用[28]。
2.1.2 抗氧化应激
在抗氧化应激方面,下调机体的ROS 及活性氮(RNS)至关重要,而SOD 等各种内源性抗氧化酶能够在一定程度上清除ROS。有研究发现,在体外干预HUVECs 氧化应激损伤模型时,黄芪多糖能够升高Cu/Zn-SOD蛋白表达,提高NO释放量,并下调细胞凋亡率,有效缓解内皮细胞损伤[16]。张敬芳等[18]亦从体内实验的角度验证了黄芪多糖可以通过氧化应激通路干预AS,并从形态学进一步证实。黄芪甲苷能够提高氧化应激后HUVECs 的SOD 活性,降低线粒体ROS 含量及NADPH 氧化酶活性,使线粒体膜电位显著增高,从而提升线粒体抗氧化能力[25]。有研究指出,PPARγ信号的激活效应有益于治疗AS等心血管疾病[49],芒柄花黄素可以通过PPARγ信号通路发挥抗氧化作用[38]。
2.1.3 调节脂质代谢
在调脂研究方面,并未发现有对黄芪有效成分降低LDL 含量进而保护血管内皮细胞作用的直接研究。但王意君等[50]发现,黄芪注射液能够对游离脂肪酸导致的主动脉环损伤产生保护作用,具体表现为通过下调NF-κB 表达,增加内皮源性NO 合成/释放。宋杰等[17]在前人工作基础上进一步从细胞角度研究了黄芪多糖对血管内皮细胞的保护作用,其机制是通过活化被游离脂肪酸所抑制的AMPK-eNOS通路所实现的。
黄芪的有效成分具有抑制炎症反应、抗氧化应激、调脂以及抗细胞凋亡[24,38]等作用,能多靶点、多通路地参与内皮细胞的保护,从而为黄芪干预AS早期斑块扩大及后期血栓形成的研究提供理论参考。
2.2 阻止巨噬细胞泡沫化
巨噬细胞泡沫化是指巨噬细胞表面的清道夫受体识别并吞噬ox-LDL 后转化成泡沫细胞的过程,这一过程是AS发生发展的关键一步[51]。因此,阻断该过程的任意一个环节均可以控制AS的进展,故调节脂质水平和分布以及干预巨噬细胞对于治疗AS 来说至关重要。
2.2.1 促进胆固醇逆向转运
胆固醇逆向转运(RCT)的强度是巨噬细胞向泡沫细胞衍变的关键因素。有研究指出,ABCA1、SR-B1等蛋白的表达水平与RCT 的强度呈正相关[52]。黄芪多糖[22]、黄芪甲苷[29,32]、黄芪总黄酮[35]能够通过上调ABCA1 的表达,降低脂质含量,从而抑制泡沫细胞生成。其中,黄芪甲苷和黄芪总黄酮通过miR-33 途径来发挥对ABCA1的调控作用。PCSK9在LDL-C代谢中起着关键作用,它能够促进LDL-R的降解,LDL-R能够通过结合并内吞LDL 调节胆固醇代谢[53]。因此,PCSK9目前成为降脂治疗的新靶点。邹红钰等[19]发现黄芪多糖具有下调THP-1 源性巨噬细胞PCSK9 蛋白及基因表达的作用,转录后水平反馈性升高LDL-R蛋白表达,并初步证明PPAR-β/δ 是其可能的作用通路之一。此外,黄芪甲苷、槲皮素也被发现具有靶向调控PCSK9的作用[26]。
2.2.2 促进巨噬细胞自噬
在一定范围内,巨噬细胞自噬是机体的抗AS保护机制。Beclin1 基因是一种哺乳动物特有的自噬特征性基因,LC3-Ⅱ被认为是自噬过程的特征蛋白,用来反应自噬体分子量。张志鑫等[31]用黄芪甲苷干预巨噬细胞后发现干预组自噬小体较对照组数量增多,LC3-Ⅱ和Beclin1 蛋白的表达水平上调,充分说明了黄芪甲苷具有诱导巨噬细胞自噬的作用,并通过小鼠体内实验进一步验证自噬是通过PI3K/Akt/mTOR 信号通路调控的。Krüppel 样转录因子2 在AS 中发挥重要作用,可以抑制自噬调节剂混合谱系激酶结构域样假激酶(MLKL)的表达。MA 等[54]发现,毛蕊异黄酮可以通过KLF2/MLKL 信号通路来上调巨噬细胞自噬,减轻巨噬细胞浸润,从而抑制泡沫细胞的形成、炎症和细胞凋亡,为黄芪抗AS 研究提供了新的研究角度。MST1是一种丝氨酸-苏氨酸激酶,参与多种生物学功能,包括下调自噬、细胞凋亡等[55]。槲皮素可以在下调MST1的同时上调LC3-Ⅱ及Beclin1 蛋白的表达来诱导巨噬细胞自噬[40]。需要注意的是,巨噬细胞自噬的结果并不能代表细胞的死亡,因此对于黄芪诱导巨噬细胞自噬的研究,需要在前人基础上验证有效成分干预后巨噬细胞的存活情况,以使抑制抗AS作用的结果更具说服力。
2.3 抑制血管平滑肌细胞增殖和迁移
VSMC 位于血管壁中膜,在泡沫细胞分泌的生长因子和促炎因子的作用下,VSMC 增殖、迁移到血管中膜,并与泡沫细胞、巨噬细胞共同参与斑块的形成。有研究表明,泡沫细胞除来源于巨噬细胞外还有一部分来自平滑肌细胞,即平滑肌细胞源性泡沫细胞[56]。黄芪有效成分同样对血管平滑肌细胞增殖和迁移有抑制作用。
有研究指出,持续高糖环境可以促进VSMC 的增殖与迁移[57]。高惠娟等[58]研究发现,黄芪能够抑制高糖诱导的VSMC 增殖和迁移,该过程主要通过调控miR-18a-5p/MFN2 轴实现。p38 MAPK 信号通路是经典的炎症反应通路,除此之外,还能通过调节细胞周期相关蛋白的表达参与VSMC 增殖以及调节细胞迁移[59]。MMP-2是调节是细胞迁移的关键因素,CHEN等[34]用黄芪甲苷干预PDGF-BB 诱导的人表皮VSMC模型,发现黄芪甲苷能上调细胞周期相关蛋白,下调平滑肌细胞特异性抗原、α-平滑肌肌动蛋白、肌间线蛋白3 种人表皮VSMC 分化表型标志物的表达水平,以此说明黄芪甲苷具有抑制VSMC 增殖与迁移的作用;并通过进一步实验发现黄芪甲苷是通过抑制MMP-2蛋白表达来抑制细胞迁移的,而发挥增殖与迁移作用最终是通过下调p38 MAPK 信号通路实现的。PDGF-BB 也能正向调节血管平滑肌细胞的迁移,芒柄花黄素能够抑制PDGF-BB 刺激下的体外细胞模型[37]。
2.4 抑制血小板聚集
内皮细胞受损后会激活血小板和凝血系统,从而形成动脉血栓。因此,阻止血栓形成亦是AS 治疗目标,而在血小板是在该过程中发挥关键作用的细胞。血栓素A2(TXA2)和前列环素I2(PGI2)均是由血小板产生的花生四烯酸的代谢活性物质,TXA2促进血小板聚集和血管收缩,PGI2 则与其作用相反;生理情况下,两者处于相对平衡,但在AS 等已形成血栓的疾病中TXA2/PGI2值则会升高[60]。早先有研究发现黄芪总皂苷有抗血小板聚集的作用,其机制可能与通过升高PGI2 含量来降低TXA2/PGI2 值以及升高NO 保护内皮细胞有关[61]。黄芪是中医临床治疗血小板聚集的核心药物[62],而近年来鲜有关于黄芪有效成分抗血小板聚集的研究。最新研究发现,与正品黄芪成分高度相似的黄芪属植物——梭果黄芪具有抗血小板聚集的特性,主要作用途径是抑制TXA2 活性[60]。因此,关于黄芪有效成分通过抗血小板聚集来抗AS 的研究仍需大量基础实验进一步探讨。
3 小结与展望
AS多累及冠状动脉、脑动脉、颈动脉等大动脉,继发于高血压、糖尿病、高血脂等基础代谢类疾病,一旦形成,大都不可逆,目前治疗多以干预原发病来防止靶器官损害为原则。所以深入探索AS发病机制,从疾病本身入手成为目前AS 治疗的研究重点。黄芪有效成分可以改善和治疗AS,并且相关研究已取得一定的进展。因此,本文以AS的病理过程中主要的参与细胞为线索,从黄芪有效成分保护内皮细胞、阻止巨噬细胞泡沫化、抑制血管平滑肌迁移和增殖以及抗血小板聚集的角度探讨了其抗AS 的途径,并发现黄芪抗AS 具有多成分、多通路、多靶点、多效果的特点。
尽管既往关于黄芪有效成分抗AS 机制的国内外研究甚多,但仍有部分问题亟待改善。①炎症反应、氧化应激或细胞凋亡等可发生于AS多个阶段,应完善研究模型,将上述反应的研究对象具体到病理环节;②黄芪有效成分抗血小板聚集等血栓形成的阶段缺乏大量严谨的基础实验来充实;③研究多停留在动物实验和细胞实验阶段,缺乏单一制剂相关的临床试验评价以及循证医学研究;④黄酮成分存在于多种植物中且黄酮化合物种类多样,通常很难使研究标准化,因此应控制黄芪黄酮中化合物的来源,优化干预手段,为进一步研究黄芪抗AS的机制奠定良好的基础。可见,针对黄芪有效成分抗AS 机制的深入研究,能够为AS 治疗药物的研究与开发起到一定的推动作用。

