艾叶油GC-FP 研究
★ 黎艳刚 李丽云 孙文强 周云龙 朱海 丁江生(云南省药物研究所/云南省中药和民族药新药创制企业重点实验室 昆明 650111)
中药指纹图谱是从物质基础角度出发,运用现代分析测试技术对不同种类或者产地的中药材经预处理后通过一定的构建办法得到的能体现该种药材质量的色谱或光谱图,是一种综合的、可量化的鉴定手段。作为一种能整体反映中药内部成分的新技术,中药指纹图谱是目前公认的较为有效的中药质量控制技术,可作为鉴别中药真伪和优劣的依据[1]。
艾叶是我国传统中药材,为菊科植物艾的干燥叶,夏季花未开时采摘,除去杂质,晒干[2];最早在《诗经》中就有记载,主产于河南、河北、安徽、湖北、山东、江西等地[3]。其化学成分主要有挥发油、黄酮类、三萜类、鞣质及微量元素等[4],具有温经止血、散寒止痛等作用[2],其中挥发油已成为研究的热点,主要成分有α-蒎烯、β-侧柏酮、樟脑、反式石竹烯等[5]。目前已应用于药品、食品、保健品等领域,开发前景广阔。
艾叶油为菊科植物艾叶经水蒸气蒸馏提取出来的挥发油,具有抗菌、消炎、平喘、祛痰等活性[6-7]。艾叶油化学成分复杂,且各成分含量存在较大差异[8],2020 年版《中华人民共和国药典》艾叶药材的含量测定只控制了桉油精和龙脑的含量,1977 年版《中华人民共和国药典》艾叶油的质量标准沿用至今,该质量标准未对含量进行控制,且现有文献未见艾叶油气相色谱指纹图谱的报道。故采用GC 法建立了艾叶油气相色谱指纹图谱的研究方法,以更全面、准确、有效地控制艾叶油的质量。
1 材料与方法
1.1 仪器
Agilent 6890N 气 相 色 谱 仪(配 有 自 动 进样器、柱温箱、FID 检测器和Agilent 色谱工作站,美国Agilent 公司);SPB-3 全自动空气发生器(北京中惠普分析技术研究所);载气为高纯氮气(99.999%);燃气为高纯氢气(99.999%);EX125ZH 电子天平(奥豪斯仪器有限公司);2012 版《中药色谱指纹图谱相似度评价系统》(V2.0)。
1.2 试药
α-蒎烯对照品(中国食品药品检定研究院,批号为110897-201803,纯度为99.90%);桉油精对照品(中国食品药品检定研究院,批号为110788-201707,纯度为100.00%);右旋龙脑对照品(中国食品药品检定研究院,批号为110688-201602,纯度为99.60%);β-石竹烯对照品(PaNPH 公司,批号为FC040301,纯度为94.90%);艾叶油样品来源于不同的厂家及实验室提取,见表1;正己烷为分析纯。
1.3 色谱条件
BD-1 毛细管柱(30 m×0.32 mm×0.25 μm);进样口温度280 ℃;FID 检测器温度280 ℃;柱温40 ℃,保持5 min,以1.5 ℃/min 升至70 ℃,再以5 ℃/min 升至200 ℃,保持5 min;流速:1 mL/min;进样量:1 μL;分流比为10∶1。
1.4 对照品溶液的制备
分别称取适量的α-蒎烯、桉油精、右旋龙脑、β-石竹烯,用正己烷制成混合对照品溶液。
1.5 自提挥发油的制备
按2020 年版《中华人民共和国药典》四部(2204 挥发油测定方法)用法进行操作。
1.6 供试品溶液的制备
精密称取,艾叶油样品50 mg,置50 mL 量瓶中,加正己烷至刻度线摇匀,滤过,取其续滤液作为供试品溶液。
1.7 方法学考察
1.7.1 稳定性实验 取同一样品(编号S1),按“1.6”项下方法制备供试品溶液1份,分别在0,2,4,6,8,10,12,18 和24 h 按“1.3”的色谱条件进样检测。
1.7.2 精密度实验 取同一样品(编号S1),按“1.6”项下方法制备供试品溶液1 份,按“1.3”的色谱条件连续测定6 次。
1.7.3 重复性实验 取同一样品(编号S1),按“1.6”项下方法制备供试品溶液6 份,按“1.3”的色谱条件进行测定。
1.8 供试品测定
取11 批不同来源的艾叶油,按“1.6”项下方法制备供试品溶液,按“1.3”的色谱条件进行测定。
2 结果
2.1 稳定性实验
以桉油精的保留时间为参照,计算各共有峰的相对保留时间,各共有峰相对保留时间RSD均小于0.5%;以桉油精的峰面积为参照,计算各共有峰的相对峰面积,各共有峰相对峰面积RSD均小于3.0%,表明样品溶液在24 h 内稳定。
2.2 精密度实验
以桉油精的保留时间为参照,计算各共有峰的相对保留时间,各共有峰相对保留时间RSD均小于0.5%;以桉油精的峰面积为参照,计算各共有峰的相对峰面积,各共有峰相对峰面积RSD均小于3.0%,表明仪器精密度良好。
2.3 重复性实验
以桉油精的保留时间为参照,计算各共有峰的相对保留时间,各共有峰相对保留时间RSD均小于0.5%;以桉油精的峰面积为参照,计算各共有峰的相对峰面积,各共有峰相对峰面积RSD均小于3.0%,表明具有较好的重现性。
2.4 艾叶油指纹图谱的建立与分析
采用11 批不同来源的艾叶油建立艾叶油的GC 指纹图谱,见图1。以桉油精(S)为参照峰,采用2012 版《中药色谱指纹图谱相似度评价系统》(V2.0)处理数据,经多点校正,以中位数法生成对照指纹图谱,并计算各艾叶油样品图谱与对照指纹图谱的相似度。结果11 批艾叶油有17 个共有峰,其指纹图谱匹配图见图1B,经过与对照品对比,确认了4 个特征指纹峰,即共有峰1 为α-蒎烯、共有峰6(S)为桉油精、共有峰8 为右旋龙脑、共有峰13 为β-石竹烯。见表1。
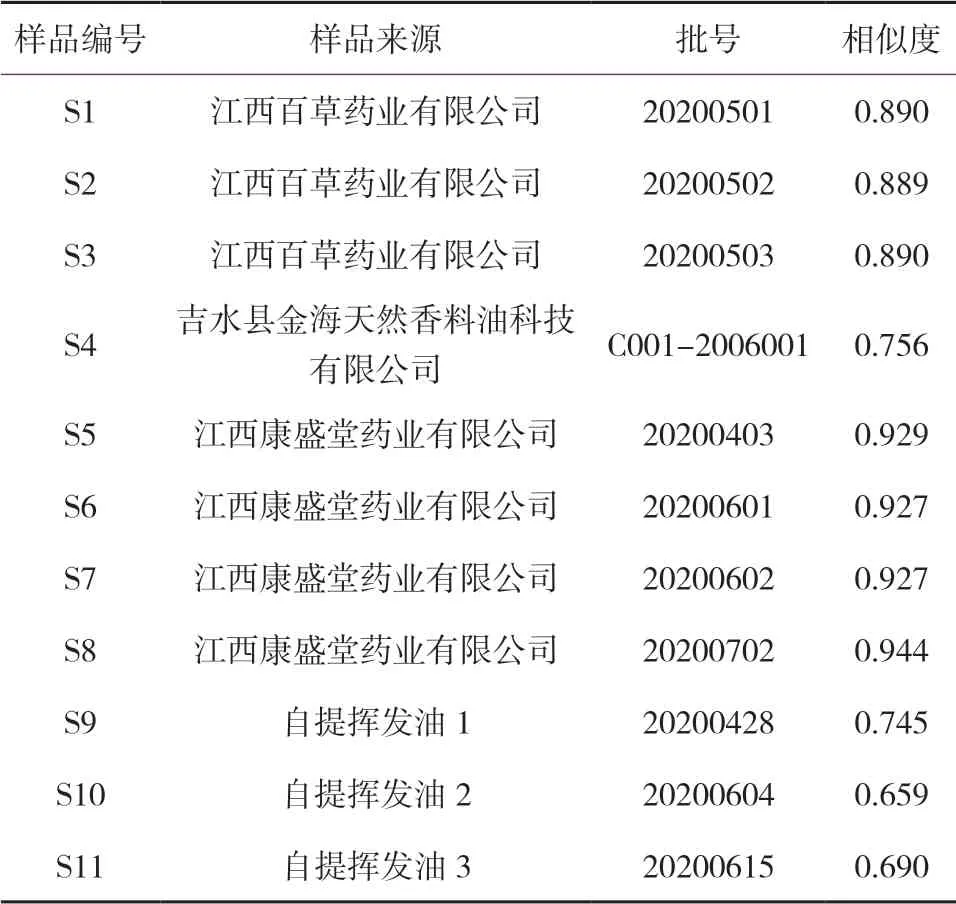
表1 艾叶油来源信息及GC相似度计算结果
江西百草药业生产的艾叶油和康圣堂生产的艾叶油GC 指纹图谱与对照指纹图谱之间的相似度均较高,吉水县金海生产的艾叶油与实验室自提的艾叶油相似度较近且与对照指纹图谱之间的相似度较低。见图1。
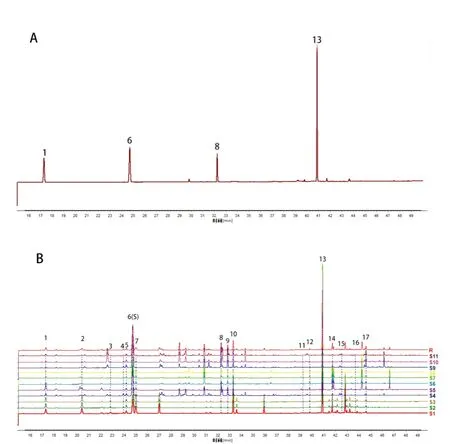
图1 艾叶油GC指纹图谱
2.5 艾叶油样品聚类分析
以GC 指纹图谱共有峰相对峰面积作为特征指标,采用SPSS 统计软件对艾叶油进行聚类分析,采用组间均连法,以欧氏距离为测度进行分类处理,聚类谱系见图2。从聚类结果可知S1,S3,S2归为第一类(百草药业艾叶油);S6,S7,S8,S5归为第二类(康盛堂艾叶油);S10,S11,S4,S9归为第三类(金海及自提艾叶油)。
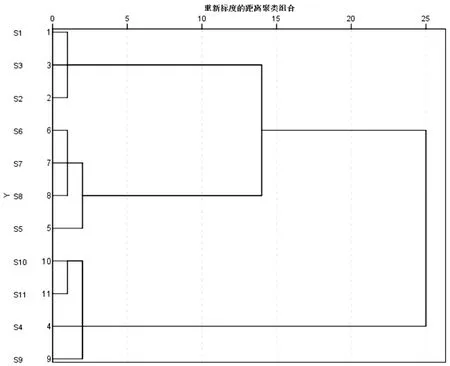
图2 艾叶油样品聚类分析树状图
3 结论
采用国家药典委员会的相似度评价系统计算的相似程度和SPSS 系统软件进行的聚类分析结果其相似性较强,都能将金海及自提的区分开,但也有着一定的区别,结合2 种分析方法,发挥各自优势,能有效地区分不同来源的艾叶油,为临床用药提供科学参考依据。
4 讨论
艾叶油中含有α-蒎烯、桉油精、侧柏酮、右旋龙脑、β-石竹烯等挥发性成分,2020 年版《中华人民共和国药典》艾叶药材质量标准中含量测定采用桉油精和龙脑为其质量控制指标。桉油精为所有艾叶油中所共有,其质量稳定,将其作为内参照峰,所得相似度结果良好,各特征色谱峰均能良好对齐。
《中华人民共和国药典》记载艾叶具有小毒[2],据研究表明β-侧柏酮[9]是有毒性的一类成分,出峰时间为29.26 min,样品S1、S2、S3 号为未检测到β-侧柏酮,推测其原因:一是可能艾叶原药材中不含β-侧柏酮,二是艾叶油的提取厂家对艾叶油做了相应的减毒处理。其他厂家及自提艾叶油中β-侧柏酮含量较低且高低不同,说明不同厂家及自提艾叶油中的β-侧柏酮的含量与艾叶生长条件、采收时期、干燥条件、储藏条件、储存时间等都有一定关系。
本研究所建立的艾叶油GC 指纹图谱研究方法操作简单、重现性好且稳定可靠。结合2012 版《中药色谱指纹图谱相似度评价系统》(V2.0)和SPSS软件聚类分析处理数据,能有效判别不同厂家及自提艾叶油之间的差异,能初步区别并推测艾叶油的生产厂家,为中医临床用药提供科学依据。此外,本研究所建立的检测方法还可以用于艾叶油中α-蒎烯、桉油精、右旋龙脑、β-石竹烯4 个主要活性成分的含量测定,为艾叶油的质量评价提供了参考。

