乌司他丁通过抑制铁死亡减轻重症急性胰腺炎模型的急性肾损伤
周少英, 王玉梅, 刘 博, 杨 珍, 李欢欢, 陈志飞, 苏 静
(1.河北省邯郸市中心医院, 河北 邯郸 056008 2.河北省邯郸市第一医院中西医结合科, 河北 邯郸 056002)
【关键字】 胰腺炎; 乌司他丁; 铁死亡; 肾损伤
急性胰腺炎(AP)是胃肠道疾病住院的主要原因,由于生活习惯改变和饮酒增加,其发病率逐年增加[1]。AP的严重程度分为轻度、中度和重度,轻度急性胰腺炎不会危及生命,但中度至重度病例可导致高死亡率,且重度 AP(SAP)其发病率和死亡率明显高于中度SAP,同时,持续超过48h的持续性器官衰竭的死亡率约为50%[2]。急性肾损伤(AKI)是急性胰腺炎患者一种常见且显著的并发症,发病率在10%~42%,死亡率高达约80%[3]。急性肾损伤的组织学特征为肾小管细胞死亡和炎症,被认为是诱发因素,铁死亡是一种铁和ROS依赖的调节细胞死亡形式,它涉及一系列独特的形态学、生化和遗传特征,不同于其他类型的调节细胞死亡,铁死亡与多种生理和病理过程有关,包括癌症、AKI、神经退行性疾病、缺血/再灌注损伤和T细胞免疫[4]。值得注意的是,在所有组织中,肾脏似乎对铁依赖性铁死亡最敏感。铁死亡调节剂谷胱甘肽过氧化物酶4(GPX4)失活通过触发小鼠肾小管细胞的铁死亡来诱导急性肾衰竭。乌司他丁(Ulinastatin,UTI)是一种来源于人尿液的糖蛋白,分子量为67kDa,可作为多种蛋白酶的抑制剂,包括胰蛋白酶,胰凝乳蛋白酶,弹性蛋白酶和各种胰腺酶[5]。多项临床研究和动物实验报道,乌司他丁的应用在预防感染性休克、强化胰腺炎、缺血再灌注器官损伤和多器官功能障碍方面可发挥重要作用,这种保护与乌司他丁的抗炎作用有关[6]。乌司他丁对重症急性胰腺炎诱导的铁死亡引起的急性肾损伤的影响机制尚不清楚。因此,本研究评估乌司他丁对重症急性胰腺炎诱导的铁死亡引起的急性肾损伤的保护作用,探讨了乌司他丁抑制铁死亡诱导的过氧化脂积累的分子机制。
1 资料与方法
1.1动物:从郑州大学动物中心购买24只成熟的Wistar雄性大鼠(体重220~250g)。将大鼠饲养在受控的气候环境中,光照/黑暗循环为12h/12h,并被允许自由进食和饮水。所有实验均经郑州大学机构动物护理和使用委员会批准,符合美国国立卫生研究院实验动物使用标准。
1.2重症急性胰腺炎大鼠模型的建立及分组:大鼠经3%戊巴比妥钠(20mg/kg)腹腔麻醉后,将5%牛磺胆酸钠(1mL/kg)逐渐引入胆管,建立SAP大鼠模型[7]。对照组大鼠给予等量生理盐水,SAP诱导后6h,通过腹膜内注射乌司他丁,剂量分别为50000U/kg和100000U/kg。将24只Wistar雄性大鼠随机分为4组,每组6只:对照组(Control),重症急性胰腺炎组(SAP),重症急性胰腺炎组+低剂量乌司他丁组(SAP+UTI-L),重症急性胰腺炎组+高剂量乌司他丁组(SAP+UTI-H)。各组大鼠在建模成功后24h后再次麻醉,通过穿刺后腔收集血液样品,并通过离心分离血清并在-80℃下冷冻直至实验。使用多聚甲醛(4%)快速固定肾脏,将多余的组织储存在-80℃以进行进一步分析。
1.3苏木精和伊红(H&E)染色:将福尔马林固定的肾组织嵌入石蜡中并切成2μm厚的切片,这些切片用H&E溶液染色。使用光学显微镜在×400的原始放大倍率下捕获图像,包括上皮简化、刷缘缺失、根尖起泡、上皮细胞脱落、肾小管扩张和管型形成。以对损伤肾小管的百分比进行分级:所有正常小管为“0”;“1”表示<10%损伤小管;“2”表示10~25%损伤小管;“3”表示26~75%损伤小管;4%表示>75%损伤小管。
1.4肾功能评估:将血液样品在4℃下以3000rpm离心10min,收集血清并储存在-80℃。分别使用尿素氮检测试剂盒和血清肌酐检测试剂盒检测血液样品中尿素氮(BUN)和血清肌酐(SCr)含量。
1.5ELISA:使用酶联免疫吸附测定(ELISA)试剂盒测量肿瘤坏死因子-α(TNF-α)和白细胞介素-6(IL-6),超氧化物歧化酶(SOD),过氧化氢(H2O2)、丙二醛(MDA)、活性氧(ROS),谷胱甘肽过氧化酶4活性的水平。
1.6铁测量:肾脏组织用磷酸盐缓冲盐水(PBS)匀浆,离心后收集上清。根据说明书使用铁含量检测试剂盒测定铁水平。
1.7Western blot:从大鼠肾脏中提取总蛋白,并使用BCA蛋白测定试剂盒,使用8~12%十二烷基硫酸钠-聚丙烯酰胺凝胶电泳分离蛋白质(50μg),并转移到聚偏氟乙烯膜上。将膜与一抗(ACSL4,GPx4,FTH1和GAPDH)在4℃孵育过夜,然后在37℃下与HRP偶联的二抗孵育2h,使用增强型化学发光试剂观察蛋白质条带。使用Image J软件检查相对于GAPDH的蛋白质水平。
1.8qRT-PCR:使用TRIzol和RNeasy试剂盒和DNaseI消化分离总RNA。使用PrimeScriptTM RT试剂盒进行逆转录反应,并使用SYBR预混料Ex Taq Ⅱ试剂盒,使用补充表S2中列出的适当引物进行稀释的互补DNA(cDNA)进行qRT-PCR分析。对于microRNA,进行茎环逆转录反应,并将2-ΔΔCt采用该方法计算RNA基因与GAPDH和U6表达的相对丰度。见表1。

表1 引物序列表
2 结 果
2.1乌司他丁减轻SAP诱导的AKI中的肾功能不全和肾小管损伤:H&E染色结果显示,乌司他丁可以减轻SAP诱导后大鼠肾组织的病理损伤,如图1A所示,为评估肾小管的组织学变化,我们分析大鼠肾组织学染色的损伤评分。图1B损伤评分结果显示,与Control组相比,SAP组的肾组织损伤评分明显升高,且SCr和BUN水平显着增加,经乌司他丁治疗后,与SAP组相比,SAP+UTI-L(P<0.01)和SAP+UTI-H(P<0.01)组肾组织损伤评分显著降低,Cr(P<0.05)和BUN(P<0.01)水平有明显下降,且差异具有统计学意义。

图1 乌司他丁减轻SAP诱导的AKI大鼠肾脏的病理损伤和肾功能障碍
2.2乌司他丁降低SAP诱导的AKI大鼠血清中炎症反应:研究表明肾损伤常伴炎症反应激活,图2结果表明,与Control组相比,SAP组中TNF-α和IL-6水平显著增加(P<0.01),差异具有统计学意义。然而,乌司他丁的治疗有效地平衡了炎症反应,特别是在高剂量下。炎症因子TNF-α和IL-6表达水平显著降低。

图2 乌司他丁降低SAP诱导的AKI大鼠血清炎症反应
2.3乌司他丁降低SAP诱导的AKI大鼠血清中氧化应激:氧自由基可以攻击多不饱和脂肪酸,然后触发细胞内脂质过氧化,诱导细胞死亡和损伤。MDA的量可以反映细胞内脂质过氧化的程度,间接反映细胞损伤的程度。图3结果表明,与Control组相比,SAP组中MDA,H2O2和ROS的水平显著增加(P<0.01),SOD水平明显下降(P<0.01),差异具有统计学意义。乌司他丁的治疗后MDA,H2O2和ROS显著降低,而SOD水平增加。

图3 乌司他丁降低SAP诱导的AKI大鼠血清氧化应激
2.4乌司他丁对SAP诱导的AKI大鼠铁死亡的影响:铁在急性肾损伤和铁死亡的启动过程中起关键作用,因此,我们研究了铁水平的变化,图4A结果发现,与Control组相比,SAP组中肾铁浓度显著增加(P<0.01),GPX4活性显著降低(P<0.01),然而,乌司他丁治疗逆转了这种效果。铁稳态受到铁代谢相关蛋白质的严格调节,ACSL4、GPX4和FTH1被认为是关键的铁死亡调节蛋白,图4B为使用Western blot检测ACSL4、GPX4和FTH1蛋白的表达水平,结果表明,与Control相比,SAP组中GPX4和FTH1蛋白表达水平明显降低(P<0.01),ACSL4的蛋白表达水平明显升高(P<0.01),差异具有统计学意义,与SPA相比,SAP+UTI-L和SAP+UTI-L组中GPX4和FTH1蛋白表达水平明显升高,ACSL4的蛋白表达水平显著降低,且与乌司他丁的剂量浓度相关。ACSL4、GPX4和FTH1的mRNA水平变化与蛋白水平变化保持一致,如图4C-I所示。
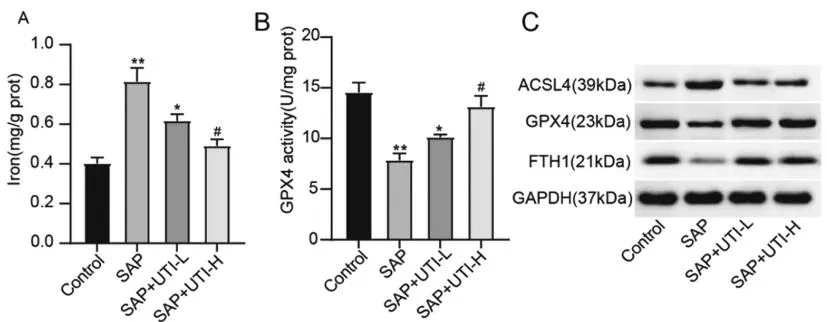
图4 乌司他丁抑制SAP诱导的AKI大鼠铁死亡
3 讨 论
SAP是一种特殊类型的胰腺炎,发病机制复杂,可导致胰腺肿胀、出血和坏死,促进大量炎性细胞因子的释放,引发免疫紊乱并诱发多种并发症,如不及时有效治疗,最终可导致多器官衰竭甚至死亡,因此,对于SAP的治疗,减少炎症,改善免疫系统和降低器官衰竭的发生率至关重要[8]。AKI是急性胰腺炎的常见并发症,通常在其他器官衰竭后发生,乌利那他汀是治疗急性胰腺炎的常用药物[9],因此,我们开展本研究,旨在探讨乌利那他汀治疗SAP诱导急性肾损伤的临床疗效,为今后的临床治疗提供可靠的理论依据。
除肾小管细胞死亡外,炎症也是AKI的重要特征,与肾功能不全的组织病理学相关。众所周知,垂死的细胞会释放炎症因子,从而放大组织损伤,细胞因子可能有助于AKI的发病机制。TNF-α直接作用于肾小球和肾小管毛细血管,导致缺血和肾小管坏死。它还刺激其他细胞因子的释放,例如IL-1β,IL-8和IL-6,它们作用于内皮细胞,导致肾缺血,血栓形成和氧自由基的释放,氧自由基可能与蛋白质和酶反应,导致细胞和细胞膜脂质过氧化,蛋白质变性和毛细血管通透性增加,缺血和直接肾细胞膜损伤[10]。铁死亡的迹象之一是膜氧化损伤,铁死亡与其他类型的调节性坏死一起被认为是免疫原性的,并且极易促炎,铁是不可或缺的成分,被肾小球过滤并在肾小管中重新吸收。全身和细胞铁代谢由铁的摄入、储存、利用和外排介导,并由多种蛋白质调节。铁稳态的畸变与肾脏疾病有关,在急性肾损伤的动物模型中,肾脏中催化铁的浓度显著增加,并与顺铂、缺血再灌注、氨基糖苷类、横纹肌溶解和血红蛋白尿等因素引起的广泛损伤相关[11]。在人类中,已经发现催化铁水平升高与急性肾损伤进展之间存在很强的关联。较高的催化铁血浆水平和较低浓度的铁调素都与急性肾损伤患者的死亡率增加有关,更重要的是,铁对于铁死亡的发生至关重要。本文研究表明,乌司他丁减少了通过SAP诱导的AKI大鼠铁积累。但是乌司他丁不能直接结合铁,因此它通过调节关键的铁代谢相关蛋白的表达来恢复肾铁稳态,如ACSL4、GPX4和FTH1。GPX4是一种抗氧化剂防御酶,可修复脂质的氧化损伤,作为铁死亡的中枢调节因子。根据我们的结果,乌司他丁减轻了铁死亡相关蛋白水平的下降,包括GPX4和SLC7A11。ACSL4和GPX4主要在肾小管中表达上皮细胞,我们推测铁死亡主要发生在肾小管上皮。这些发现表明铁死亡发生在大鼠肾损伤模型的研究是SAP诱导AKI的治疗靶点。
乌利那他汀是一种从新鲜尿液中提取的广谱蛋白酶抑制剂,在既往研究中已被证明可阻断炎性细胞因子与白细胞之间的相互作用,并能显著改善炎症反应[12]。在本研究中,发现TNF-α和IL-6的水平在大鼠SAP模型中明显增加,反映了炎症反应的程度。此外,ROS和H2O2的水平增加,表示氧化损伤的激活,而MDA水平的增加表明脂质过氧化的程度。这些氧化和炎症介质已被证明参与由各种致病引起的肾脏损伤,乌司他丁的应用有利于预防AKI。为了研究乌司他丁保护作用的可能机制,建立了大鼠SAP模型,发现乌司他丁通过抑制氧化应激和炎症反应来减少肾脏病理损伤。
总之,本研究发现乌司他丁通过抑制炎症过程和氧化应激,抑制铁死亡保护重症急性胰腺炎诱导的急性肾损伤。因此,乌利司他汀可能是重症急性胰腺炎诱导的急性肾损伤的有价值的临床候选药物。因此,在未来的研究中,应使用增加的样本量,以进一步了解乌司他丁的保护机制。

