大蒜辣素软膏的体外透皮吸收特性研究
刘 红, 宋百灵, 马雪红, 李新霞
(1新疆医科大学药学院, 乌鲁木齐 830017; 2伊犁州友谊医院药剂科, 新疆 伊宁 839300;3新疆胡蒜研究院(有限公司); 4新疆大蒜药用研究重点实验室, 乌鲁木齐 830013)
大蒜(AlliumsativumL.)为百合科(Liliaceae)葱属(Allium)植物的地下鳞茎,具有杀虫、解毒、消肿、止痢、消食等功效,主要用于腹泻、痢疾、鼻炎、银屑病等疾病的治疗[1-4]。大蒜辣素(Allicin)是从新鲜大蒜中分离得到的一种含硫化合物,具有多种药理活性,如抗炎、抗菌、抗病毒、抗氧化、调血脂、降压、降糖、抗肿瘤、免疫调节等[5-7]。大蒜辣素性质不稳定,易受多种因素影响,在一定程度上限制了其成药性[8]。皮肤给药的优点在于避免了消化道对大蒜辣素的代谢。本研究通过建立离体大鼠完整背部皮肤及去角质层皮肤透皮模型,采用超高效液相色谱-质谱-质谱串联法(UPLC-MS-MS)测定大蒜辣素软膏皮肤渗透特性,现报道如下。
1 仪器与试药
1.1 仪器ACQUITY UPLC型超高效液相色谱仪(美国Waters沃特世公司);ACQUITY® TQD型质谱仪(美国沃特世公司);Empower 3型液相工作站(美国沃特世公司);TP-6型智能透皮试验仪(天津市鑫州科技有限公司);AB135-S型分析天平(美国梅特勒公司);Milli-Q超纯水系统,Millipore超纯水机(德国默克公司);2-16K型低温离心机(德国赛多利斯公司)
1.2 试药蒜氨酸 (新疆胡蒜研究院(有限公司),批号AL080317);蒜酶(新疆胡蒜研究院(有限公司),批号20171001),羟苯乙酯(中国药品生物制品检定所,批号20180324),色谱甲醇(美国Sigma-Aldrich公司,批号180630),色谱乙腈(美国Sigma-Aldrich,批号180331),色谱无水甲酸(天津市福晨化学试剂厂,批号2019013),0.9%氯化钠注射液(西安京西双鹤药业有限公司,批号C20180912),大蒜辣素软膏(新疆胡蒜研究院(有限公司),批号20191015);空白软膏(新疆胡蒜研究院(有限公司),批号20191035)。
1.3 动物SD健康雄性大鼠50只,体重(200±20)g,SPF级,由新疆医科大学动物实验中心提供,实验动物质量合格证号:SCXK(新) 2018-0003。在新疆医科大学实验动物中心屏障实验室饲养,饲养环境温度(23±2)℃,相对湿度20%~45%。
2 方法与结果
2.1 溶液的配制
2.1.1 大蒜辣素对照溶液的配置 取蒜氨酸对照品溶液和蒜酶溶液混匀,室温反应后超滤离心,取上清液,即得浓度为0.107 4 mg/mL的大蒜辣素对照溶液。
2.1.2 羟苯乙酯对照品溶液的配置 取羟苯乙酯对照品适量,用50%甲醇溶解并稀释,摇匀即得浓度为0.200 7 mg/mL的羟苯乙酯对照品溶液。
2.2 色谱与质谱条件色谱条件:色谱柱为ACQUITY UPLC BEH C18 (2.1 mm×100 mm,1.7 μm),柱温30℃,进样量8 μL,流速0.25 mL/min,流动相A为0.1%甲酸,流动相B为甲醇,梯度洗脱,梯度洗脱程序见表1。质谱条件:电喷雾离子化(ESI),正离子,毛细管电压为3.00 KV,离子源温度为150℃,脱溶温度为350℃,氩气流速为150 L/h,氮气流速为900 L/h,扫描模式为MRM 模式(多反应离子扫描),定量离子选择见表2。
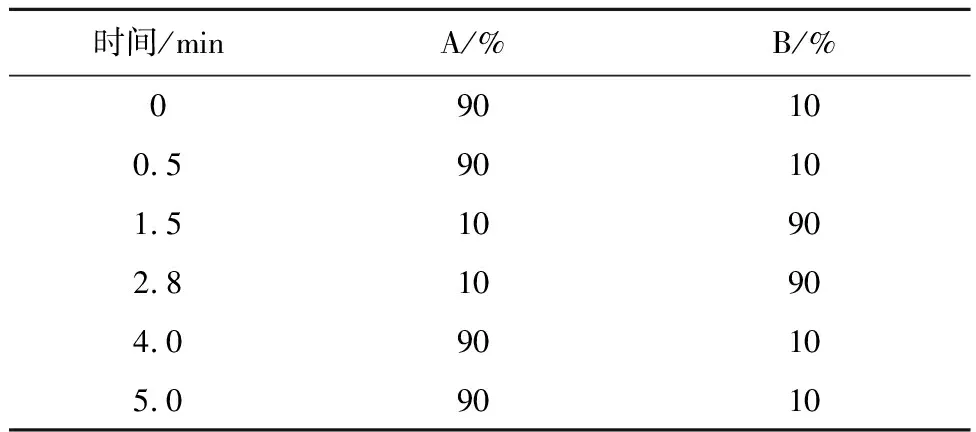
表1 梯度洗脱程序
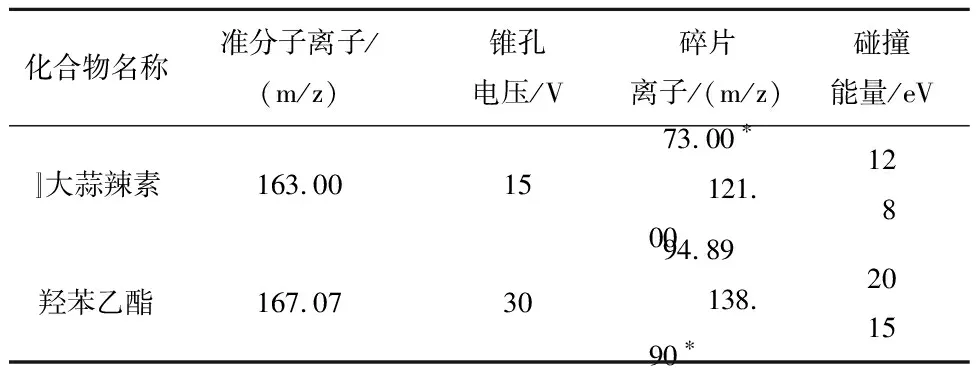
表2 大蒜辣素和羟苯乙酯一级、二级质谱电离碎片离子的分子量
2.3 UPLC-MS-MS方法学验证
2.3.1 对照溶液的制备 取适量“2.1.1”项下的大蒜辣素对照液和“2.1.2”项下羟苯乙酯对照品溶液,摇匀即得对照溶液。
2.3.2 空白基质软膏接收液的制备 取空白软膏适量,均匀涂布于固定在Franz扩散池的大鼠皮肤上,5 h后得空白基质软膏接收液。
2.3.3 样品溶液的制备 取大蒜辣素软膏适量,均匀涂布于固定在Franz扩散池的大鼠皮肤上,5 h后得样品溶液。
2.3.4 样品前处理 制备的溶液中加入乙腈500 μL,涡旋混匀2 min,再加入羟苯乙酯对照品溶液50 μL,12 000 r/min离心15 min,取上清液。
2.3.5 专属性实验 分别取“2.3.1”、“2.3.2”和“2.3.3”项下的液体经样品前处理按“2.2”项下色谱质谱条件进样,采用二级谱,分别对163.00→73.00及167.07→138.88定量离子对进行MRM扫描(图1)。结果表明,在该色谱质谱条件下空白基质软膏在两个通道163.00→73.00大蒜辣素主峰及167.07→138.88内标峰处不出峰,被测物的色谱峰形良好,基线平稳,无杂峰干扰,具有良好的专属性。

图1 专属性考察的MRM色谱图(注: 1.大蒜辣素 2.羟苯乙酯)
2.3.6 标准曲线的制作 取空白基质软膏接收液0.5 mL,分别加入不同浓度大蒜辣素溶液50 μL,得到浓度分别为:47.54、475.40、950.80、1 426.00、4 754.00 ng/mL的系列浓度溶液,经样品前处理后按“2.2”项下色谱质谱条件进样测定。以大蒜辣素溶液质量浓度为横坐标(X),大蒜辣素与羟苯乙酯峰面积比值为纵坐标(Y)进行线性回归,得回归方程:Y=0.005 2X-0.094 9,r=0.999 8,大蒜辣素在47.54 ~ 4 754.00 ng/mL浓度范围内线性关系良好。
2.3.7 定量限与检测限 取大蒜辣素对照品溶液适量,加入一定量的空白基质软膏接收液,经样品前处理后按“2.2”项下色谱质谱条件进样测定,以S/N≥10,测得大蒜辣素定量限为40.15 ng/mL;S/N≥3,测得大蒜辣素检测限为18.06 ng/mL。
2.3.8 精密度实验 取空白基质软膏接收液0.5 mL,分别加入不同浓度大蒜辣素溶液50 μL,得低、中、高浓度样品溶液(335.6、657.1、986.1 ng/mL),每种浓度平行制备4份,按“2.2”项色谱质谱条件进样测定,计算不同浓度的日内RSD值分别2.6%、1.1%、1.6%;每天测定1个分析批,连续测定5 d,计算不同浓度的日间RSD值分别4.1%、2.8%、2.9%,表明仪器的精密度良好。
2.3.9 重复性实验 取“2.3.4”项下样品溶液,按“2.2”项色谱质谱条件对每个浓度连续测定6次,计算不同浓度的重复性,RSD值分别2.3%、1.7%、0.99%,表明重复性良好。
2.3.10 样品稳定性实验 取“2.3.4”项下样品溶液,分别置于室温及0~4℃环境下,于0、2、4、6、8 h按“2.3.1”项下方法处理进样分析;0~4℃条件下RSD值分别为2.9%、1.5%、1.1%;室温条件下RSD值分别为8.6%、6.0%、4.9%,表明大蒜辣素样品溶液在0~4℃条件下较稳定,在室温下放置8 h后,大蒜辣素样品溶液RSD值未超过3.0%,表明在8 h内样品稳定性良好。
2.3.11 加样回收率实验 精密量取已知测定含量的样品9份,分为3组,每组3份,分别加入低、中、高浓度(630.6、432.0、215.7 ng/mL)的大蒜辣素溶液,经样品前处理后,按“2.2”项下色谱质谱条件进样,计算回收率。低、中、高3种浓度大蒜辣素的平均回收率分别为90.36%、94.03%、94.54%,RSD分别为1.7%、1.7%、1.4%。
2.4 体外透皮试验
2.4.1 离体皮肤的制备 (1)完整皮肤的制备:大鼠腹腔注射10%水合氯醛2 mL致死,剔除背部皮肤的鼠毛,剪净绒毛,剪下大鼠背部皮肤,剥离皮下粘连和脂肪组织,用生理盐水反复冲洗,剪成适当大小,置于加生理盐水的密封袋中,-20℃保存,7 d内使用。(2)去角质层皮肤的制备:同法处理皮肤,再用胶带条将表皮的角质层粘去,得到去角质层的大鼠背部皮肤。
2.4.2 供试品溶液的检测 取处理好的离体皮肤,自然解冻,用生理盐水清洗干净,用滤纸吸干表面水分。将皮肤(完整皮肤、去角质层皮肤)固定于Franz扩散池中。在接收池中加入接收液溶液(生理盐水)16 mL,池内温度为 37℃,300 r/min恒温磁力搅拌,平衡30 min,使皮肤与液面紧密接触。取大蒜辣素软膏,精密称定,均匀涂抹在皮肤表面,分别于0.5、 1、 2、 3、 4、 5 h取出0.5 mL接收液,同时向接收池中补加等体积同温度的生理盐水,取出的接收液经样品前处理后按照“2.2”项下色谱质谱条件进样分析,计算单位面积累积透皮量(Q)。

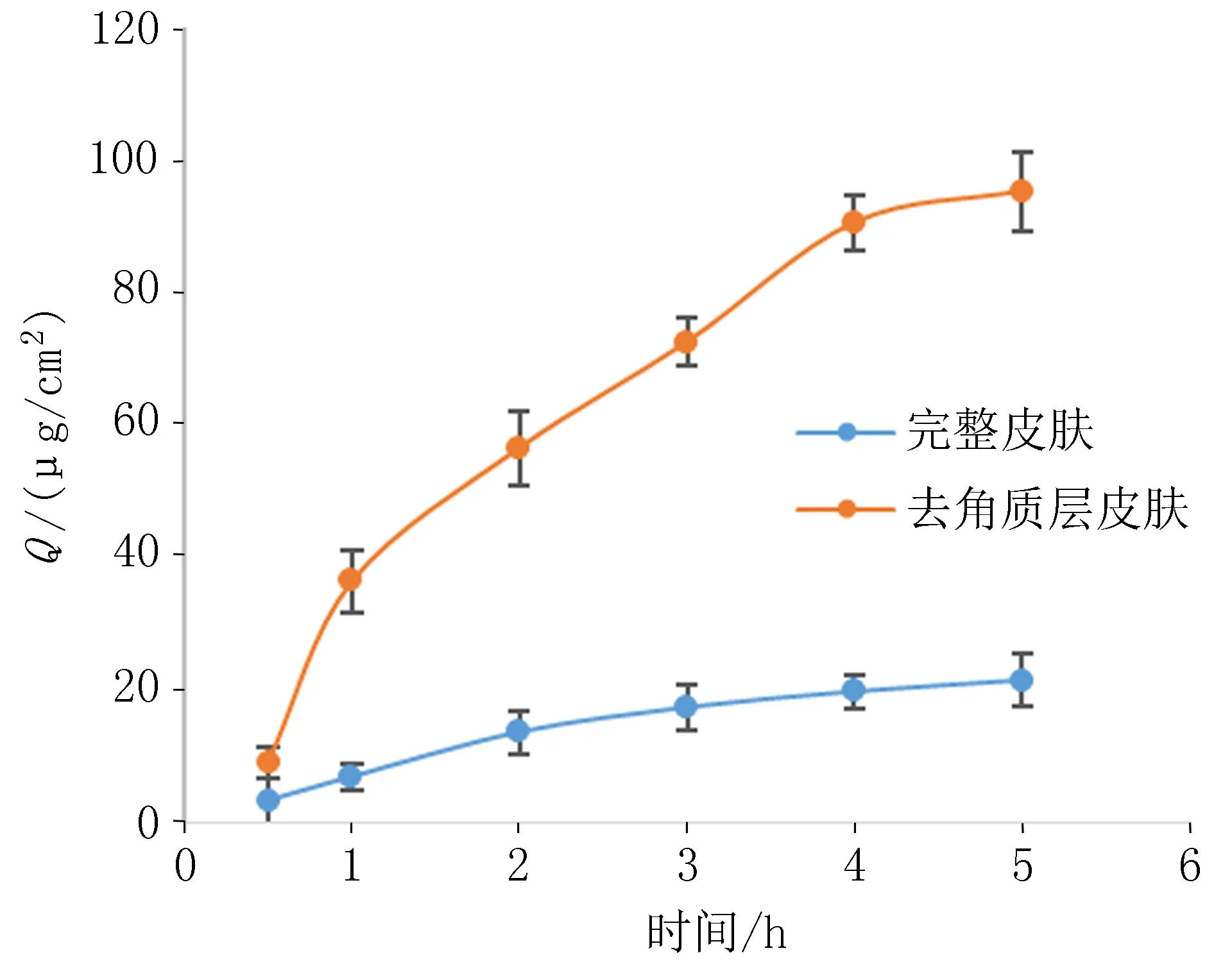
图2 大蒜辣素软膏的透皮曲线
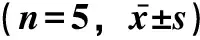
表3 体外释药模型拟合结果
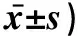
表4 完整皮肤和去角质层皮肤的体外透皮特性(n=5,
3 讨论
外用制剂具有不受肝脏首过效应和肠胃道破坏影响、可直达病灶部位的独特优点,药物透皮吸收效果直接决定药效[9]。皮肤是药物吸收的主要屏障,药物需透过皮肤屏障到达靶组织发挥药效。皮肤表面的角质层是亲脂性很强的生物膜,药物的理化性质对经皮吸收能力至关重要。理想的经皮吸收候选药物要求分子量<600,熔点<200℃,油水分配系数logP在1~3之间[10]。大蒜辣素纯品为无色油状液体,分子量为162.3,油水分配系数logP为1.09,是较理想的候选药物[11]。
通过对大蒜辣素软膏在大鼠完整皮肤与去角质层皮肤的透皮特性研究表明,大蒜辣素软膏具有良好的透皮性能,两种皮肤性质的透皮吸收规律相似,累计释药量与时间线性关系良好,均符合 Higuchi方程,大蒜辣素软膏在皮肤的吸收机制主要为被动扩散。去角质层皮肤的J远高于完整皮肤,是完整皮肤的4.74倍,说明药物经皮吸收速率被皮肤的屏障作用所限制,角质层是影响大蒜辣素透过皮肤的重要因素。本实验结果表明软膏的有效成分大蒜辣素以原型形式透过皮肤,发挥药效作用。课题组对大蒜辣素改善银屑病样皮损的研究已取得良好实验结果[4],而银屑病、湿疹、特异性皮炎和溃疡等本身具有皮肤屏障功能损伤,当使用药物时可能会增加皮肤的吸收能力[12]。
本研究建立 UPLC-MS-MS测定透皮吸收液中大蒜辣素的分析方法,采用多反应离子监测(MRM)模式,经过母离子和子离子的双重筛选,降低了基质干扰。方法专属性强,灵敏度高,与课题组前期建立的大蒜辣素含量测定方法相比[13],检出限提高100倍,为后续生物样品中大蒜辣素定量分析提供了参考方法。

