吉西他滨联合顺铂方案治疗复发性三阴性乳腺癌的疗效观察
申鹏,刘正义,闫园,于博凡,于洋
河南省人民医院乳腺外科,郑州 450000
三阴性乳腺癌(triple-negative breast cancer,TNBC)是指雌激素受体、孕激素受体以及人表皮生长因子受体2 均阴性的特殊类型乳腺癌[1],其发病率约占乳腺癌的15%~20%。TNBC 患者对靶向药物不敏感,临床治疗难度大[2]。蒽环、紫杉类药物是目前临床治疗TNBC 的一线化疗方案,多数患者可从中获益,但仍有部分患者治疗后易复发。复发性TNBC 患者可能出现耐药,且预后较差,因此延长生存时间、提高生存质量是此类患者的主要治疗目标[3]。吉西他滨联合卡培他滨方案是目前临床较常用的复发性TNBC 化疗方案,但整体治疗效果并不理想。吉西他滨、顺铂的抗肿瘤机制与紫杉类药物不同,不会产生交叉耐药性,对紫杉类药物耐药者较为适宜。吉西他滨为一种新型的胞嘧啶核苷衍生物,顺铂为一种重金属铂类络合物,均具有抗肿瘤范围广、作用力强等优点[4],两药联用可产生协同增效的作用。研究发现[5],吉西他滨联合顺铂治疗耐药性晚期乳腺癌患者的临床疗效确切,且安全性高。但其应用于复发性TNBC 患者的研究报道较少。基于此,本研究旨在探讨吉西他滨联合顺铂方案在蒽环、紫杉类药物治疗后复发性TNBC 患者中的应用效果,以期为临床治疗复发性TNBC 患者提供参考。现报道如下。
1 资料与方法
1.1 一般资料
选取2019 年1 月~2021 年1 月期间某院收治的81 例蒽环、紫杉类药物治疗后复发性TNBC 患者作为研究对象,采用随机、单盲试验研究方法,依据随机数字表法分为A 组(n=40)和B 组(n=41)。A 组:年龄39~58 岁,平均年龄(48.26±8.79)岁;病程18~30 个月,平均病程(23.46±5.16)个月;体重指数(body mass index,BMI)20.12~26.11kg/m2,平均BMI(23.16±2.36)kg/m2。B 组:年龄39~60 岁,平均年龄(49.11±9.13)岁;病程17~31 个月,平均病程(24.65±6.12)个月;BMI 19.44~27.13kg/m2,平均BMI(23.15±3.41)kg/m2。两组患者一般资料比较无统计学差异(P>0.05),具有可比性。本研究经医院伦理委员会审批通过,所有患者及家属均签署知情同意书。
纳入标准:①符合《中国晚期乳腺癌临床诊疗专家共识》(2018 版)[6]中乳腺癌相关诊断标准,且均接受穿刺检查明确为TNBC 者。②均为首次复发者。③复发后均未进行放化疗治疗者。④具有可测量及能够明确诊断的病灶者。⑤预期生存期为3 个月及以上者。
排除标准:①患有认知障碍,不能明确表述自身意愿者。②合并其他重要脏器严重病变者。③合并其他恶性肿瘤者。④患者未完成全部治疗,中途退出者。
1.2 治疗方法
A 组患者给予注射用盐酸吉西他滨[浙江海正药业股份有限公司,国药准字H20093418,规格1.0g(按C9H11F2N3O4计)]联合卡培他滨片(江苏恒瑞医药股份有限公司,国药准字H20133365,规格0.5g):将注射用盐酸吉西他滨1000mg/m2加至150ml 氯化钠注射液(辰欣药业股份有限公司,国药准字H20056758,规格50ml∶0.45g)中,静脉滴注,d1、8。口服卡培他滨片250mg/m2,d1~14。B 组患者给予注射用盐酸吉西他滨联合注射用顺铂(齐鲁制药有限公司,国药准字H37021356,规格30mg)方案进行治疗,注射用盐酸吉西他滨用法用量与A 组相同。将注射用顺铂75mg/m2加至200ml 氯化钠注射液中静脉滴注,d1~3。21 天为1 个疗程。根据患者的化疗情况,治疗3~6 个疗程,化疗前给予水化、止吐、抗过敏等处理。在治疗3 个疗程后评估患者的临床疗效。
1.3 观察指标
(1)临床疗效。根据《实体瘤治疗疗效评价标准:RECIST》[7]评估患者的临床疗效:分别于治疗前后评估患者病灶等级,并将其划为Ⅰ型、Ⅱ型、Ⅲ型,分别表示渐增型、平台型、流出型,若存在多种类型则归为混合型,根据其上升、下降趋势评价患者的治疗效果。①完全缓解:患者原发病灶完全消失,持续时间在1 年以上,且患者病灶等级明显降低。②部分缓解:患者病灶等级有所降低,且最大病灶直径降低30%及以上。③治疗无效:出现新病灶或患者最大病灶直径降低不足30%,或患者的最大病灶直径扩大5mm。治疗有效率(%)=(完全缓解+部分缓解)例数/每组总例数×100%。
(2)肿瘤标志物。分别于治疗前后采集患者清晨空腹外周静脉血3ml,4℃静置30min,采用Microfuge 16 台式微量离心机(美国贝克曼库尔特公司,r=12.5cm),以3000r/min(4 ℃)离心10min 后,取血清。采用电化学发光法检测患者血清癌胚抗原(carcinoembryonic antigen,CEA)、糖类抗原153(carbohydrate antigen 153,CA153)、糖类抗原125(carbohydrate antigen 125,CA125),试剂盒购自罗氏诊断产品(上海)有限公司。
(3)欧洲癌症研究与治疗组织生命质量量表(European Organization for Research and Treatment of Cancer Quality of Life Questionnaire Core 30,EORTC QLQ-C30)。分别于治疗前后通过EORTC QLQ-C30 评分评价患者的生活质量,对患者疲劳、恶心呕吐、失眠、食欲丧失、便秘症状及总体健康进行评分,总体健康总得分越高,表示患者的生活质量越高;症状总得分越高,表示患者的生活质量越低[8]。
(4)不良反应发生情况及预后。观察并记录两组患者治疗期间不良反应的发生情况:肝功能不全(典型症状表现为食欲减退、恶心、乏力、黄疸、皮肤瘙痒、下肢水肿或腹水、腹泻、腹胀、血液凝固障碍、出血、肝掌和蜘蛛痣等)、恶心、胃肠道反应(腹痛、消化不良、胀气、饱胀感或不适等症状)、腹泻(排便次数明显增多、粪便稀薄或呈水样,并伴有腹部不适)、脱发(头发数量明显减少或掉发)。此外,以门诊复查的方式对患者随访2 年,并记录患者在2 年内的复发情况(随访期内出现新病灶或疾病复发)、无进展生存期、稳定病例(随访期内保持疾病稳定状态患者)情况。
1.4 统计学方法
应用SPSS 23.0 软件进行数据的处理分析。计数资料以n(%)表示,采用χ2检验;计量资料以±s表示,采用t检验。P<0.05 为具有统计学差异。
2 结果
2.1 基线资料
两组患者基线资料比较无统计学差异(P>0.05),具有可比性(表1)。
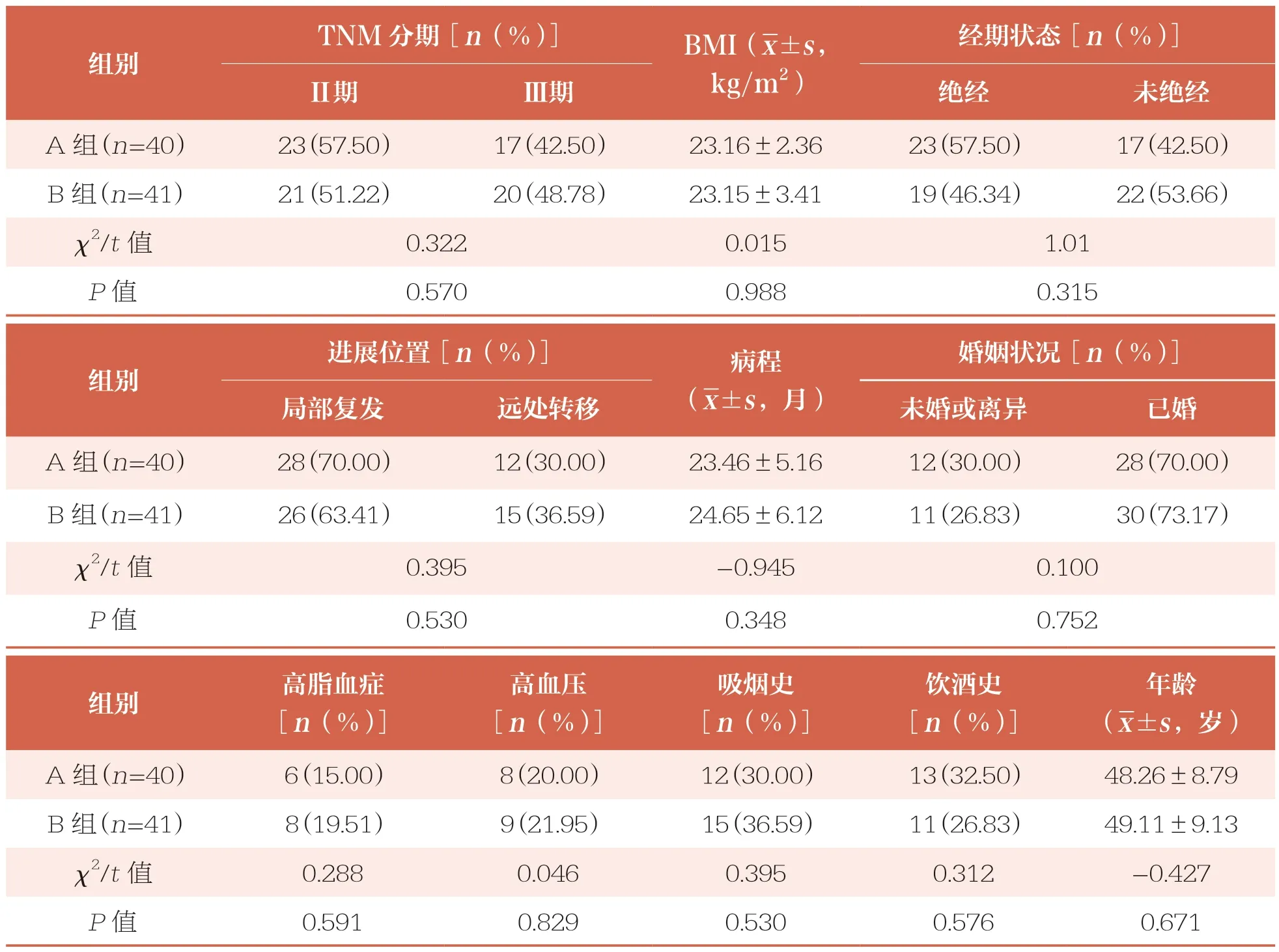
表1 两组基线资料比较
2.2 临床疗效
B 组治疗总有效率(82.93%)高于A 组(60.00%,P<0.05)(表2)。
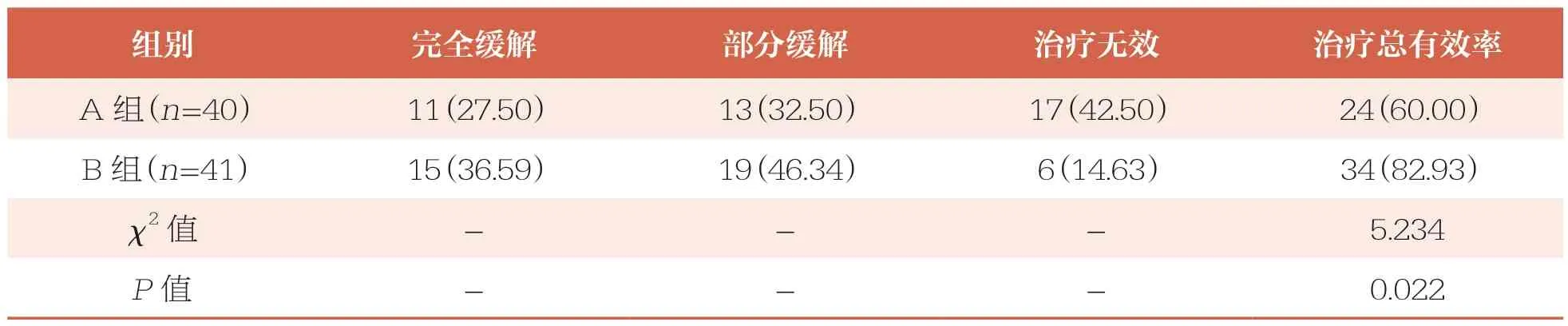
表2 两组临床疗效比较 n(%)
2.3 肿瘤标志物水平
治疗前,两组患者血清各项肿瘤标志物水平比较均无统计学差异(P>0.05)。治疗后,两组血清CEA、CA153、CA125 水平均降低(P<0.05),且B 组低于A 组(P<0.05)(表3)。
表3 两组肿瘤标志物水平比较 ±s
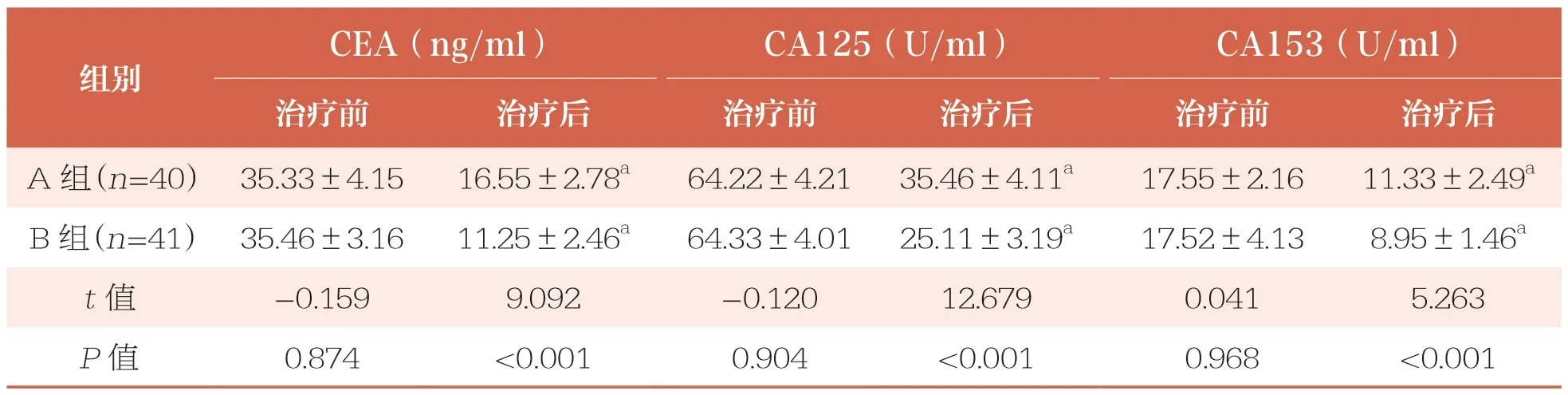
表3 两组肿瘤标志物水平比较 ±s
CEA:癌胚抗原;CA125:糖类抗原125;CA153:糖类抗原153;与同组治疗前比较:a:P<0.05。下同
CEA (ng/ml)CA125(U/ml)CA153(U/ml)治疗前治疗后治疗前治疗后治疗前治疗后A 组(n=40) 35.33±4.1516.55±2.78a64.22±4.2135.46±4.11a17.55±2.1611.33±2.49a B 组(n=41) 35.46±3.1611.25±2.46a64.33±4.0125.11±3.19a17.52±4.138.95±1.46a t 值-0.159 9.092 -0.120 12.679 0.041 5.263 P 值0.874 <0.0010.904 <0.0010.968 <0.001组别
2.4 EORTC QLQ-C30 评分
治疗前,两组EORTC QLQ-C30 评分比较无统计学差异(P>0.05)。治疗后,两组EORTC QLQ-C30 评分在疲劳、失眠方面均降低(P<0.05),且B 组低于A 组(P<0.05);两组EORTC QLQ-C30评分在总体健康方面均升高(P<0.05),且B 组高于A 组(P<0.05);两组EORTC QLQ-C30 评分在恶心呕吐、食欲丧失、便秘方面比较无统计学差异(P>0.05)(表4)。
表4 两组EORTC QLQ-C30 评分比较 ±s,分
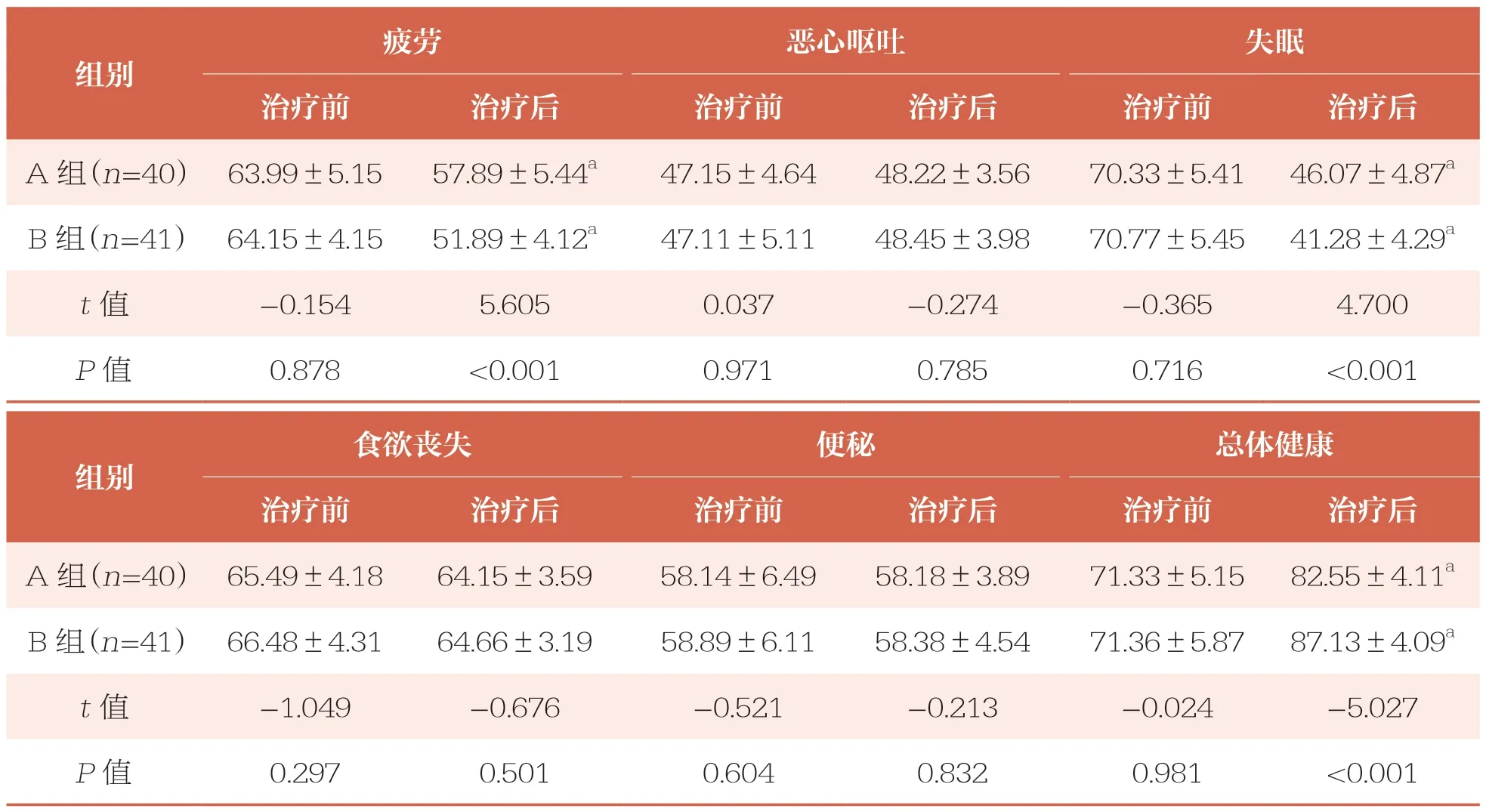
表4 两组EORTC QLQ-C30 评分比较 ±s,分
EORTC QLQ-C30:欧洲癌症研究与治疗组织生命质量量表
疲劳恶心呕吐失眠治疗前治疗后治疗前治疗后治疗前治疗后A 组(n=40) 63.99±5.1557.89±5.44a47.15±4.6448.22±3.5670.33±5.41 46.07±4.87a B 组(n=41) 64.15±4.1551.89±4.12a47.11±5.1148.45±3.9870.77±5.4541.28±4.29a t 值-0.154 5.605 0.037 -0.274 -0.365 4.700 P 值0.878 <0.0010.971 0.785 0.716 <0.001组别食欲丧失便秘总体健康治疗前治疗后治疗前治疗后治疗前治疗后A 组(n=40) 65.49±4.1864.15±3.59 58.14±6.4958.18±3.8971.33±5.1582.55±4.11a B 组(n=41) 66.48±4.3164.66±3.1958.89±6.1158.38±4.5471.36±5.8787.13±4.09a t 值-1.049 -0.676 -0.521 -0.213 -0.024 -5.027 P 值0.297 0.501 0.604 0.832 0.981 <0.001组别
2.5 不良反应及预后情况
两组患者治疗期间不良反应的总发生率比较无统计学差异(P>0.05)。B 组患者2 年内的复发率(14.63%) 低于A 组(40.00%,P<0.05), 中位无进展生存期[(6.65±1.45)个月]长于A 组[(4.26±1.23)个月,P<0.05],稳定病例数(58.54%)高于A 组(30.00%,P<0.05)(表5)。
表5 两组不良反应及预后比较 ±s,n(%)

表5 两组不良反应及预后比较 ±s,n(%)
组别肝功能不全胃肠道反应恶心腹泻骨髓抑制脱发合计A 组(n=40)1(2.50)2(5.00)3(7.50)1(2.50)1(2.50)8(20.00)B 组(n=41)2(4.88)1(2.44)4(9.76)2(4.88)3(7.32)12(29.27)χ2 值-----0.935 P 值-----0.333组别中位无进展生存期(月)稳定病例数(例)复发率A 组(n=40)4.26±1.2312(30.00)16(40.00)B 组(n=41)6.65±1.4524(58.54)6(14.63)t/χ2 值-7.9906.678 6.585 P 值0.0000.010 0.010
3 讨论
乳腺癌是临床常见的引起女性死亡的恶性肿瘤之一。流行病学调查发现,我国女性乳腺癌的发病率约为41.82/10 万[9]。TNBC 患者对于内分泌治疗、靶向治疗的反应性均较差,更易在早期出现复发、转移,且患者预后较差[10]。目前,化疗是临床治疗TNBC 的主要治疗手段,蒽环、紫杉类药物是TNBC 患者的首选化疗方案。蒽环类药物可嵌入肿瘤细胞的DNA 双链碱基,影响其DNA 复制。紫杉类药物为红豆杉属植物紫杉的次生代谢产物,可通过促进微管的正常循环而干扰肿瘤细胞分裂。但仍有约40%的TNBC 患者在经蒽环、紫杉类药物化疗后出现耐药、复发,因此需要选择其他化疗药物进行治疗[11-12]。
吉西他滨是一种细胞周期特异性抗代谢类药物,可作用于DNA 合成期的肿瘤细胞,阻止G1 期向S 期进展,目前在非小细胞肺癌、乳腺癌等疾病的化疗中应用较多[13]。吉西他滨联合卡培他滨是临床治疗复发性TNBC 患者的常用方案,但其整体疗效欠佳。顺铂是第一代铂的金属络合物,可与肿瘤细胞DNA 形成链间及链内交链,干扰肿瘤细胞增殖,对乳腺癌、肺癌等均具有较好的临床疗效[14]。吕建男等[15]研究发现,吉西他滨联合顺铂方案对蒽环、紫杉类药物耐药复发性TNBC 患者的临床疗效与长春瑞滨联合顺铂方案相仿,但吉西他滨联合顺铂方案的不良反应较少,更有利于延长患者无进展生存期。
本研究发现,B 组治疗总有效率(82.93%)高于A 组(60.00%,P<0.05);B 组患者2 年内的复发率(14.63%)低于A 组(40.00%,P<0.05),中位无进展生存期[(6.65±1.45)个月]长于A 组[(4.26±1.23)个月,P<0.05],稳定病例数(58.54%)高于A 组(30.00%,P<0.05)。以上结果提示,与吉西他滨联合卡培他滨相比,吉西他滨联合顺铂方案对蒽环、紫杉类药物治疗后复发性TNBC 患者具有更好的治疗效果。吉西他滨可迅速吸收,在体内经脱氧胞嘧啶激酶活化,由胞嘧啶核苷脱氨酶代谢转化成活性成分氟尿嘧啶,通过抑制肿瘤细胞DNA合成和核糖核苷酸还原酶活性,促进肿瘤细胞凋亡,抑制转移[16]。顺铂是以二价铂为中心同两个氯原子和两个氨分子结合的重金属络合物,可抑制DNA复制,且与多种抗肿瘤药物联用不易产生交叉耐药性[17],提示吉西他滨联合顺铂方案可有效抑制肿瘤细胞增殖,并防止其复发。
肿瘤标志物是特征性存在于肿瘤细胞,或因肿瘤而产生的物质[18]。CEA 是一种广谱肿瘤标志物,既往应用于结直肠癌的诊断,近年来发现其在消化道肿瘤、乳腺癌、卵巢癌、甲状腺癌患者中表达水平也会升高[19]。CA153、CA125 均为糖类抗原,在乳腺癌、肺癌、卵巢癌、子宫癌、结肠癌等患者体内高表达[20]。本研究发现,经治疗后,两组血清CEA、CA153、CA125 水平均降低(P<0.05),且B 组低于A 组(P<0.05),提示与吉西他滨联合卡培他滨相比,吉西他滨联合顺铂方案可有效降低患者血清肿瘤标志物水平,抑制肿瘤细胞的复制活性。
对于蒽环、紫杉类药物治疗后复发性TNBC 患者而言,改善其生存质量是目前临床治疗的重要目标之一。而化疗不良反应、肿瘤恶液质、精神心理状态不佳等均可降低患者的生存质量[21]。EORTC QLQ-C30 是临床用于评价恶性肿瘤患者生存质量的常用工具,具有良好的信度和效度。本研究发现,治疗后,两组EORTC QLQ-C30 评分在疲劳、失眠方面均降低(P<0.05),且B 组低于A 组(P<0.05);两组EORTC QLQ-C30 评分在总体健康方面均升高(P<0.05),且B 组高于A 组(P<0.05),提示与吉西他滨联合卡培他滨相比,吉西他滨联合顺铂方案可有效改善患者的生存质量,这可能与其更强的抗肿瘤效果有关。此外,两组患者治疗期间不良反应总发生率比较无统计学差异(P>0.05),这与临床报道中吉西他滨联合顺铂方案的不良反应低于吉西他滨联合卡培他滨方案的结论并不一致[22]。这可能与本研究纳入样本量较少,对结果产生一定的偏倚有关。今后将进行大样本量的研究,进一步探讨2 种治疗方案在不良反应方面的优劣性。
综上所述,与吉西他滨联合卡培他滨相比,吉西他滨联合顺铂方案在蒽环、紫杉类药物治疗后复发性TNBC 患者中治疗效果更佳,可有效降低患者血清肿瘤标志物水平,提高生活质量,改善预后,但仍需进一步研究证实。

