碳气凝胶修饰纳米α-Fe2O3的可控制备及表征
陈进洪,罗大为,郑友坤,陈锐志,周坤扬
(深圳职业技术学院 应用化学与生物技术学院,广东 深圳 518055)
碳气凝胶修饰纳米α-Fe2O3的可控制备及表征
陈进洪,罗大为*,郑友坤,陈锐志,周坤扬
(深圳职业技术学院 应用化学与生物技术学院,广东 深圳 518055)
通过水热反应和碳气凝胶(CA)修饰的方法制备了 α-Fe2O3@CA复合材料,探讨了水热合成温度、时间和添加活性剂对合成复合材料的影响,采用XRD、SEM和TGA等方法对材料的结构、形貌和α-Fe2O3负载数量进行了表征.研究结果表明,采用水热合成法可以在碳气凝胶表面修饰空心球状和橄榄球状α-Fe2O3,且负载α-Fe2O3的数量与水热时间有关.200℃下水热合成24 h时,α-Fe2O3在复合材料中负载高达96.53%.
α-Fe2O3;碳气凝胶;制备;形貌
α-Fe2O3(赤铁矿)是一种非常重要的过渡金属氧化物,因其具有无毒、耐光、耐热、耐磨及化学稳定性好等特点[1-3],且兼具原料丰富、价格便宜及环境友好等优点,在光、电、磁等许多方面都具有完全不同于体相材料的独特特性,广泛应用于涂料、吸附、催化、气敏材料、电化学、生物医学工程等领域,特别是在锂电池负极材料方面具有广泛的应用前景[4-5].近年来,关于不同结构 α-Fe2O3合成与性能研究较多,如催化高氯酸铵热分解研究[6],如各种形态α-Fe2O3作为锂离子电池电极材料提高电化学性能的研究[7].但在这些领域使用过程中,α-Fe2O3的缺点是导电性不好且纳米 α-Fe2O3颗粒太细易团聚,从而影响α-Fe2O3的使用效果,因而采用各种碳材料(包括碳纳米管以及石墨烯等[8-9])对其进行修饰成为近年来研究的热点.
碳气凝胶(carbon aerogel,CA)是一种超轻且拥有连续的三维多孔网络结构的纳米级碳材料,具有导电性好、比表面积大及密度变化范围广等特点[10-11].众所周知,纳米材料的化学性能不仅与材料尺寸有关,更取决于其形貌和结构.本文以FeCl3·6H2O为铁源,采用水热合成法,在碳气凝胶表面合成不同结构、形貌和尺寸的纳米α-Fe2O3粉末,以期达到制备形貌可控且尺寸均一的复合材料,通过 XRD、SEM 手段对不同形貌产物及组成的纳米结构单元进行表征,通过热重测试手段研究氧化铁在复合材料中的负载数量.
1 实验部分
1.1 材料的制备
在对α-Fe2O3进行修饰前,首先采用超临界干燥的方法制备碳气凝胶[11-12],并对碳气凝胶进行活化,然后采用水热合成法在碳气凝胶上负载α-Fe2O3.具体方法:称取1.08 g FeCl3.6H2O、0.02 g NH4H2PO4和一定数量的碳气凝胶溶解于100 ml去离子水中,加入0.1 g聚乙烯吡咯烷酮(PVP)作为表面活性剂,超声波震荡 30 min,磁力搅拌30 min,转移到聚四氟乙烯内衬中,在一定温度下保温不同时间,冷却到室温.再用去离子水洗涤 3次以上,放入 80℃真空干燥箱中保温 8h,烘干收藏.为了研究水热合成温度、时间以及添加表面活性剂对复合材料结构的影响,具体实验条件见表 1,得到的样品分别标记为 α-Fe2O3@CA-x,x表示序号.不加入碳气凝胶,合成单一的纳米α-Fe2O3粉末.

表1 在不同条件下制备α-Fe2O3@CA复合材料
1.2 材料表征与电化学性能测试
对制备的碳气凝胶和 α-Fe2O3@CA复合材料分别进行物相分析(XRD,日本理学公司D/Max2550型X射线衍射仪)和微观形貌观察(SEM,日本日立公司 SU-70型扫描电子显微镜).在空气气氛条件下,使用Q50型热重分析仪(TGA)测定 α-Fe2O3的含量,升温速率为10 ·min℃-1,温度截止于600℃.
2 结果与讨论
2.1 物相分析
图 1是在碳气凝胶和不同条件下得到α-Fe2O3@CA复合材料的XRD图谱,从图1可以看出碳气凝胶在 2θ为 24°和 43°附近存在2个宽峰,但没有发现石墨晶体尖锐的 d002和d100特征衍射峰,呈现明显“馒头峰”特点,表明所制备的碳气凝胶是一种非晶态物质.对比分析不同条件下α-Fe2O3@CA复合材料XRD图谱,所有图谱的主要衍射峰类似,样品分别在2θ=24°、33°、35°、40°、49°、54°、62°和 64°等8个位置的衍射峰与赤铁矿α-Fe2O3的标准图谱(JCPDS Card No. 33-0664)完全吻合,表明该复合材料的主晶相是 α-Fe2O3.复合材料中碳气凝胶的衍射峰表现很弱,也表明了碳气凝胶的引入并未对 α-Fe2O3的晶体结构产生太大影响.
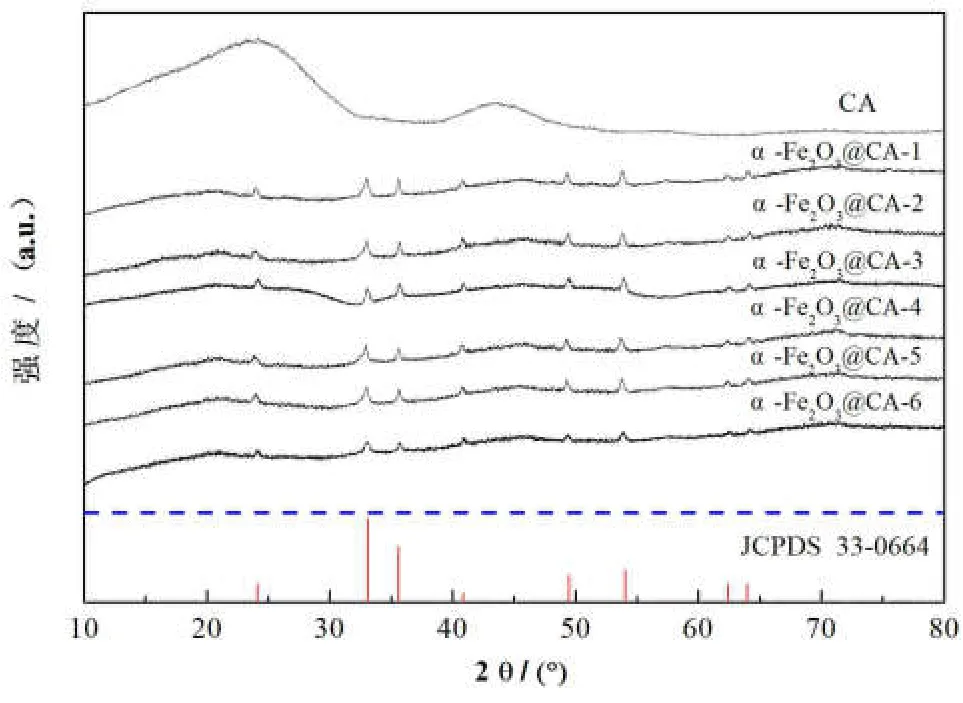
图1 碳气凝胶及不同条件下合成α-Fe2O3@CA复合材料的XRD图谱
根据XRD分析结果,可以推测α-Fe2O3在气凝胶表面的合成过程.首先在NH4H2PO4的作用下,FeCl3·6H2O发生水解反应(式1),得到中间产物Fe(OH)3,随后在水热合成中Fe(OH)3发生分解生成α-Fe2O3(式2):

2.2 微观形貌分析
图2是碳气凝胶及α-Fe2O3@CA-x复合材料的微观形貌,从图2(a)可以看出,所制备碳气凝胶由直径约100 nm的球状颗粒堆积成发达的网络结构,网络孔洞相对比较独立,呈现典型的无序多孔网络结构[13].从图2(b)可见,未使用PVP活性剂时,α-Fe2O3@CA复合材料与碳气凝胶外观区别不大,仍然可以清晰看到碳气凝胶基体的网络结构,从图2(b)左下方高倍形貌图可以发现在气凝胶表面依稀可见到棒状颗粒物,通过其他复合材料形貌(图2(c)至图2(g))对比并结合前面XRD 分析的结果,颗粒物应该是α-Fe2O3,结果表明,当未使用PVP活性剂时,α-Fe2O3负载在碳气凝胶表面的数量非常有限.PVP是一种两性表面活性剂,一端带有羰基,另一端为碳链.在合成过程中,PVP 带有羰基的一端可以与氧化铁表面的羟基形成氢键而结合,另一端的碳链与碳气凝胶在水溶液体系中由于缔合作用而有相互吸引的趋势,因而当未加入PVP时,α-Fe2O3与碳气凝胶结合较差,很难有效负载碳气凝胶表面.

图2 碳气凝胶(a)、复合材料α-Fe2O3@CA-1(b)、α-Fe2O3@CA-2(c)、α-Fe2O3@CA-3(d)、α-Fe2O3@CA-4(e)、α-Fe2O3@CA-5(f)和α-Fe2O3@CA-6(g)的SEM形貌
图2 (c)和图2(d)分别给出了水热合成温度分别为180℃和200℃下复合材料的外观形貌,相同之处在于在碳气凝胶表面均均匀覆盖一层颗粒状物质,结合 XRD分析结果,这些颗粒状物质应该是α-Fe2O3.对比发现,水热合成温度不同时,在碳气凝胶表面负载 α-Fe2O3结构不同,当水热合成温度为180℃时,通过图2(c)左下方高倍形貌清晰可见 α-Fe2O3为空心球状结构;当水热温度上升到200℃时,负载的α-Fe2O3转化为橄榄球状结构.根据式(2)可知,在水热合成过程中,Fe(OH)3脱水反应生成α-Fe2O3和水,由于发生脱水反应,前驱体结构中必然产生孔洞,因而表现出图 2(c)所示孔状结构.由于水热反应在填充度一定的条件下,随着水热反应温度的升高,反应釜内的压强增大.当温度升高后,孔洞将破裂,容易沿单一方向生长得到一维结构[14],因而得到图2(d)所示橄榄球状结构.
图 2(e)、2(d)、2(f)、2(g)是 α-Fe2O3@CA复合材料在200℃温度下合成21 h、24 h、27 h和30 h的SEM形貌,直径和长度均匀且分散性良好,完全没有明显的团聚迹象,且可以看出随着水热时间的延长,橄榄状 α-Fe2O3明显长大,当水热时间达到30 h时,橄榄状α-Fe2O3直径约200 nm,平均长度约1 μm.
2.3 热重分析
为确定 α-Fe2O3在复合材料中的含量,对在200℃水热合成不同时间的复合材料进行热重分析,结果如图3所示.由热重曲线可知,热失重主要存在2个部分,从室温到200℃的质量损失是由于物理吸附和化学吸附水的挥发,从 200℃开始,质量下降速度很快,500℃后复合材料质量几乎不再变化,分析认为这部分的质量损失主要源于碳气凝胶的燃烧,从图3可知,水热合成21 h,24 h,27 h及30 h的α-Fe2O3@CA复合材料中碳气凝胶质量损失分别为4.28%,3.47%,8.62%和10.26%,因此复合材料中α-Fe2O3含量依次为95.72%,96.53%,91.38%和 89.74%.结果表明随着水热合成时间的延长,在碳气凝胶表面富集α-Fe2O3数量并未表现出线性逐渐增加的趋势,分析认为这主要是因为随着水热合成时间的增加,α-Fe2O3颗粒逐渐长大(图 2),导致与碳气凝胶的结合变得困难,因而当水热时间达 30h时,α-Fe2O3含量反而低至89.74%.

图3 α-Fe2O3@CA复合材料的热重曲线
3 结 论
本文以FeCl3·6H2O为原料,通过改变水热合成温度和时间实现了α-Fe2O3@CA复合材料的可控制备.α-Fe2O3@CA复合材料形貌与合成温度有关,当温度为180℃和200℃时,α-Fe2O3分别表现出空心球状结构和橄榄球状结构.PVP活性剂有助于α-Fe2O3在气凝胶表面的负载,当在200℃下水热合成24 h时,α-Fe2O3在复合材料中负载高达96.53%.
[1] Huang L H, Chen Y G. Successful Hydrothermal synthesis of α-Fe2O3hexagonal micro-platelets and its application in Li-Ion battery[J]. Rare Metal Mat Eng,2013,42(10):2014-2018.
[2] 李娟,任保平.锂离子电池负极材料α-Fe2O3的水热合成与性能研究[J].电源技术,2010,34(9):881-884.
[3] Chai X H, Shi C S, Liu E Z, et al. Carbon-coated Fe2O3nanocrystals with enhanced lithium storage capability[J].Appl Surf Sci, 2015,347:178-185.
[4] 程琥,梁妹芳.纳米SnO2作为锂离子电池负极材料的研究进展[J].化工新型材料,2017,45(1):28-30.
[5] 张勤伟,李运勇,沈培康.三维多级孔类石墨烯载三氧化二铁锂离子电池负极材料[J].电化学,2015,21(1):66-71.
[6] 李小红,江向平,文思逸,等.不同形貌纳米α-Fe2O3粉末水热合成及其催化高氯酸铵热分解研究[J].人工晶体学报,2013,42(6):1132-1137.
[7] 康利莹,杨正龙,姜玮,等.锂离子电池负极材料α-Fe2O3的研究进展[J].化工新型材料,2016,44(11):11-13.
[8] Luo D W, Lin F, Xiao W D, et al. Silica aerogels modified SnSb/CNTs as high cycling performance anode materials for lithium batteries[J]. Trans Ind Ceram Soc,2016,75(3):1-5.
[9] Zhang X, Zhi W X, Yan B, et al. α-Fe2O3/PPy/Ag functional hybrid nanomaterials with core/shell structure:Synthesis, characterization and catalytic activity[J].Powder Technol, 2012,221:177-182.
[10] Akimov Y K. Fields of application of aerogels [J].Instrum Exp Tech, 2003,46(3):287-299.
[11] Guan D Y, Shen J, Liu N P, et al. The electrochemical performance of carbon-aerogel-based nanocomposite anodes compound with graphites for lithium-ion cells[J]. J Reinf Plast Comp, 2011,30(10):827-832.
[12] 周秋玲,李春忠,顾锋,等.水热合成氧化铁纳米结构及机理分析[J].功能材料,2008,39(9):1522-1524.
[13] 罗大为,陈佳明,李世伟,等.碳气凝胶修饰 SnSb复合负极材料的制备及性能研究[J].人工晶体学报,2017,46(1):8-12.
[14] Liu N P, Shen J, Liu D. A Fe2O3nanoparticle/carbon aerogel composite for use as an anode material for lithium ion batteries[J]. Electrochim Acta, 2013,97:271-277.
Abstract: The α-Fe2O3@CA particles were prepared by a simple hydrothermal method and modification of carbon aerogel, and this study focuses on the structure, morphology and α-Fe2O3loading content. Both the structure, the morphology and α-Fe2O3loading content of the α-Fe2O3@CA were characterized by XRD, SEM and TGA. The results show that hollow spherical and rugby-like α-Fe2O3are loaded on the carbon aerogel by hydrothermal method, and the α-Fe2O3loading content is related to the hydrothermal time. The loading of α-Fe2O3was up to 96.53wt%, when 24 h by hydrothermal synthesis at 200℃.
Key words: α-Fe2O3; carbon aerogel; synthesis; morphology
Controlled Synthesis and Characterization of α-Fe2O3Nanoparticle by Modification of Carbon Aerogel
CHEN Jinhong, LUO Dawei*, ZHENG Youkun, CHEN Ruizhi, ZHOU Kunyang
(School of Applied Chemistry and Biological Technology, Shenzhen Polytechnic, Shenzhen, Guangdong 518055, China)
TM912
A
1672-0318(2017)05-0059-05
10.13899/j.cnki.szptxb.2017.05.011
2017-05-27
*项目来源:广东省大学生科技创新培育专项资金资助项目(pdjh2017a0712);深圳市科技计划资助项目(JCYJ20160523113743114)
陈进洪(1995-),男,广东汕头人,大专.
*通讯作者:罗大为(1983-),男,博士,副教授,主要从事新型锂电池负极材料的研究.

