云木香二氯甲烷提取物抗肝纤维化活性成分的鉴定*
黄韵秋, 张正宽, 李靖, 付琼, 李晶, 廖尚高*
(贵州医科大学 药学院, 贵州 贵阳 550025)
云木香 [Saussrureacostus(Falc.) Lipech或AucklandialappaDecne]又称木香、青木香、广木香及兴瞿草[1-2]。云木香为云南道地药材,后引种至我国贵、川、两广等高寒潮湿等地,是全国重点中药材生产品种[3]。中国药典收录的多种中成药如小儿香精丸、八宝坤顺丸、三九胃泰胶囊等均采取云木香为主要原料[4]。云木香根茎入药,具有解除平滑肌痉挛、降压、抗菌、健胃及止痛的功效[5],现代药理研究对云木香及其活性成分主要集中在抗肿瘤、抗炎及抑菌方面[5]。已有的研究表明,云木香中存在单萜、倍半萜、三萜、糖苷、蒽醌及其它小分子类化合物,其中分离得到的倍半萜类单体占比最多,达200余个,为云木香的主要活性成分,涉及愈创木烷、吉玛烷、桉叶烷及橄榄烷等骨架类型,其中桉叶烷型骨架类型在该种属中数量最丰富[6]。随着对云木香的深入研究,含量较少的倍半萜二聚体和倍半萜与氨基酸杂合体也更多地被发现[6]。本课题组前期预实验结果显示,云木香95%乙醇提取物的二氯甲烷部位具有较好的抗肝纤维化(hepatic fibrosis,HF)作用[半数抑制浓度(the half maximal inhibitory concentration,IC50)=62 mg/L],但其活性成分未知。因此,本研究对该部位的化学成分进行研究,并评价各化学成分对人肝星状细胞(hepatic stellate cells,HSC)株LX-2的增殖作用的影响,确定二氯甲烷部位抗HF的活性成分。
1 材料与方法
1.1 实验材料
1.1.1主要药材及细胞来源 本研究所用的药材购自贵州土特产中药材批发市场,经贵州医科大学龙庆德副教授鉴定为凤毛菊属植物云木香(S.costus)的根,该药材标本(20190710)保存于贵州医科大学天然药物化学教研室;人HSC株LX-2购自广州吉尼欧有限公司。
1.1.2主要试剂 色谱分析、分离用的薄层层析硅胶GF254和柱层析硅胶(青岛海洋化工厂),Sephadex LH-20(瑞士Pharmacia Biotech),石油醚(60~90 ℃,上海泰坦科技股份有限公司),分析纯醋酸乙酯和甲醇(国药集团化学试剂有限公司),色谱甲醇和乙腈(上海萨恩化学技术有限公司),分析纯丙酮和氯仿(上海申博化工有限公司),胎牛血清(加拿大维森特生物技术有限公司),二甲基亚砜(dimethylsulfoxide,DMSO)和噻唑蓝(methyl thiazolyltetrazolium,MTT;北京索莱宝科技有限公司)。
1.1.3主要仪器 Bruker AVANCE NEO 600M核磁共振(NMR)波谱仪(德国 Bruker公司),Thermo Scientific TSQ Endura三重四级杆质谱仪(美国赛默飞世尔科技公司),全波长多功能酶标仪(Bio-Tek)和SW-CJ-2D 型超净工作台(苏州净化设备有限公司),2001HY-6003型CO2细胞培养箱以及TS-8 型转移脱色摇床(海门市其林贝尔仪器制造有限公司)。
1.2 研究方法
1.2.1提取与分离 干燥的云木香药材根茎30 kg打成粗粉,室温浸泡24 h,95%乙醇加热回流提取2 h,共3次,合并粗提物并减压浓缩得到醇提浸膏5 kg;水溶浸膏,按等体积量有机试剂极性从小到大依次用石油醚、二氯甲烷、醋酸乙酯及正丁醇进行萃取,共计3次,完成分段处理。对二氯甲烷萃取部位(1 000 g),以正相硅胶(300~400目)为吸附剂,石油醚∶醋酸乙酯(纯石油醚、10∶1、5∶1、2∶1、1∶1、纯醋酸乙酯)进行梯度洗脱,薄层色谱检识后合并相同组分,共得到7个流分(Fr.1~Fr.7)。Fr.1(2.0 g)通过硅胶柱(300~400目)层析,以石油醚∶丙酮(40∶1、20∶1、5∶1)梯度洗脱,所得组分再经硅胶柱(300~400目)层析,以石油醚∶醋酸乙酯(40∶1、20∶1、5∶1)进行梯度洗脱,得到化合物11(5.0 mg)。Fr.2(39.7 g)通过硅胶柱(300~400目)层析,以石油醚∶丙酮(40∶1、20∶1、5∶1)梯度洗脱,得到11个组分(Fr.2-1~Fr.2-11);Fr.2-6经硅胶柱(300~400目)层析(石油醚∶醋酸乙酯,30∶1、10∶1、5∶1)梯度洗脱后得到6个组分(Fr.2-6-1~Fr.2-6-6);Fr.2-6-1经反复硅胶柱(300~400目)层析(石油醚∶醋酸乙酯,50∶1、30∶1、10∶1)梯度洗脱分离得到化合物2(20.1 mg)。Fr.2-6-2经正相制备型高效液相色谱(preparative HPLC, pHPLC;石油醚∶醋酸乙酯为70∶30)分离得到化合物3(2.3 mg)。对Fr.2-6-5先经Sephadex LH-20层析(氯仿∶甲醇为3∶2)进行分离除杂,再经反相pHPLC(甲醇∶水为68∶32)分离得到化合物13(7.1 mg)。Fr.2-8经反复硅胶柱(300~400目)层析(石油醚∶醋酸乙酯,50∶1、30∶1、10∶1)梯度洗脱分离得到化合物1(19.5 mg)。Fr.3(7.3 g)经硅胶柱(300~400目)层析(石油醚∶丙酮,20∶1、10∶1、5∶1)进行梯度洗脱分离得到13个组分(Fr.3-1~Fr.3-13)。Fr.3-3经反相pHPLC(甲醇∶水为68∶32)分离得到化合物12(5.1 mg)。Fr.3-9经硅胶柱(300~400目)层析(石油醚∶醋酸乙酯为20∶1、0∶1)分离后再利用pHPLC(甲醇∶水为65∶35)纯化后得到化合物16(1.2 mg)。Fr.4(11.2 g)经硅胶柱(300~400目)色谱,以石油醚∶丙酮(20∶1、10∶1、5∶1、7∶3、3∶2)梯度洗脱,得到5个组分Fr.4-1~Fr.4-5。Fr.4-3采用MCI(乙醇∶水,0%~100%)洗脱,分离得到9个组分Fr.4-3-1~Fr.4-3-9。Fr.4-3-8经硅胶柱(二氯甲烷∶醋酸乙酯为1∶0、0∶1)后经过正相pHPLC(石油醚∶醋酸乙酯为60∶40)分离得到化合物8(2.0 mg)。Fr.4-3-2经过反相pHPLC(甲醇∶水为60∶40)分离得到化合物15(4.1 mg)。Fr.4-3-3经硅胶柱(300~400目)层析(二氯甲烷∶甲醇为1∶0、0∶1) 洗脱得到Fr.4-3-3-1~Fr.4-3-3-5。Fr.4-3-3-1经过硅胶柱(300~400目)层析(石油醚∶丙酮为20∶1、0∶1)分离得到化合物14(1.2 mg)。Fr.4-3-4经羟丙基葡聚糖凝胶柱(sephadex LH-20,氯仿∶甲醇为3∶2)洗脱得到6个组分Fr.4-3-4-1~Fr.4-3-4-6,Fr.4-3-4-3经过硅胶柱(300~400目)层析(二氯甲烷∶醋酸乙酯为1∶0、0∶1)洗脱得到5个组分(Fr.4-3-4-3-1~Fr.4-3-4-3-5),Fr.4-3-4-3-4经反相pHPLC(甲醇∶水为56∶44)分离得到化合物6(1.5 mg),其中Fr.4-3-4-3-1经过正相pHPLC(石油醚∶醋酸乙酯为60∶40)分离得到化合物5(1.3 mg),Fr.4-3-3-4经过反相pHPLC(甲醇∶水为64∶36)分离得到化合物4(1.4 mg)。Fr.4-2经过硅胶柱(300~400目)层析(二氯甲烷∶甲醇为1∶0、0∶1)洗脱后得到9个组分(Fr.4-2-1~Fr.4-2-9),Fr.4-2-3先经羟丙基葡聚糖凝胶柱(Sephadex LH-20)分离后经正相pHPLC(石油醚∶醋酸乙酯为40∶60)纯化得到化合物9(2.2 mg)和化合物10(1.5 mg);Fr.4-2-6过硅胶柱(300~400目)层析(石油醚∶醋酸乙酯为1∶0、0∶1)和反相pHPLC(甲醇∶水为72∶28)分离纯化得到化合物7(2.1 mg)。
1.2.2化合物单体成分及阳性药的配制 二甲基亚砜溶解单体化合物以及阳性药索拉非尼,配制成100 mmol/L母液,-20 ℃保存备用。
1.2.3细胞培养 LX-2细胞使用含有10%胎牛血清和1%双抗(青霉素和链霉素)的DMEM高糖培养基(完全培养基)于37 ℃、5%CO2及90%湿度环境中孵育,显微镜下观察细胞长满培养瓶至80%~90%后进行一传二培养,每隔2 d换液,取处于对数期细胞用于抗HF活性测试。
1.2.4抗HF活性测试 取处于对数生长期的LX-2细胞,胰蛋白酶消化,用培养基混悬以50个/L的密度以100 μL/孔体积接种于96孔培养板中,边缘加无菌PBS 200 μL,铺板24 h,弃上清;1、10、50、100及200 μmol/L不同浓度单体化合物组以100 μL/孔加入板中,另设正常对照组、DMSO对照组、阳性药对照组,以上各组均设6个复孔;给药48 h,弃上清,避光加5 g/L MTT溶液100 μL,孵育4 h,除尽上清液,加二甲亚砜100 μL,摇床摇匀10 min;选定测定波长为492 nm,于酶标仪上测定溶液的吸光度(absorbance,A),计算细胞存活率。
2 结果
2.1 结构鉴定
经质谱和NMR数据分析,所分离到的16个化合物结构分别得以鉴定(如图1)。
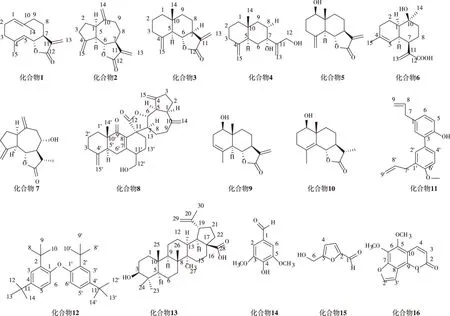
图1 从云木香中分离得到的16个化合物Fig.1 16 compounds isolated from Saussurea costus
2.1.1化合物1无色针晶(丙酮)。ESI-MS为 255.1 [M+Na]+。1H-NMR (DMSO-d6,600 MHz)δ: 6.05 (1H,d,J=3.6 Hz,H-13a),5.66 (1H,d,J=3.6 Hz,H-13b),4.79 (1H,dd,J=11.2,3.6 Hz,H-1),4.74 (2H,m,H-5,6),2.61 (1H,m,H-7),2.31~2.20 (3H,m,H2-9,H-3a),2.09~2.05 (3H,m,H-3b,H2-2),1.95~1.91 (1H,m,H-8a),1.69~1.65 (1H,m,H-8b),1.63 (3H,s,CH3-15),1.34 (3H,s,CH3-14);13C-NMR (150 MHz,DMSO-d6)δ: 170.0 (C-12),140.6 (C-11),140.5 (C-4),137.0 (C-10),127.5 (C-1),126.2 (C-5),119.4 (C-13),81.2 (C-6),49.5 (C-7),40.4 (C-9),38.8 (C-3),27.1 (C-8),25.8 (C-2),17.0 (C-15),15.9 (C-14)。化合物1鉴定为木香烯内酯。
2.1.2化合物2无色针晶(丙酮)。ESI-MS为 253.1 [M+Na]+。1H-NMR (CDCl3,600 MHz)δ: 6.26 (1 H,d,J=3.3 Hz,H-13a),5.53 (1H,d,J=3.3 Hz,H-13b),5.31 (1H,d,J=1.8 Hz,H-15a),5.11 (1 H,d,J=1.8 Hz,H-15b),4.94 (1H,br s,H-14a),4.86 (1H,br s,H-14b),4.00 (1H,t,J=9.3 Hz,H-6);13C-NMR (150 MHz,CDCl3)δ: 170.2 (C-12),151.2 (C-11),149.2 (C-4),139.7 (C-10),120.1 (C-13),112.6 (C-15),109.5 (C-14),85.2 (C-6),52.0 (C-5),47.6 (C-7),45.1 (C-1),36.2 (C-3),32.5 (C-9),30.9 (C-8),30.2 (C-2)。化合物2鉴定为脱氢木香内酯。
2.1.3化合物3淡黄色胶状物。ESI-MS为 271.1 [M+K]+。1H-NMR (CD3OD,600 MHz)δ: 6.01 (1H,d,J=3.1 Hz,H-13a),5.49 (1H,d,J=3.1 Hz,H-13b),4.93 (1H,s,H-15a),4.76 (1H,s,H-15b),4.06 (1H,t,J=10.9 Hz,H-6),2.63 (1H,m,H-7),0.89 (3H,s,CH3-14);13C-NMR (150 MHz,CD3OD,)δ:173.4(C-12),146.9 (C-4),141.8 (C-11),117.5 (C-13),109.5 (C-15),82.3 (C-6),56.5 (C-5),51.5 (C-7),43.2 (C-1),41.2 (C-3),40.2 (C-10),37.5 (C-9),24.5 (C-8),23.0 (C-2),18.8 (C-14)。化合物3鉴定为β-环木香烯内酯。
2.1.4化合物4白色粉末。ESI-MS为 259.2 [M+Na]+。1H-NMR (CDCl3,600 MHz)δ: 5.16 (1H,s,H-13a),5.13 (1H,s,H-13b),4.72 (1H,d,J=1.3 Hz,H-15a),4.39 (1H,d,J=1.3 Hz,H-15b),4.33 (2H,s,H2-12),3.49 (1H,s,-OH),2.30 (1H,m,H-5),2.29~2.27 (1H,m,H-3b),2.03 (1H,m,H-3a);13C-NMR (150 MHz,CDCl3)δ: 154.3 (C-11),150.0 (C-4),110.5 (C-13),104.8 (C-14),74.1 (C-7),64.4 (C-12),43.4 (C-5),40.9 (C-1),36.4 (C-3),35.1 (C-6),35.6 (C-9),35.1 (C-10),32.1 (C-8),23.0 (C-2),14.9 (C-15)。化合物4鉴定为7α-木香醇。
2.1.5化合物5白色粉末。ESI-MS为 271.1 [M+Na]+。1H-NMR (CDCl3,600 MHz)δ: 6.09 (1H,d,J=3.1 Hz,H-13a),5.41 (1H,d,J=3.1 Hz,H-13b),4.99 (1H,s,H-15a),4.86 (1H,s,H-15b),4.03 (1H,t,J=10.9 Hz,H-6),3.53 (1H,dd,J=11.5,4.6 Hz,H-1),2.18 (1H,d,J=10.9 Hz,H-5),0.82 (3H,s,CH3-14);13C-NMR (150 MHz,CDCl3)δ: 170.8 (C-12),142.6 (C-4),139.4 (C-11),117.2 (C-13),110.8 (C-15),79.7 (C-6),78.4 (C-1),53.1 (C-5),49.7 (C-7),43.1 (C-10),35.8 (C-9),33.7 (C-3),31.5 (C-2),21.6 (C-8),11.8 (C-14)。化合物5鉴定为瑞诺木烯内酯。
2.1.6化合物6白色粉末。ESI-MS为 273.1 [M+Na]+。1H-NMR (CD3OD,600 MHz)δ: 6.21 (1H,s,H-13a),5.50 (1H,s,H-13b),5.10 (1H,s,H-5),2.83~2.68 (2H,m,H-6,7),2.13 (1H,m,H-2a),1.99 (1H,m,H-3a),1.90 (1H,m,H-3b),1.81 (1H,dd,J=9.2,5.2 Hz,H-1),1.59~1.75 (3H,m,H-9a,H-9b,H-2b),1.54 (3H,s,CH3-15),1.17 (3H,s,CH3-14);13C-NMR (150 MHz,CD3OD)δ: 170.0 (C-12),145.8 (C-11),136.5 (C-4),124.4 (C-13),122.4 (C-5),73.8 (C-10),45.6 (C-1),42.9 (C-9),42.9 (C-7),37.6 (C-6),29.6 (C-3),25.9(C-8),25.1 (C-14),23.8 (C-15),23.1 (C-2)。化合物6鉴定为10α-羟基青蒿酸。
2.1.7化合物7无色油状物。ESI-MS为 271.1 [M+Na]+。1H-NMR (CD3OD,600 MHz)δ: 5.13 (1H,s,H-15a),4.99 (1H,s,H-15b),4.94 (1H,s,H-14a),4.85 (1H,s,H-14b),3.94 (1H,t,J=9.7 Hz,H-6),3.61 (1H,td,J=9.3,5.4 Hz,H-8),2.96 (1H,m,H-1β),2.83 (1H,t,J=9.1 Hz,H-5),2.68 (1H,dd,J=12.6,5.3 Hz,H-9a),2.61 (1H,dq,J=10.7,7.1 Hz,H-11) 2.52~2.46 (2H,m,H-3a,3b),2.17~2.08 (1H,m,H-9b),1.95 (1H,m,H-2a),1.86 (1H,m,H-2b),1.33 (3H,d,J=7.1 Hz,CH3-13);13C-NMR (150 MHz,CD3OD)δ: 181.7 (C-12),153.5 (C-4),146.8 (C-10),114.2 (C-14),109.5 (C-15),82.3 (C-6),76.1 (C-8),56.4 (C-7),53.8 (C-5),48.4 (C-1),48.3 (C-9),42.7 (C-11),33.4 (C-2),31.0 (C-3),16.5 (C-13)。化合物7鉴定为8α-羟基-11β-11,13-二氢去氢海桑内酯。
2.1.8化合物8白色粉末。ESI-MS为 485.3 [M+Na]+。1H-NMR (CDCl3,600 MHz)δ: 5.30 (1H,s,J=1.8 Hz,H-15a),5.07 (1H,s,J=1.8 Hz,H-15b),4.93 (1H,s,H-15′a),4.84 (1H,s,H-14a),4.77 (1H,s,H-14b),4.67 (1H,s,H-15′b),4.03 (1H,t,J=9.6 Hz,H-6),3.85 (1H,dd,J=10.7,4.3 Hz,H-12′a),3.80 (1 H,dd,J=10.7,7.2 Hz,H-12′b),3.12 (1H,t,J=9 Hz,H-5),2.95 (1H,m,H-7),2.86 (1H,m,H-1),2.75 (1H,s,H-6′a),2.53 (2H,m,H-3),2.49 (1H,m,H-11′),2.48 (1H,m,H-5′),2.46 (1H,s,H-9a),2.32 (1H,m,H-3′a),2.28 (1H,s,H-6′b),2.09~2.03 (1H,m,H-1),1.97~1.89 (5H,m,H-2a,H-3′b,H-9b,H-13a,H-13′a),1.84~1.75 (3H,m,H-2′,H-13b),1.82 (1H,m,H-8),1.78 (1H,m,H-13′b),1.44 (1H,m,H-1′b,H-2′b),1.25 (1H,m,H-2b),0.91 (1H,s,CH3-14′);13C-NMR (150 MHz,CDCl3)δ: 202.7 (C-16),180.8 (C-12′),159.6 (C-12),152.8 (C-4),152.0 (C-4′),150.6 (C-10),147.8 (C-10′),130.6 (C-14′),111.5 (C-14),109.7 (C-15′),108.3(C-15),84.1 (C-6),64.5 (C-6′),51.8 (C-5′),50.1 (C-5),47.9 (C-7),47.0 (C-1′),46.2 (C-1),44.9 (C-11),43.5 (C-13),38.0 (C-7′),35.9 (C-9),33.4 (C-11′),32.8 (C-9′),31.4 (C-3),30.2 (C-17),29.8 (C-2′),29.4 (C-3′),24.1 (C-2),22.8 (C-8′),21.0 (C-8),15.4 (C-13′)。化合物8鉴定为Vlasouliolide B。
2.1.9化合物9白色粉末。ESI-MS为 271.1 [M+Na]+。1H-NMR (CD3OD,600 MHz)δ: 5.94 (1H,d,J=3.2 Hz,H-13a),5.43 (1H,d,J=3.2 Hz,H-13b),5.31 (1H,m,H-3),3.97 (1H,t,J=11.0 Hz,H-6),3.55 (1H,dd,J=10.1,6.7 Hz,H-1),2.51 (1H,m,H-7),2.33 (1H,m,H-5),2.26 (1H,m,H-2α),2.06~2.00 (1H,m,H-8α),2.04 (1H,m,H-9β),1.97 (1H,m,H-2β),1.76 (3H,s,H-15),1.64~1.56 (1H,m,H-8β),1.30~1.24 (1H,m,H-9α),0.81 (3H,s,H-14);13C-NMR ( 150 MHz,CD3OD)δ: 172.9 (C-12),141.1 (C-11),134.8 (C-4),123.0 (C-3),117.2 (C-13),83.6 (C-6),76.0 (C-1),52.5 (C-5),52.3 (C-7),42.3 (C-10),35.7 (C-9),33.6 (C-2),23.8 (C-15),22.3 (C-8),11.5(C-14)。化合物9鉴定为珊塔玛内酯。
2.1.10化合物10淡黄色粉末。ESI-MS为 273.1 [M+Na]+。1H-NMR (CD3OD,600 MHz)δ: 3.42 (1H,dd,J=12.2,3.5 Hz,H-1),3.33 (1H,s,OH),2.39 (1H,dq,J=11.6,3.3 Hz,H-11),2.18 (1H,m,H-3),2.05 (1H,m,H-3),1.98 (1H,m,H-9b),1.92 (1H,m,H-8),1.80 (3H,s,CH3-15),1.77~1.67 (1H,m,H-2a),1.67~1.61 (2H,m,H-2b),1.57 (1H,m,H-8),1.32 (1H,m,H-9a),1.16 (3H,d,J=6.9 Hz,CH3-13),0.93 (3H,s,CH3-14);13C-NMR (150 MHz,CD3OD)δ: 181.4 (C-12),131.1 (C-5),126.3 (C-4),84.5 (C-6),78.5 (C-1),54.4 (C-7),43.2 (C-10),42.0 (C-11),39.7 (C-9),34.5 (C-3),27.8 (C-2),25.2 (C-8),19.9 (C-15),18.9 (C-14),12.6(C-13)。化合物10鉴定为草蒿素。
2.1.11化合物11亮黄色油状。ESI-MS为 319.3 [M+K]+。1H-NMR (CDCl3,600 MHz)δ: 7.38~6.83 (6H,m,Ar-H),5.99 (2H,m,H-8,8′),5.16~5.04 (5H,m,H2-9,9′,OH),3.88 (3H,s,OCH3),3.43 (2H,d,J=6.6 Hz,H2-7),3.35 (2H,d,J=6.6 Hz,H2-7′);13C-NMR (150 MHz,CDCl3)δ: 157.4 (C-4),151.2 (C-2′),138.2 (C-8′),136.9 (C-8),132.5 (C-5′),130.9 (C-2),130.6 (C-6′),130.6 (C-5),129.4 (C-1),129.1 (C-3),128.6 (C-1′),128.3 (C-6),116.3 (C-9′),115.9 (C-9),115.8 (C-4′),111.3 (C-3′),55.9 (OCH3),39.8 (C-7′),34.6 (C-7)。化合物11鉴定为4-O-和厚朴酚。
2.1.12化合物12无色蜡状固体。ESI-MS为 395.3 [M+H]+。1H-NMR (CDCl3,600 MHz)δ: 7.54 (2H,d,J=8.6 Hz,H-6,6′),7.36 (2H,d,J=2.4 Hz,H-3,3′),7.13 (2H,dd,J=8.6,2.4 Hz,H-5,5′),1.34 (18H,s,H3-12~14,12′~14′),1.29 (18H,s,H-8~10,8′~10′);13C-NMR (150 MHz,CDCl3)δ: 147.8 (C-1,1′),147.2 (C-4,4′),138.7 (C-2,2′),124.6 (C-3,3′),124.1 (C-5,5′),119.3 (C-6,6′),35.0 (C-7,7′) ,34.7 (C-11,11′),31.6 (C-12,13,14,12′,13′,14′),30.3 (C-8,9,10,8′,9′,10′)。化合物12鉴定为2,2-氧双(1,4)-二叔丁基苯。
2.1.13化合物13白色无定型粉末状。ESI-MS为 501.2 [M+HCOO]-。1H-NMR (DMSO-d6,600 MHz)δ: 12.05 (1H,s,OH-28),4.65 (1H,d,J=2.1 Hz,H-29b),4.56 (1H,d,J=1.3 Hz,H-29a),1.63 (3H,s,CH3-30),0.94 (3H,s,CH3-27),0.88 (3H,s,CH3-26),0.87 (3H,s,CH3-23),0.77 (3H,s,CH3-25),0.66 (3H,s,CH3-24);13C-NMR (150 MHz,DMSO-d6)δ: 177.2 (C-28),150.3 (C-20),109.6 (C-30),76.8 (C-3),55.4 (C-17),54.9 (C-5),49.9 (C-10),48.5(C-19),46.6 (C-18),42.0 (C-14),40.2 (C-8),38.5 (C-1),37.6 (C-4),37.6 (C-13),36.7 (C-9),36.1 (C-22),33.3 (C-7),31.7 (C-16),29.5 (C-21),28.1 (C-15),27.5 (C-23),27.2 (C-2),26.5 (C-12),19.8 (C-11),18.9 (C-29),17.3 (C-6),15.9 (C-25),15.8 (C-24),15.7 (C-26),14.4 (C-27)。化合物13鉴定为桦木酸。
2.1.14化合物14白色粉末。ESI-MS为 205.1 [M+Na]+。1H-NMR (CDCl3,600 MHz)δ: 9.83 (1H,s,CHO),7.16 (2H,s,H-2,H-6),6.08 (1H,s,OH),3.98 (6H,s,OCH3);13C-NMR (150 MHz,CDCl3)δ: 190.9 (-CHO),147.5 (C-3,C-5),140.9 (C-4),128.2 (C-1),106.8 (C-2,C-6),56.6 (OCH3)。化合物14鉴定为4-羟基-3,5-二甲氧基苯甲醛。
2.1.15化合物15浅黄色固体。 ESI-MS为127.2 [M+H]+。1H-NMR (CD3OD,600 MHz)δ: 9.54 (1H,s,-CHO),7.38 (1H,d,J=3.6 Hz,H-3),6.58 (1H,d,J=3.6 Hz,H-4),4.61 (2H,s,H2-6);13C-NMR (150 MHz,CD3OD)δ: 179.6(-CHO),163.4 (C-5),154.1 (C-2),125.1 (C-3),110.9 (C-4),57.8 (C-6)。化合物15鉴定为5-羟甲基糠醛。
2.1.16化合物16淡黄色针状结晶。ESI-MS为269.0 [M+Na]+。1H-NMR (CDCl3,600 MHz)δ: 8.09 (1H,d,J=9.7 Hz,H-4),7.66 (1H,d,J=2.1 Hz,H-2),7.08 (1H,d,J=2.1 Hz,H-3),6.37 (1H,d,J=9.7 Hz,H-3),4.15 (3H,s,C5-OCH3),4.03 (3H,s,C6-OCH3);13C-NMR (150 MHz,CDCl3)δ: 161.0 (C-2),150.0 (C-9),145.6 (C-2′),144.6 (C-5),143.4 (C-7),140.1 (C-4),135.3 (C-6),114.3 (C-3),113.9 (C-8),109.6 (C-10),104.5 (C-3′),62.6 (C6-OCH3),61.4 (C5-OCH3)。化合物16鉴定为茴芹内酯。
2.2 活性测试
化合物的抗HF活性测试结果(表1)表明,与空白对照比较,多数化合物对LX-2细胞的增殖有不同程度的抑制作用。其中,化合物2、8、9及11在考察的浓度范围内可以更加有效抑制LX-2细胞的增殖,其IC50依次为14.86、51.09、47.23及40.84 μmol/L;从活性数据来看,愈创木烷型化合物的活性相对突出,其中的化合物2具有最为显著的LX-2细胞增殖抑制作用;桉烷类倍半萜9虽然也表现出了一定的LX-2细胞增殖抑制作用,但该类结构中的其它化合物活性则相对较弱。
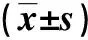
表1 不同浓度分离化合物对LX-2的细胞存活率及IC50 的影响Tab.1 Effect of different concentrations of isolated compounds on LX-2 cell survival rates and IC50
3 讨论
HF是各种急慢性肝损伤引起的以炎症反应和在肝脏中由于胶原累积形成过量细胞外基质(extracellular matrix,ECM)为主要损伤修复特点的病理过程[7]。目前抗HF的方法主要包含中医疗法、西医疗法、中西医结合治疗以及其它疗法,中医治疗主要采用中药复方(膈下逐瘀汤、鳖甲煎丸)、中药单体(大黄素、五味子素)以及针灸疗法,西医治疗采用抗HF治疗、抗病毒治疗(核苷类药物、微生态制剂联用及干扰素联合抗病毒治疗),虽然药物品种繁多,但尚无有效根治HF的药物[7]。
HF的形成机制比较复杂,涉及多种因素。其中,HSC增殖活化激活后并转化为肌成纤维细胞是HF的中心环节[8];在正常生理条件下肝脏中HSC处于静息状态,当肝脏受到外界刺激时静息的HSC会被激活,并表现出明显的细胞增殖[8]。因此,抑制HSC的活化和增殖为抗HF药物研发提供了思路。
人HSC株 LX-2细胞是从正常人的肝脏中分离出来并在低血清条件下进行培养而得来的HSC,与人体内激活的HSC极为相似,是抗HF药物筛选的重要工具[8]。本课题组前期预实验抗HF药物筛选中发现,云木香的氯仿萃取物对人HSC株 LX-2细胞的增殖具有显著的抑制作用,但是其抗HF活性物质尚未可知。本研究以抗HSC增殖的抑制活性为导向,对云木香的二氯甲烷部位进行了化学成分研究,从中分离得到了16个化合物,将分离化合物的波谱数据与国内外研究[9-24]分别比对最终确定化合物1~16的结构归属。其中化合物1~10为倍半萜类化合物(化合物8为二聚倍半萜),是其中的主要化合物;化合物13为三萜类化合物;化合物11和16为苯丙素类化合物;这些倍半萜类成分以桉烷型(化合物3、4、5、9及10)为主,并同时包括愈创木烷型(化合物2、7及8)、杜松烷型(化合物6)和吉玛烷型(化合物1)倍半萜;在这些化合物中,化合物4、11、12及16为首次从云木香中分离得到;从16个化合物的LX-2细胞增殖抑制作用来看,化合物2、8、9及11活性相对突出,可能是云木香的主要抗HF活性成分;从化合物8的结构看,二聚体的存在似乎对愈创木烷类倍半萜的活性有利,这与二聚倍半萜的特殊作用相一致[25]。同时,不饱和环外双键五元内酯环结构可能是该类结构中的化合物2活性最强的主要原因。在5个桉烷性倍半萜中,具有该类结构的化合物5和9均有不同程度的HSC增殖抑制活性,而无该结构的化合物4和10则没有活性,说明该结构对此类化合物的HSC增殖抑制活性至关重要。另一方面,构效关系分析表明,相较于Δ3(15)双键(化合物5),Δ3双键(化合物9)对活性更有利。这些构效关系的发现对倍半萜抗HF的研究提供参考。有关这些化合物抗HF机制的研究对该类化合物抗HF的药物研发也将产生重要影响。
——青蒿素

