肉芽肿性多血管炎并发大动脉病变诊疗一例
杨华夏,陈茹萱,陈 洋,冯瑞娥,蒋 颖,张奉春
作者单位:100730北京,中国医学科学院北京协和医学院北京协和医院风湿免疫科风湿免疫病学教育部重点实验室 (杨华夏、陈茹萱、陈洋、蒋颖、张奉春),北京协和医院病理科 (冯瑞娥)
肉芽肿性多血管炎(granulomatosis with polyangiitis,GPA)属于系统性血管炎分类的小血管炎中抗中性粒细胞胞质抗体(anti-neutrophil cytoplasmic antibody,ANCA)相关血管炎中的一种[1],其病变主要累及小血管,包括毛细血管、微静脉、微动脉、中/小静脉、中/小动脉等。GPA并发大动脉病变在临床上少见,迄今仅有国外少数关于GPA可并发主动脉及其一级分支受累的个案报道,表现为血管周围炎、管壁增厚、管腔狭窄、夹层等,血管病变严重者需外科或介入手术治疗。目前国内尚未见到GPA并发大动脉病变的病例报道。
1 病例报告
患者,男,27岁,因胸痛 1年、眼红 3个月于2017年2月就诊于北京协和医院。患者2016年1月无诱因出现胸痛,伴胸闷、乏力感,无发热、盗汗等症状,行胸部CT平扫检查发现右肺下叶空洞,其内未见液平(图1);升主动脉、无名动脉起始部管壁增厚,呈环形高密度影。主动脉CT血管成像显示升主动脉及主动脉弓前部管壁增厚(图2),考虑为主动脉夹层,故行升主动脉及主动脉弓置换术。术中见主动脉外膜水肿,主动脉管壁明显变硬变厚,弹性差。北京协和医院病理科检查提示病变累及主动脉壁及其周围组织,可见较多淋巴细胞、浆细胞、中性粒细胞浸润,可见小血管炎,散在多核巨细胞聚集形成肉芽肿,并见坏死及微脓肿形成(图2)。术后患者胸痛症状缓解。2016年11月患者无诱因出现左眼球结膜红肿、眼痒、异物感、烧灼感及胀痛,伴少许脓血性分泌物,当地医院给予左氧氟沙星滴眼液点眼,治疗后症状无明显改善。2016年12月患者无诱因发热,伴胸痛、咳嗽、咳少量白痰,偶有暗红色血丝痰,当地医院初步诊断为肺脓肿,先后给予莫西沙星、万古霉素、美罗培南等药物全身应用,症状无改善,为进一步诊治收入北京协和医院。患者既往史、个人史及家族史无特殊发现。体格检查:双上肢血压135/75 mm Hg(1 mm Hg=0.133 kPa),心率85次/min。患者双眼结膜充血,鼻旁窦区无压痛,双耳听力正常。双侧颈总动脉、锁骨下动脉及腹主动脉可闻及收缩期吹风样杂音,主动脉瓣听诊区可闻及收缩期III级杂音,肾动脉、髂动脉及股动脉未及血管杂音。双肺未及干湿啰音,腹部检查未发现异常。实验室检查:血、尿、便常规正常,血肌酐76 μmol/L,红细胞沉降率(erythrocyte sedimentation rate,ESR)22 mm/h,超敏 C 反应蛋白 7.75 mg/L,ANCA 反应阳性,C1:20,PR3-ANCA>200 RU/ml,抗核抗体(antinuclear antibody,ANA)反应阴性。主动脉CT血管成像可见头臂干管腔内内膜片影,疑似小夹层可能;升主动脉、主动脉弓、头臂干、左侧颈总动脉及锁骨下动脉起始段局部管腔周围可见软组织影,左侧颈总动脉起始段管腔狭窄;腹腔干起始段管腔中度狭窄;不能排除右侧肾动脉远端小动脉瘤;右肺团块状高密度影伴多发空洞形成,周围多发索条影;右肺小结节影;未见胸腔积液及心包积液。鼻旁窦CT及眼眶CT影像未见明显异常。眼科检查:左眼角膜病变。诊断:GPA,伴肺脏、眼部和大动脉受累。给予糖皮质激素冲击疗法,即甲泼尼松龙1 g/d,连续用药3 d,序贯大剂量糖皮质激素并按规律减量;环磷酰胺注射液静脉滴注(0.2 g,隔天1次),1个月后序贯口服。治疗1个月后患者胸痛、眼红症状消失,ESR正常,ANCA反应阴性。治疗后半年CT影像上肺部团块影消失(图1),主动脉弓及头臂干管壁病变好转。
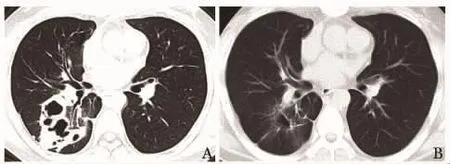
图1 患者治疗前后肺部病变的CT影像学变化Fig 1 CT imaging change of pulmonary lesions in present pretient before and after treatment
2 讨论
GPA是主要累及小血管的系统性血管炎,常并血清学ANCA反应阳性,病理学特点表现为肉芽肿、坏死及血管炎。GPA常累及耳鼻喉、呼吸道和肾脏组织,小血管炎并发大动脉受累患者非常少见。本例患者存在肺部影像学异常,病理检查提示动脉周围肉芽肿性炎症,符合1990年美国风湿病学会GPA分类标准中第2条[2],GPA诊断明确,患者血清中PR3-ANCA高滴度升高亦支持GPA的诊断。患者主动脉病变的病理表现为典型的肉芽肿、坏死和微脓肿,为GPA的典型病理表现,因此从一元论的角度出发,考虑大动脉病变为GPA原发病所致。GPA累及大动脉的发病机制可能与ANCA介导的坏死性肉芽肿性炎症累及血管壁的滋养血管,进而导致血管周围炎及血管炎有关[3-4]。通过文献复习,主动脉周围炎为GPA的最常见大动脉受累表现[5]。主动脉周围炎的CT影像为围绕于主动脉周围的软组织密度影,炎症局限于主动脉外膜。本病常见的鉴别诊断包括:(1)感染性动脉周围炎葡萄球菌、链球菌、假单胞菌、分枝杆菌、梅毒、真菌等病原体感染所致。(2)炎症性动脉粥样硬化性动脉瘤[6]是重度动脉粥样硬化的少见表现,最常累及腹主动脉,组织病理学特点包括主动脉外膜重度炎症,以淋巴细胞和浆细胞浸润为主,亦可见嗜酸性粒细胞,主动脉壁厚度超过4 mm。(3)慢性特发性主动脉周围炎[7]包括炎症性腹主动脉瘤、特发性腹膜后纤维化(Ormond病)及二者的混合型。(4)自身免疫病合并的主动脉周围炎多发性大动脉炎、肉芽肿性多血管炎、系统性红斑狼疮、类风湿关节炎、IgG4相关疾病等均可出现。本病的其他大血管受累表现还包括管壁增厚、管腔狭窄闭塞和动脉瘤形成,应当引起临床医师的重视。

图2 患者主动脉病变CT血管成像及组织病理学表现Fig 2 CT angiographic image and pathologic findings of aorta in this patient A:可见主动脉管壁增厚、管腔狭窄(↑);B:组织病理学显示小血管炎和小静脉管壁炎性细胞浸润,并可见主动脉外膜,周围组织较多炎性细胞浸润(HE×100);C:多核巨细胞聚集形成肉芽肿(HE×100);D:中性粒细胞聚集形成微脓肿(HE×100)
GPA并发大动脉受累需要与多发性大动脉炎(takayasu arteritis,TA)进行鉴别。(1)病理特点:TA为常见的累及大动脉的炎症性疾病,病理多为肉芽肿性炎症,常见淋巴细胞、浆细胞等炎性细胞浸润,坏死少见。而GPA的病理特点除了肉芽肿性炎症外,还包括坏死、微脓肿和小血管炎,尤其是合并血管周围炎时,常伴坏死,典型者可表现为地图样坏死,以上特点在TA中少见。(2)血管病变的范围:显著的血管周围炎和夹层是ANCA相关血管炎并发大动脉受累的最主要表现,表现为血管周围软组织包块、动脉瘤、夹层和(或)破裂[8-9]。相比而言,TA主要表现为血管狭窄,而不是显著的血管周围炎。TA在病变急性期多引起中膜、内膜中膜交界处及外膜的水肿和炎性细胞浸润,后期多表现为中膜外层和外膜的肉芽肿性炎症,可引起外膜纤维化。而GPA的病理特点是可以只表现为血管周围炎,以血管外膜和血管周围受累为主。(3)其他:TA常见动脉壁增厚,主要为内膜及外膜层增厚,多为环周性增厚,而GPA引起的动脉壁增厚多为偏心性、主要累及血管壁外层[5]。本例患者的主动脉病变明确提示有坏死、微脓肿和小血管炎,因此大动脉病变应为GPA原发病所致,可能与大动脉壁的滋养血管受累有关。文献回顾中有血管病理的患者也与上述结果一致。
GPA大动脉受累是罕见且危重的情况,早期识别此类GPA及临床并发症并积极行免疫抑制治疗可能使血管病变发生逆转,降低患者的致残及致死风险。

