琥珀酰明胶致围手术期严重过敏反应病因诊断一例
林 静,肖 浩,张虹婷,孟 娟
作者单位:610041成都,四川大学华西医院麻醉科 (林静),华西医院耳鼻咽喉头颈外科过敏性鼻炎诊治中心 (肖浩、张虹婷、孟娟)
围手术期严重变态反应60%~70%由IgE介导,在2011年前的25年间全球已报道7000多例[1]。本文报告1例在麻醉诱导期由IgE介导的琥珀酰明胶严重变态反应。
1 病例报道
患者,男性,19岁。患者于2周前因高处坠落伤半个月在外院全身麻醉下行肠破裂修补术,术中无不良反应,术后恢复顺利。患者既往无过敏性疾病及其他特殊疾病史,本次入院术前常规体格检查未见异常。患者接受手术前半小时以头孢呋辛静脉滴注,麻醉诱导期给予丙泊酚110 mg、舒芬太尼20 μg、顺式阿曲库铵15 mg、咪达唑仑1 mg、盐酸戊乙奎醚0.5 mg静脉推注,待患者意识消失后插入气管导管,常规机械通气,见气道压正常,生命体征平稳;麻醉维持期先后给予右美托咪啶0.4 μg/(kg·h)静脉泵入、盐酸瑞芬太尼0.1 μg/(kg·min)静脉泵入、硫酸阿托品0.3 mg静脉推注及氨甲环酸1 mg缓慢静脉滴注。术中因术野渗血严重,输入琥珀酰明胶500 ml、乳酸林格液500 ml扩容。麻醉诱导1 h后患者血压降至70/40 mm Hg(1 mm Hg=0.133 kPa),心率90次/min,血氧饱和度98%,体格检查未见皮疹,双肺未闻及干、湿啰音,气道压正常,考虑低血容量型低血压,追加琥珀酰明胶500 ml、钠钾镁钙葡萄糖500 ml静脉滴注后患者血压恢复正常。30 min后患者血压突然再次降低,最低降至56/30 mm Hg,心率120次/min,出现频发房性早搏,体格检查可见胸部及上肢大面积风团,双肺未闻及干、湿罗音,气道压正常,考虑为围手术期过敏性休克,立即停用所有可疑致敏药物,给予甲泼尼龙120 mg、肾上腺素10 μg静脉推注2次,然后给以肾上腺素0.05~0.1 μg/(kg·min)静脉持续泵入,建立大通道加快输注晶体溶液,患者血压稳定后停用肾上腺素,皮疹消失。后续手术使用维库溴铵替代顺式阿曲库铵,具体使用药物、给药时间、反应发生时间见表1。
术后第3天对患者进行第1次围手术期严重过敏反应致敏药物检测。根据麻醉记录,选用致敏可能性最大的药物顺式阿曲库铵、琥珀酰明胶及氨甲环酸进行皮肤试验。先行皮肤点刺试验(skin prick test,SPT)(表2),分别以生理盐水、10 mg/ml组胺 (丹麦ALK-Abelló公司) 为阴性及阳性对照,15~20 min后判读结果,以风团直径较阴性对照大3 mm或以上判读为阳性,出现红斑或痒感者更支持阳性判读[2];SPT呈阴性或可疑阳性者则再行皮内试验 (intradermal test,IDT)。IDT药品浓度及稀释液浓度见表2,15 min判读结果,皮丘直径扩大3 mm或以上、出现红斑和痒感者为阳性反应[3]。本例患者3种可疑致敏药物SPT、IDT结果均为阴性,且SPT阳性对照者无明显风团,仅出现红斑 (图1)。
术后第5周再次行围手术期严重变态反应致敏药物检测。此次检测的可疑致敏药物包括咪达唑仑、顺式阿曲库铵、丙泊酚、阿托品、氨甲环酸和琥珀酰明胶,与术后第3天比较,风团及红晕反应明显;琥珀酰明胶1∶100稀释液IDT患者出现皮丘明显扩大,并伴有明显红晕,为强阳性反应 (图2);顺式阿曲库铵1∶100稀释液IDT可见皮丘直径扩大3 mm,无红晕,呈可疑阳性反应(图3);其余药物SPT、IDT均呈阴性反应。最终诊断:琥珀酰明胶变态反应、顺式阿曲库铵可疑变态反应,建议患者围手术期避免用琥珀酰明胶及顺式阿曲库铵,可用维库溴铵替代顺式阿曲库铵。
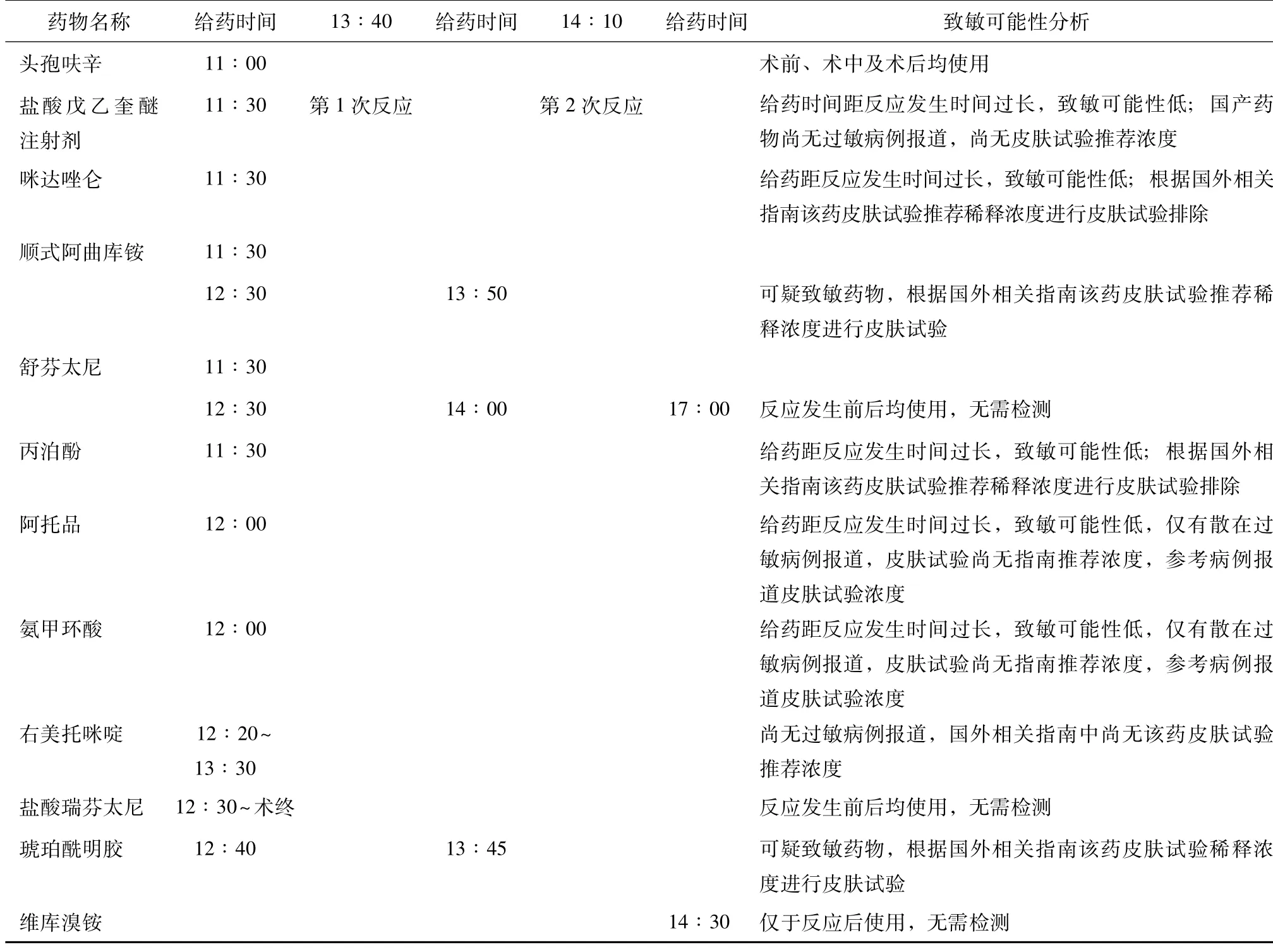
表1 药物致敏可能性分析
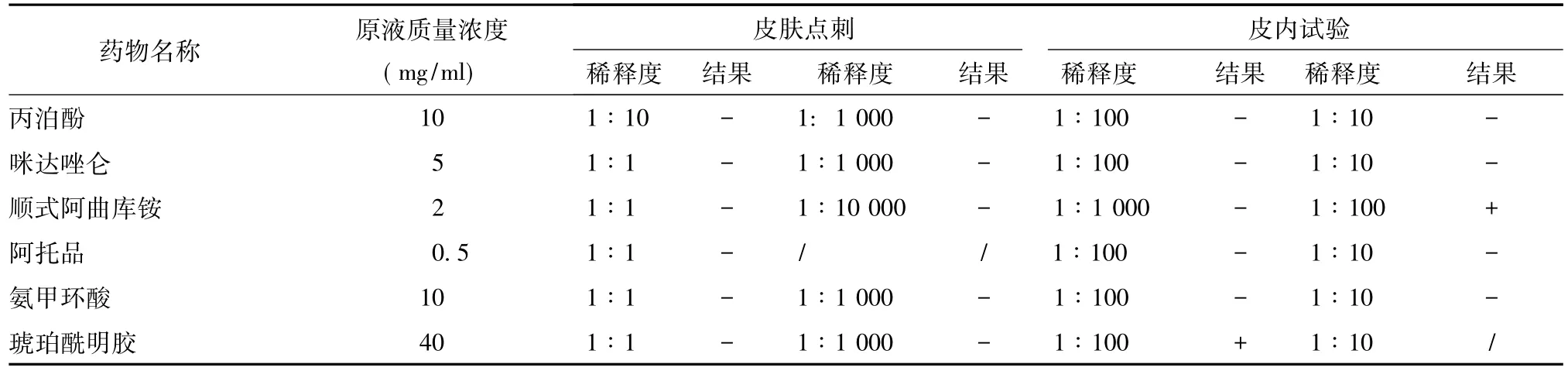
表2 皮肤试验药物浓度及第2次皮肤试验结果
2 讨论

图1 第1次可疑致敏药物皮肤试验结果阳性对照仅呈红晕反应,无明显风团;顺式阿曲库铵、氨甲环酸、琥珀酰明胶皮肤点刺试验及SPT、IDT均为阴性(标注圈为皮内试验药物注入皮内形成皮丘)

图2 琥珀酰明胶阳性结果最内圈为IDT药物注射形成皮丘,中间圈为IDT 15 min后扩大皮丘,最外圈为IDT 15 min后红晕范围

图3 顺式阿曲库铵皮内试验阳性结果最内圈为IDT药物注射形成皮丘,中间圈为IDT 15 min后扩大皮丘
流行病学调查显示,法国围手术期严重变态反应发生率为1/13 000,其中女性患者高于男性,男女之比为1 ∶3[9],澳大利亚为 1/10 000~20 000[10-11]。欧洲药物过敏协作组曾于2011年总结了1980年以来英文和法文文献,表明常见的引起围手术期严重过敏反应的药物及试剂依次为神经肌肉阻滞剂(63%)、乳胶 (14%)、镇静催眠药 (7%)、抗生素(6%)、血浆代用品 (3%)及阿片类 (2%),其他药物还有氯已定 (洗必泰)、肝素、亚甲蓝以及非甾体类抗炎药 (non-steroid anti-inflammation drugs,NSAIDs)等,局部麻醉药过敏者罕见,尚未发现吸入麻醉剂过敏的报道。60%~70%的围手术期严重过敏反应是由IgE介导的,在2011年之前的25年间全球报道的围手术期发生IgE介导严重变态反应共7 000多例[1]。我国目前尚未建立围手术期严重变态反应报告机制,且围手术期严重过敏反应的病因诊断尚未得到公认,因此缺乏相关流行病学数据。
在患者严重变态反应发作期内,血清类胰蛋白酶测定为唯一的血液学检测指标,该指标含量的升高是肥大细胞活化及脱颗粒的标志。血清类胰蛋白酶在严重变态反应发生后30 min内即开始升高,其半衰期约为120 min,随后逐渐降低[12]。因此欧洲相关指南推荐,严重变态反应发生后需进行多个时点的血清类胰蛋白酶检测,第1次采样应在复苏成功后尽早进行,第2次采样在发作后2 h进行,由于血清类胰蛋白酶增高可以持续数小时,因此6 h内采样均有诊断价值,第3次采样应在发作24 h之后进行,目的是获得患者血清类胰蛋白酶基线值[6,13]。血清类胰蛋白酶的升高为严重变态反应的诊断依据,但血清类胰蛋白酶检测结果正常也不能排除严重变态反应的可能。我国目前缺乏血清类胰蛋白酶检测合法商业化试剂,故严重变态反应的诊断主要依据临床症状及体征,缺乏实验室检测数据的支持。
根据症状的严重程度,严重变态反应可分为四级:Ⅰ级仅有皮肤症状,如皮肤潮红、风团、血管神经性水肿;Ⅱ级可观察到不危及生命的症状,包括皮肤表现、低血压、心动过速及呼吸窘迫 (咳嗽、通气困难);Ⅲ级:威胁生命的症状,如心动过速或心动过缓、心律紊乱、支气管痉挛;Ⅳ级者可发生心搏和/或呼吸停止[1]。本例患者严重过敏反应严重程度为Ⅲ级。严重变态反应可发生在围手术期的任何阶段,但90%以上发生在麻醉诱导期。本例患者严重变态反应发生在麻醉维持期,相对少见。总体来说,发生于麻醉维持期的严重变态反应较发生于诱导期的病因诊断难度更大,因为涉及的可疑致敏药品种类更多;非IgE介导的严重变态反应可能性更大,而皮肤试验可能无法测出,需进行药物激发试验,以明确致敏药物,如NSAID、某些阿片类药物 (吗啡、可待因)等。严重过敏反应发生时间与可能诱发药物和试剂见表3[6]。
血浆扩容剂引起的严重变态反应占围手术期严重变态反应的 4%[4,14]。一项共纳入 200 906例输入胶体扩容剂患者的多中心前瞻性研究显示69例发生严重变态反应,明胶严重变态反应发生率为0.038%,高于血浆清蛋白的0.003%、羟乙基淀粉

表3 严重过敏反应发生时间与可能的诱发药物和试剂
的0.006%和右旋糖苷的0.008%[15];另外一项纳入19 593例输入胶体扩容剂患者的前瞻性研究发现43例出现严重变态反应,发生率为0.219%,其中明胶发生率最高,为0.345%,右旋糖苷为0.273%,血浆清蛋白 0.099%,羟乙基淀粉为0.058%[16]。目前临床中常用的明胶制剂包括交联明胶、尿联明胶 (聚明胶肽)及琥珀酰明胶,其中交联明胶过敏率为0.62%,尿联明胶为0.15%~0.85%(0.05%为严重变态反应),琥珀酰明胶为0.07%~0.34%(0.016%为严重变态反应)[17],可见在明胶中琥珀酰明胶过敏率最低。明胶引起变态反应的机制目前尚未明确,仅部分是由IgE介导的,所以部分明胶过敏的患者可通过皮肤试验确诊[18-20],亦可进行明胶sIgE检测 (瑞典赛默飞世尔公司,C74)。明胶皮肤试验和 (或)sIgE检测结果阳性可确诊明胶过敏,但阴性结果不能完全排除明胶过敏。目前国内尚无明胶sIgE检测试剂,故本例患者仅尝试行琥珀酰明胶皮肤试验,较低质量浓度(1∶100,即0.04 mg/ml)IDT即出现强阳性反应。术中患者出现第1次过敏反应距开始静脉滴注琥珀酰明胶的时间约为1 h,发生时间较晚,可能与给药方式有关,静脉推注给药变态反应发生迅速,多在给药后数分钟发生。患者第1次反应表现为血压下降及心率增快,因未发现皮疹,初步判断是低血容量性休克,故再次追加琥珀酰明胶,患者再次发生变态反应,时间间隔更短,症状更重,且出现皮疹。结合皮肤试验结果及病史,可以确诊该患者是由IgE介导的施琥珀酰明胶过敏。
本例患者在用1∶100的顺式阿曲库铵IDT在1∶100稀释度 (指南推荐的不引起皮肤非特异性刺激反应的最高浓度)时发生阳性反应。通常肌肉松弛剂引起的严重变态反应多发生在麻醉诱导期,而本例患者发生在维持期,由于肌肉松弛剂的特殊药理特性,因此无法进行药物激发试验以确诊。从保证临床安全的角度考虑,建议患者术中避免使用顺式阿曲库铵。由于肌肉松弛剂均具有铵盐基团,因此不同的肌肉松弛剂之间可能有交叉反应。当全身麻醉中所使用的肌肉松弛剂皮肤试验为阳性时应对其他可替代肌肉松弛剂进行皮肤试验。本例患者在出现变态反应后使用维库溴铵替代顺式阿曲库铵,患者生命体征平稳,故未再进行交叉反应皮肤试验。
指南通常推荐皮肤试验最好在围手术期严重变态反应发生后4~6周进行,以免严重变态反应后体内sIgE消耗殆尽处于不应期而出现假阴性结果。若患者病情需要亦可在严重变态反应发生后6周内进行,试验阳性者有诊断价值,结果阴性者6周后应复查[1,6]。本例患者第1次诊断呈阴性结果,原因可能如下:(1)检测时间距变态反应发生的时间太近;(2)术中为了控制严重变态反应使用大剂量静脉用糖皮质激素后使得皮肤的反应受到抑制,这一点可从第1次检测时阳性对照 (组胺)反应非常微弱,仅有红晕而无明显风团即可证实,患者5周后的第2次检测发现对琥珀酰明胶反应阳性,提示若非病情需要,应尽量在严重变态反应发生4~6周后再进行皮肤试验,以免出现假阴性结果。
嗜碱性粒细胞活化试验可通过流式细胞仪对嗜碱性粒细胞表面的活化标志分子的检测进行评估,包括CD63、CD203c等,识别诱发严重变态反应的药物。但由于该检测方法尚未标准化,如血标本存储时间、染色方法、检测流程、流式细胞仪所用激光波长、药物浓度等均仍尚在探索之中[21-22],因此目前主要用于科研,并未成为临床常规检测项目。在英国围手术期严重变态反应诊疗指南中未推荐嗜碱性粒细胞活化试验[6],欧洲的相关指南中指出,嗜碱性粒细胞活化试验可作为皮肤试验的补充,但不能替代皮肤试验,若皮肤试验或者特异性IgE检测已经明确了致敏原,则无须再行嗜碱性粒细胞活化试验[1]。本例患者经皮肤试验已确定了致敏药物,故未再进行嗜碱性粒细胞活化试验。
在围手术期严重变态反应的病因诊断流程中,麻醉科和变态反应科医生之间的交流和合作非常重要。麻醉科医生需向变态反应科医生提供详细的麻醉记录单、患者变态反应出现的时间和临床表现、患者的基础疾病等信息,而非仅提供麻醉中所使用药物的简要清单。这些详细、准确的信息对于变态反应科医生初步分析和判断患者是否为过敏反应,进而选择皮肤试验所需的可疑药物或试剂,并确定拟检测药物的优先顺序均具有重要的参考价值。本例患者能够尽快明确致敏药物,即是麻醉科医生和变态反应科医生相互交流、相互配合的结果。
总之,围手术期严重变态反应发生率虽低,但可危及生命。在我国建立围手术期严重变态反应报告系统,完善流行病学统计调查数据,加强变态反应科与麻醉科的合作,建立围手术期严重变态反应规范诊断流程对于保证围手术期医疗安全具有重要的临床意义。

