中性粒细胞参与大疱性类天疱疮发生的相关机制
王亚男,赵文玲,李 丽
作者单位:100730北京,中国医学科学院北京协和医学院北京协和医院皮肤科
大疱性类天疱疮 (bullous pemphegoid,BP)是一种获得性自身免疫性疱病,临床上以躯干、四肢出现张力性大疱为主要特点。BP患者体内的循环自身抗体,如抗BP180、BP230抗体,攻击真表皮交界处半桥粒的组分BP180(BPAG2或XVII型胶原)、BP230(BPAG1e),通过激活补体、肥大细胞脱颗粒、中性粒细胞和嗜酸性粒细胞聚集等过程产生多种蛋白酶,降解真表皮交接处的正常组织结构,导致真表皮分离,产生水疱[1]。早在1997年,Liu等[2]发现被动转移鼠模型注射抗鼠BP180抗体可诱发水疱的形成,而用抗中性粒细胞特异性抗体消耗小鼠循环中的中性粒细胞后可见IgG、C3沉积在真表皮交界处,但没有炎症反应或水疱发生。由此证实中性粒细胞在BP的发生中起到至关重要的作用,中性粒细胞的有无直接决定了水疱能否形成。Oswald等[3]通过动物实验发现,用Ly-6G特异性单克隆抗体可使BP动物模型外周血中中性粒细胞明显减少,预先用Ly-6G单克隆抗体消耗中性粒细胞后BP动物模型的水疱临床活动评分明显降低,说明消耗中性粒细胞可以部分地抑制水疱的形成。血液中中性粒细胞变化与BP的关系正在引起更多的关注,为了更深入地了解BP的发病机制,本文就中性粒细胞参与BP的炎症反应过程进行综述,为BP的防治研究寻找潜在的靶点。
1 中性粒细胞的早期聚集
BP180IgG抗体在攻击真表皮交界处时,抗体Fab及Fc段分别结合相应受体参与下游反应,其中抗体Fab段与抗原BP180的结构域,即主要的抗原致病表位NC16A结合,并通过巨胞饮的方式内吞入表皮角质形成细胞[4],而抗体Fc段与中性粒细胞免疫球蛋白 (Ig)Fc段受体FcRIII结合[5],明显加快致病性抗体的降解,降低致病性抗体的循环半衰期,从而减少致病性IgG抗体[6]。抗原抗体结合后激活补体通路,包括经典激活途径和旁路激活途径,其中经典激活途径是参与BP发生的主要途径[7],生成补体C3a、C5a等,其中经典补体激活途径的产物C5a可通过直接及间接的方式促进中性粒细胞聚集,一方面作为中性粒细胞趋化因子直接诱导中性粒细胞趋化[5];另一方面,通过刺激局部细胞释放炎症介质,如白细胞介素 (interleukin,IL)-8,间接诱导中性粒细胞聚集[7],减少中性粒细胞向皮损处聚集,进而对BP起到治疗作用[8]。同时C3a和 C5a可共同激活肥大细胞,后者释放糜蛋白酶,促进中性粒细胞聚集。因此抗原抗体结合后主要通过补体激活及肥大细胞脱颗粒,促进中性粒细胞聚集,此为中性粒细胞的早期聚集[9-11]。
另外,在中性粒细胞聚集过程中还需要整合素介导的黏附及渗出。Liu等[2]分别用抗淋巴细胞功能相关抗原-1(lymphocyte function associated antigen-1,LFA-1)(CD11a/CD18)抗体、抗巨噬细胞抗原复合体1(macrophage antigen complex-1,MAC-1)抗体 (CD11b/CD18)对野生型小鼠进行预处理,发现注射了BP180致病性IgG抗体的小鼠并没有水疱产生,且MAC-1基因敲除小鼠体内出现中性粒细胞的浸润,最终没有水疱产生。说明中性粒细胞表面的整合素LFA-1及MAC-1对于中性粒细胞的聚集发挥了重要的作用,其中LFA-1主要参与早期及晚期中性粒细胞的聚集;而MAC-1主要作用于晚期中性粒细胞的聚集及凋亡[12-13]。同时,动物实验证实,一种在BP患者疱液中大量存在的中性粒细胞趋化因子脂质介质白三烯B4(lipid mediator leukotriene B4,LTB4)及其受体BLT1在中性粒细胞的聚集过程中也发挥关键作用。LTB4是致病性BP180抗体沉积于真表皮交界处后中性粒细胞浸润皮肤的关键驱动因子,缺乏LTB4合成的关键酶5-脂氧合酶的小鼠表现出抵抗中性粒细胞募集的现象,因而炎症反应受到抑制[14-15]。研究发现,减少中性粒细胞聚积至30%即可抑制表皮下水疱的形成,因此,中性粒细胞的量与疾病的严重性直接相关[13]。
2 中性粒细胞对皮肤组织的损伤机制及晚期聚集
聚集的中性粒细胞释放中性粒细胞弹性蛋白酶 (neutrophil elastase,NE)、组织蛋白酶 (cathepsin G,CG)和基质金属蛋白酶9(matrix metalloproteinase 9,MMP-9)[6],共同参与组织基底膜的损伤。Lin等[12]研究发现,缺乏NE的小鼠不能诱发出BP,NE的主要作用是降解BP180的胞外结构域,形成多肽P561及P506,B6小鼠局部注射NE后可促进中性粒细胞向皮肤浸润,而注射α1蛋白酶抑制剂可完全阻断上述中性粒细胞趋化过程,主要原因在于NE降解BP180的多肽产物P561对中性粒细胞具有趋化作用。α1蛋白酶抑制剂是主要的NE抑制剂,其活性中心环与目标丝氨酸蛋白酶结合可形成高度稳定的、灭活的丝氨酸蛋白酶复合物,从而抑制丝氨酸蛋白酶,即中性粒细胞弹性蛋白酶的降解作用。据文献报道,先天性α1蛋白酶抑制因子缺乏的患者对NE的抑制作用减弱,过多的NE可降解肺泡壁的蛋白组分,造成肺气肿,因此,国外已将α1蛋白酶抑制剂用于部分肺气肿患者的治疗[16],目前尚无治疗BP的相关报道。MMP-9通过间接抑制α1蛋白酶抑制剂来调节NE的活性,MMP-9与NE还可将BP180切割成一些三肽,例如脯氨酸-甘氨酸-脯氨酸 (proline-glycine-proline,PGP),对中性粒细胞产生趋化作用[6],导致中性粒细胞进一步聚集,炎症反应加重,形成炎症的正反馈环路,此即中性粒细胞的晚期聚集。因此NE、MMP-9除了具有对BP180及胞外基质的切断作用外,还参与促进晚期中性粒细胞的聚集作用[12](图1)。此外中性粒细胞和单核细胞可产生趋化因子配体10(Cxc chemokine ligand 10,CXCL10)[17],激活胞外激酶1/2、P38、PI3K(Akt) 通路[18],进一步激活还原型辅酶氧化酶 (nicotinamide-adenine dinucleotide phosphate oxidase,NADPHO),产生活性氧[19],活性氧及血纤维蛋白溶酶系统可激活MMP-9的前体物质,促进MMP-9的产生。中性粒细胞与肥大细胞产生的IL-17可促进CXCL10的产生,进一步上调MMP-9与NE 的产生[6,20-21],甲强龙或复合体A(一种新型的非甾体激素受体配体)可抑制这个过程[17,19-20],说明甲强龙可通过抑制中性粒细胞而对BP发挥治疗作用。
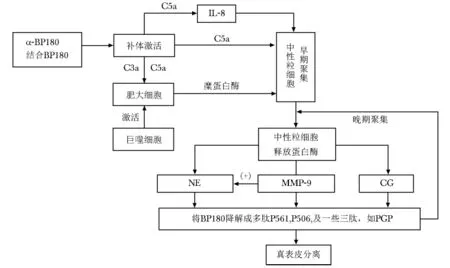
图1 BP发生和发展过程中中性粒细胞对皮肤组织的损伤机制IL:白细胞介素;NE:中性粒细胞弹性蛋白酶;MMP-9:基质金属蛋白酶9;CG:组织蛋白酶;PGP:脯氨酸-甘氨酸-脯氨酸
3 小结
BP180IgG抗体可攻击皮肤组织的基底膜带,通过激活补体、肥大细胞脱颗粒而促进中性粒细胞的早期聚集,聚集的中性粒细胞释放多种蛋白酶以裂解基底膜带,从而产生水疱;同时,上述过程中的裂解物通过趋化作用促进中性粒细胞的晚期聚集,加重疾病的严重程度。综上所述,中性粒细胞在BP的发生和发展中扮演关键的角色,深入了解中性粒细胞参与BP的分子机制有助于为BP的治疗寻找新的靶点。

