血必净联合乌司他丁及奥曲肽治疗重症急性胰腺炎的疗效观察
朱晶晶,白艳丽,张腊梅
河南科技大学第一附属医院消化内科,洛阳 471000
急性胰腺炎是一种常见的、以胰腺局部炎症反应为主要特征的消化系统急症,约5%~10%的患者会进展为重症急性胰腺炎(severe acute pancreatitis,SAP)[1]。SAP 患者典型的临床表现为持续性上腹部剧烈疼痛、上腹部压痛、血清淀粉酶浓度异常升高及肠鸣音减弱或消失等,伴有持续(>48h)的器官功能障碍。SAP 患者病死率高,临床需高度重视。现阶段临床治疗SAP 的措施纷繁各异,但仍缺乏针对性的特异性药物。乌司他丁联合奥曲肽是当前治疗SAP 的常用方案,但SAP病理过程复杂、病情凶险,患者预后仍有较大的改善空间[2-3]。血必净是一种具有化瘀解毒功效的中药复方静脉注射制剂,可有效拮抗内毒素和炎症介质、改善凝血功能、增强机体免疫功能、保护重要脏器功能等,对SAP 的防治具有重要价值[4]。既往研究[5-6]显示,SAP 的发生发展与Toll 样受体4(Toll-like receptor 4,TLR4)/核因子κB(nuclear factor-κB,NF-κB)信号通路下游炎症因子的表达水平及辅助性T 细胞17 型(T helper cell 17,Th17)/调节性T 细胞(regulatory T cell,Treg)免疫失衡密切相关。目前尚无关于血必净联合乌司他丁及奥曲肽对SAP 患者血清TLR4/NF-κB 信号通路下游炎症因子水平和外周血Th17/Treg 免疫平衡影响的相关研究。基于此,本研究以2019 年1 月~2020 年12 月某院收治的SAP 患者为研究对象,采用血必净联合乌司他丁及奥曲肽进行治疗,通过观察其临床疗效以及该治疗方案对上述指标的影响,旨在探讨其可能的作用途径,为该治疗方案的临床应用提供一定参考。现报道如下。
1 资料与方法
1.1 一般资料
选取2019 年1 月~2020 年12 月某院收治的120 例SAP 患者为研究对象,采用随机数字表法分为观察组与对照组,每组60 例。其中,观察组:男性36 例,女性24 例;年龄27~70 岁,平均年龄(49.2±8.4)岁;病因构成为胆源性24 例、高甘油三酯血症性19 例、酒精性15 例、其他原因2 例;发病至就诊时间5~64h,平均时间(33.6±7.4)h。对照组:男性38 例,女性22 例;年龄25~69 岁,平均年龄(48.3±7.9)岁;病因构成为胆源性25 例、高甘油三酯血症性16 例、酒精性16 例、其他原因3 例;发病至就诊时间3~60h,平均时间(32.1±6.9)h。两组一般资料比较无统计学差异(P>0.05),具有可比性。本研究经本院医学伦理委员会审批通过(伦理批号:2019-03-021)。
纳入标准:①满足SAP 诊断标准[7]者。②既往对本研究涉及药物(血必净、乌司他丁、奥曲肽等)中任何成份无过敏史者。③年龄18~70 岁者,性别不限。④无认知及精神障碍者。⑤发病至就诊时间≤72h 者。⑥自愿签订知情同意书者。⑦入组前无相关治疗史者。排除标准:①合并其他消化系统疾病者。②伴有重要脏器(心肺肝肾等)疾病者。③患有免疫系统、血液系统或内分泌系统疾病者。④近1 个月内有外伤或手术史者。⑤过敏体质者。⑥合并感染性胰腺坏死等严重并发症需行手术治疗者。
1.2 治疗方法
所有患者入院后均给予相同的常规治疗,包括液体治疗、肠内营养支持治疗、镇痛、针对病因的治疗、并发症防治及合理使用抗菌药物等。对照组在常规治疗的基础上给予:注射用乌司他丁(广东天普生化医药股份有限公司,国药准字H19990134,规格10 万单位,产品批号20181105、20191207、20201004)静脉滴注,每次将10 万单位注射用乌司他丁加入250ml 氯化钠注射液(苏中药业集团股份有限公司,国药准字H32025057,规格250ml∶2.25g)中充分稀释后给药,bid,连用3 天,之后调整为10 万单位/次,qd,连用7 天;注射用醋酸奥曲肽(上海上药第一生化药业有限公司,国药准字H20060171,规格0.1mg,产品批号20181009、20191006、20200813),首次剂量为0.1mg,用20ml 氯化钠注射液稀释后缓慢静脉推注,而后调整为0.6mg/d,并以25μg/h速率持续静脉泵入。
观察组在对照组治疗基础上加用血必净注射液(天津红日药业股份有限公司,国药准字Z20040033,规格每支装10ml,产品批号1810025、1911016、2007036)静脉滴注,每次将100ml 血必净注射液加入100ml 氯化钠注射液中均匀混合后给药,bid。两组均连续治疗10 天。
1.3 观察指标
①临床疗效[8]。痊愈:治疗期间患者症状及体征(包括腹痛、上腹部压痛等)消失,肠鸣音恢复,且实验室指标(腹部CT 检查、血清淀粉酶)复常。显效:治疗期间患者症状及体征(包括腹痛、上腹部压痛等)消失,实验室指标明显改善;并发症未完全消失,或急性生理学和慢性健康状况评分Ⅱ(acute physiology and chronic health evaluationⅡ,APACHEⅡ)评分降低≥50%。有效:治疗期间患者症状及体征(包括腹痛、上腹部压痛等)好转,影像学检查(包括CT)及相关辅助检查指标较入院时有一定改善,但尚未复常,或APACHEⅡ评分降低<50%。无效:治疗期间患者症状及体征(包括腹痛、上腹部压痛等)无变化,或APACHEⅡ评分降低<30%,或加重转手术治疗者。临床治疗总有效率=(痊愈+显效+有效)例数/总例数×100%。②典型临床表现改善时间。统计两组腹痛、上腹部压痛消失时间及血清淀粉酶复常、肠鸣音恢复时间。③血清TLR4/NF-κB 信号通路下游相关炎症因子水平。入院当天(治疗前)和治疗10 天后次日清晨于患者空腹状态下采用无抗凝剂的真空采血管收集患者肘静脉血3ml,在室温下静置1h 后,采用LC-04L 型离心机(江苏正基仪器有限公司,r=13.5cm)以4000r/min 在4℃环境下离心10min,分离上清液,-40℃冻存备用,采用MK3 型酶标仪(美国赛默飞世尔科技公司)测定血清IL-8、IL-1β和TNF-α水平,试剂盒均购自北京百奥莱博科技有限公司,操作均按说明书;其中,IL-8 试剂盒的产品批号为201811003、201907015、202003010,IL-1β试剂盒的产品批号为201809025、201905017、202002006,TNF-α试剂盒的产品批号为201810019、201906030、202004029。④外周血Th17、Treg 细胞比例。入院当天(治疗前)和治疗10 天后次日清晨于患者空腹状态下采用含肝素钠的真空采血管收集患者肘静脉血3ml,制备外周血单个核细胞(peripheral blood mononuclear cells,PBMCs)悬液,加入荧光标记的鼠抗人CD4、CD25、CD127、IL-17单克隆抗体,经孵育、洗涤、重悬细胞后避光放置备用,采用FACSCalibur 型流式细胞仪(美国BD公司)测定外周血Th17、Treg 细胞比例,并计算Th17/Treg 比值,实验所需抗体均购自美国贝克曼库尔特公司,操作均按说明书;其中,CD4 试剂盒的产品批号为1809234、1906127、2004082,CD25 试剂盒的产品批号为1811205、1908153、2005172,CD127 试剂盒的产品批号为1811032、1907193、2004161,IL-17 试剂盒的产品批号为1810215、1906093、2003182。⑤不良反应发生情况。详细记录两组药物相关不良反应的发生情况,包括注射部位疼痛、腹泻、血糖紊乱、肝功能异常等。
1.4 统计学方法
运用SPSS 20.0 软件对数据进行统计分析。计数资料以n(%)表示,行χ2检验;计量资料以±s 表示,组内和组间两两比较分别行配对与独立样本t检验。P<0.05 为具有统计学差异。
2 结果
2.1 临床疗效
观察组治疗总有效率(91.7%)高于对照组(75.0%,P<0.05)(表1)。
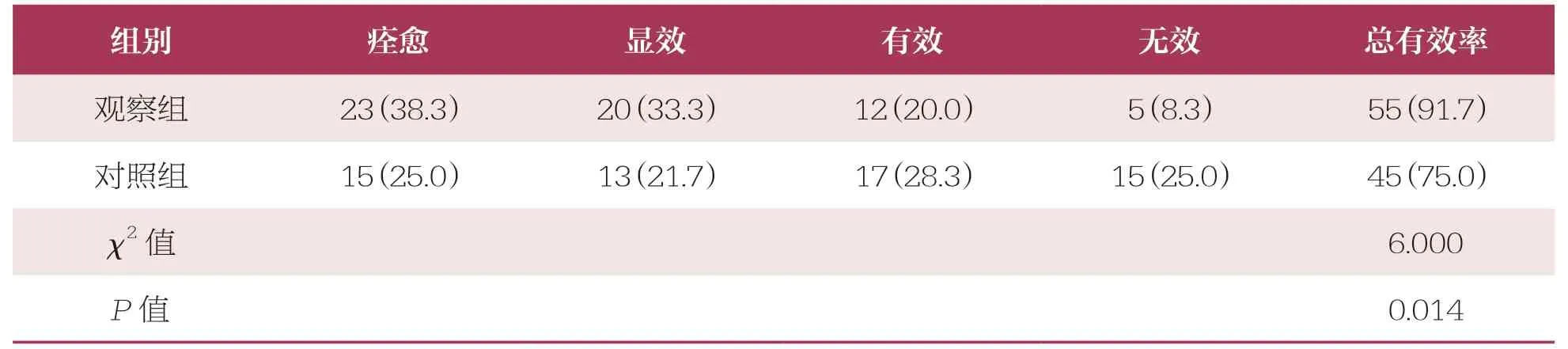
表1 两组临床疗效比较 n=60,n(%)
2.2 典型临床表现改善时间
观察组腹痛、上腹部压痛消失时间和血清淀粉酶复常、肠鸣音恢复时间均短于对照组 (P<0.05)(表2)。
表2 两组典型临床表现改善时间比较 n=60,±s,天
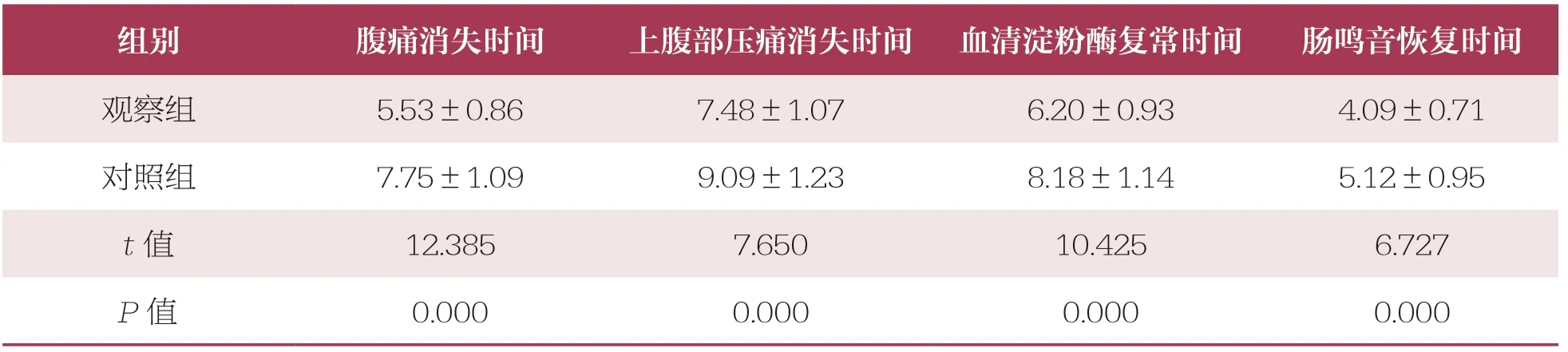
表2 两组典型临床表现改善时间比较 n=60,±s,天
组别腹痛消失时间上腹部压痛消失时间 血清淀粉酶复常时间肠鸣音恢复时间观察组5.53±0.867.48±1.076.20±0.934.09±0.71对照组7.75±1.099.09±1.238.18±1.145.12±0.95 t 值12.3857.65010.4256.727 P 值0.0000.0000.0000.000
2.3 血清TLR4/NF-κB 信号通路下游相关炎症因子水平
治疗后,两组血清TLR4/NF-κB信号通路下游相关炎症因子(IL-8、IL-1β、TNF-α)水平均低于治疗前,且观察组的各项指标水平低于对照组(P<0.05)(表3)。
表3 两组血清TLR4/NF-κB 信号通路下游相关炎症因子水平比较 n=60,±s,ng/L
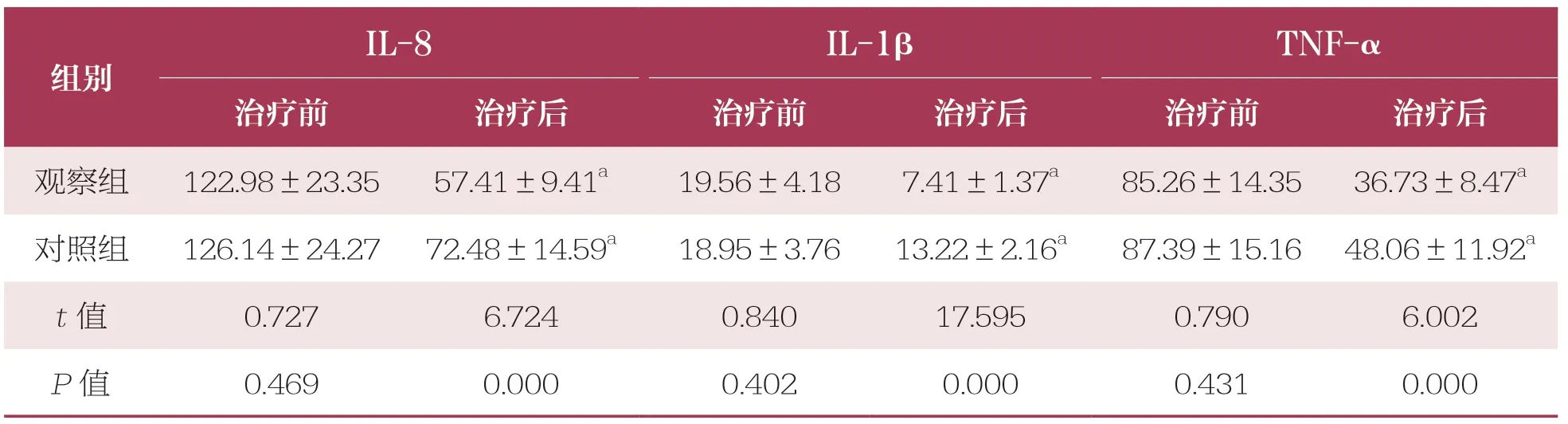
表3 两组血清TLR4/NF-κB 信号通路下游相关炎症因子水平比较 n=60,±s,ng/L
与同组治疗前比较,a:P<0.05。下同
IL-8IL-1βTNF-α治疗前治疗后治疗前治疗后治疗前治疗后观察组122.98±23.3557.41±9.41a19.56±4.187.41±1.37a85.26±14.3536.73±8.47a对照组126.14±24.27 72.48±14.59a18.95±3.7613.22±2.16a87.39±15.16 48.06±11.92a t 值0.7276.7240.84017.5950.7906.002 P 值0.4690.0000.4020.0000.4310.000组别
2.4 外周血Th17、Treg 细胞比例
治疗后,两组外周血Th17、Treg细胞比例及Th17/Treg比值均下降,且观察组低于对照组(P<0.05)(表4)。
表4 两组外周血Th17、Treg 细胞比例比较 n=60,±s

表4 两组外周血Th17、Treg 细胞比例比较 n=60,±s
Th17 细胞比例(%)Treg 细胞比例(%)Th17/Treg 比值治疗前治疗后治疗前治疗后治疗前治疗后观察组2.92±0.760.94±0.23a8.54±2.316.41±1.29a0.35±0.080.15±0.04a对照组2.89±0.701.68±0.47a8.92±2.097.12±2.37a0.33±0.070.24±0.05a t 值0.22510.9540.9452.0381.45710.887 P 值0.8220.0000.3470.0440.1480.000组别
2.5 不良反应发生率
对照组共有4 例(6.7%)患者发生不良反应,包括注射部位疼痛(1 例)、腹泻(1 例)、血糖紊乱(1 例)及一过性转氨酶轻度升高(1 例);观察组共有6 例(10.0%)患者发生不良反应,包括注射部位疼痛(1 例)、血糖紊乱(1 例)、头晕(1 例)、一过性转氨酶轻度升高(1 例)和腹泻(2 例)。两组不良反应发生率比较无统计学差异(P>0.05)。
3 讨论
近年来,急性胰腺炎的发病率呈上升趋势。在我国,胆石症是其主要病因,其次为高甘油三酯血症和过度饮酒,其他包括内镜逆行胰胆管造影术后、感染、遗传等[9]。临床上,部分急性胰腺炎患者会发展为SAP,该疾病具有病情复杂多变、并发症多、治疗难度大、病死率高等特点,现阶段内科治疗仍是SAP 多学科综合治疗的重要组成部分[10]。奥曲肽是一种人工合成的生长抑素八肽衍生物,可通过抑制胰腺分泌、松弛Oddi 括约肌、减轻胰腺组织损伤、降低血液内毒素水平、抑制胆汁分泌、改善低钙血症与酸中毒、抑制胃酸和胃蛋白酶及胃泌素分泌、促进胰腺修复和机化等多重途径达到防治SAP 的作用[11]。乌司他丁系从人尿提取精制而成的一种广谱、高效的蛋白酶抑制剂,能有效抑制胰酶、中性粒细胞弹性蛋白酶活性,抑制溶酶体酶释放并稳定溶酶体膜,还可抑制炎症因子释放和白细胞过度激活、清除氧自由基、改善机体微循环和胰腺血循环,从而阻止全身炎症反应综合征(systemic inflammatory response syndrome,SIRS)的发生,对改善SAP 患者预后具有积极作用[12]。1 项Meta分析[13]显示,奥曲肽联合乌司他丁治疗急性胰腺炎的临床疗效优于单用二者之一或常规治疗。不过,SAP 作为临床常见的急危重症,寻找更佳的治疗药物及方案仍是当前SAP 防治领域的研究热点。
血必净是王今达教授及其团队在“菌毒炎并治”理论和“三证三法”辨证论治基础上,以清代王清任《医林改错》中的活血化瘀名方血府逐瘀汤为基础方研制而成,主要是由5 味药材(红花、丹参、川芎、赤芍、当归)经现代制药工艺精制而成的纯中药注射剂,有扶正固本、清热凉血、溃散毒邪、活血化瘀、通络止痛等功效[14]。现代药理学研究[15]发现,血必净可能通过抑制内源性炎性介质失控性释放、改善免疫功能、改善微循环、清除氧自由基、协助体内内毒素清除、改善酸碱失衡、维持血流动力学稳定、脏器保护等多靶点、多层次及多环节的药理作用,有效切断SAP 病情逐步恶化的路径。1项Meta 分析[16]表明,采取血必净辅助治疗急性胰腺炎能迅速缓解患者症状,缩短住院时间,并可进一步抑制体内IL-6、IL-8、TNF-α等炎症因子的表达水平,临床疗效较佳,提示血必净是临床治疗SAP 的潜在有效药物。本研究中,观察组采取血必净联合乌司他丁及奥曲肽治疗后,其临床治疗总有效率达91.7%,高于单纯联用乌司他丁与奥曲肽治疗的对照组(75.0%),且腹痛、上腹部压痛消失时间和血清淀粉酶复常、肠鸣音恢复时间均短于对照组,同时两组不良反应均少而轻微。该结果提示血必净联合乌司他丁及奥曲肽治疗SAP 是安全、可行且有效的,该治疗方案有望成为SAP 患者临床治疗的新选择。
TLR4/NF-κB 信号通路下游相关炎症因子(如IL-8、IL-1β、TNF-α)在SAP 整个病理生理过程中发挥着关键作用,并对病情的发展与转归有决定性作用[17]。其中,IL-8 是中性粒细胞的趋化因子和诱导物,当机体处于急性胰腺炎的病理状态时,体内单核-巨噬细胞系统被激活,大量释放IL-8 等促炎因子,参与患者肾脏损伤及多器官功能衰竭[18]。IL-1β、TNF-α等炎症因子所启动的级联反应起始于NF-κB 的活化,在急性胰腺炎病理状态下,NF-κB 先被激活,进而上调IL-1β、TNF-α等致炎因子的表达水平,过量合成并释放的IL-1β、TNF-α等炎症因子又反过来以正反馈调节的方式进一步激活NF-κB,致使IL-1β、TNF-α等细胞因子持续、过度释放,形成“瀑布样”级联反应,导致胰腺炎症和腺泡细胞坏死不断加重,并可引发SIRS,同时还会导致多器官病理损害。向珂等[19]研究发现,乌司他丁可能通过抑制TLR4、NF-κB的表达,从而降低血中TNF-α、IL-1β等炎性介质水平,以减轻胰腺组织及全身的损害,从而发挥治疗SAP 的作用。此外,血必净可能通过降低急性胰腺炎模型大鼠血清中TNF-α、IL-1β等炎症因子水平,抑制体内炎症级联反应,进而减轻胰腺组织病理损伤、改善预后[20]。本研究结果显示,观察组的治疗方案对IL-8、IL-1β和TNF-α水平的下调作用较对照组更显著,提示血必净联合乌司他丁及奥曲肽在下调SAP 患者血中TLR4/NF-κB 信号通路下游相关炎症因子表达方面具有协同作用,该联合用药方案更有利于促进患者恢复。
Th17 细胞可分泌促炎因子IL-17,进而诱导IL-6、TNF-α等炎症因子的过量合成和释放,参与SAP 失控性炎症反应的发生发展。Treg 细胞是一类具有强大负性免疫调节功能的T 细胞亚群,当其在血中的含量增高时,可暂时性抑制体内过激的免疫反应、抑制效应细胞的增殖能力与免疫活性,但会使机体处于免疫抑制状态,增加患者感染风险[21]。SAP打破了机体原有的免疫平衡,使机体陷入极度复杂的免疫紊乱状态,随着TLR4 信号通路的激活,外周血Th17、Treg 细胞比例增加且功能活性增强,但以Th17 细胞比例增加更为显著,导致Th17/Treg免疫平衡向Th17 偏移,体内促炎因子合成增加,进而可导致SAP 病情持续加重[22]。陈智峰[23]的研究发现,乌司他丁可有效降低重症脓毒症患者外周血Treg、Th17 细胞比例,改善机体免疫状态,从而利于缓解患者病情;邵敏等[24]指出,脓毒症患者外周血Th17、Treg 细胞比例会增加,且与病情严重程度呈正相关,而血必净能有效降低脓毒症患者外周血Th17、Treg 的异常表达,缩短患者住在重症加强护理病房的时间,并对降低病死率有积极作用。本研究中,观察组的治疗方案对外周血Th17、Treg 细胞比例及Th17/Treg 比值的下调作用较对照组更明显,提示血必净联合乌司他丁及奥曲肽能协同发挥纠正SAP患者外周血Th17/Treg 免疫紊乱的作用。笔者推测这可能是本研究加用血必净治疗SAP 实现增效的重要原因之一,但其具体的作用机制尚需进一步探究。
本研究尚存在一些不足,例如本研究为单中心、小样本、无安慰剂的研究,其代表性有限,研究结果可能存在一定的偏倚,有关结果与结论尚需更大规模的前瞻性、多中心、安慰剂的随机对照临床试验加以验证与补充。
综上所述,血必净联合乌司他丁与奥曲肽治疗SAP 的临床疗效确切,可安全、有效且迅速地缓解患者症状,并可进一步下调血清TLR4/NF-κB 信号通路下游相关炎症因子的表达水平、维持Th17/Treg 免疫平衡,值得临床推广应用。

