外泌体在胃癌远处转移和耐药性中的研究进展
陈舒 张静蕾 荣康 张楠 孙维义
1河南中医药大学(郑州 450046);2中山大学附属第一医院(广州 510080);3郑州大学第五附属医院消化内科(郑州 450052);4河南中医药大学第一附属医院普外科(郑州 450003)
胃癌(GC)是最常见的肿瘤之一,是全球癌症相关死亡的第四大原因[1-2]。目前,中国发病率仍居高不下,每年国内胃癌新发病例占世界总数的46.8%[3]。早期胃癌缺乏特异性体征,大多数病例确诊时已经是晚期,常伴有浸润和远处转移[4]。在转移性(晚期)胃癌患者中,虽首选的治疗方法是手术,但效果较差,往往辅以放化疗治疗[5]。由于耐药性的迅速出现,许多患者在化疗后仍会复发,严重影响患者的预后[6]。外泌体(EXOs)这一癌症细胞间通讯调控剂的发现,为肿瘤的深入研究提供了新的视角[7]。EXOs 是直径范围为30 ~150 nm 的纳米级膜囊泡,其脂质双层结构可保护其内容物免受降解,使其在参与许多生理和病理过程的细胞间通讯中起着至关重要的作用[8-9]。大量研究表明[10-13],EXOs可通过肿瘤微环境(TME)内的细胞间通讯参与胃癌的远处转移和耐药性的发生。在本综述中,我们总结了源自癌细胞和TME的EXOs 影响胃癌转移及化疗耐药的机制(图1),为未来胃癌转移及耐药的治疗提供潜在方向和理论基础。
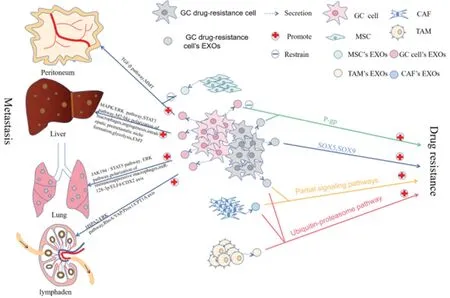
图1 外泌体在GC 远处转移和耐药发生的潜在机制Fig.1 Potential mechanisms of exosomes in distant metastasis and drug resistance in gastric cancer
1 外泌体概述
1989 年,JOHNSTONE[14]将在网织红细胞成熟期间,与转铁蛋白受体释放到细胞外这一过程相关的功能性囊泡定义为外泌体。外泌体起源于细胞膜表面的内吞作用,通过向内“出芽”形成早期内体,后慢慢成熟为晚期内体,其包裹特定的蛋白质,核酸和其他物质以形成多个腔内囊泡(ILVs),这是外泌体的前体。这些囊泡在晚期内体中积累,从而将内体转化为多囊泡体(MVBs)。随后,这些MVBs 或与溶酶体融合,导致被降解;或与质膜融合,导致其内部囊泡的释放,即外泌体的释放[15](图2)。
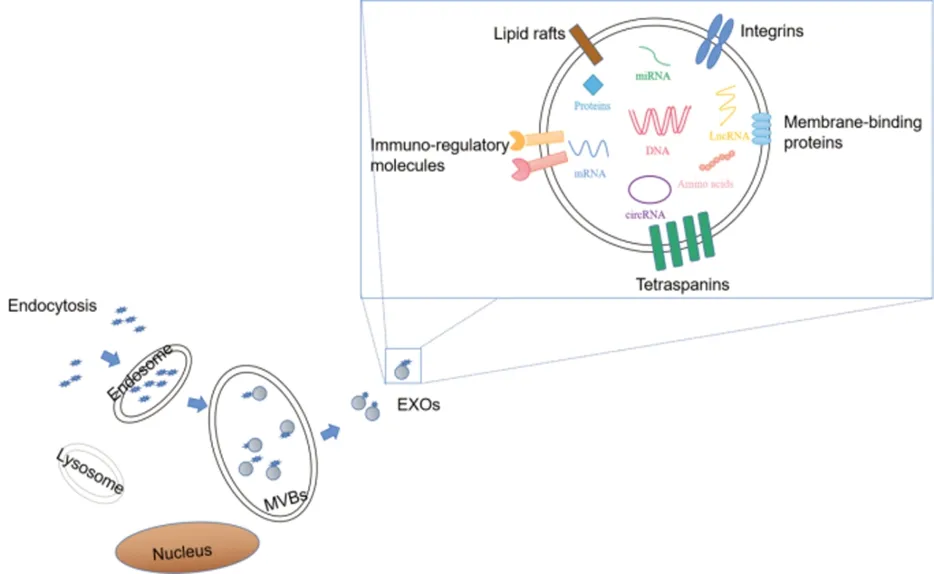
图2 外泌体的结构组成和生物发生的示意图Fig.2 Schematic diagram of the structural composition and biogenesis of exosomes
2 外泌体在胃癌远处转移中的作用
原发性肿瘤发展为远端继发性肿瘤这一过程称为远处转移,一旦确诊就被认为是大多数癌症类型的最后阶段。转移发生的机制非常复杂,与原发肿瘤的分裂、侵袭、逃避免疫监视和组织微环境的调节有关[16]。由于外泌体在转移前生态位(PMN)和癌症转移的形成中起着不可或缺的作用。因此,研究外泌体介导的胃癌远处转移的潜在机制可能为确定胃癌治疗的新治疗靶点提供新的线索。目前,胃癌的远处转移多见于腹膜转移、肝转移、肺转移及淋巴转移(表1)。
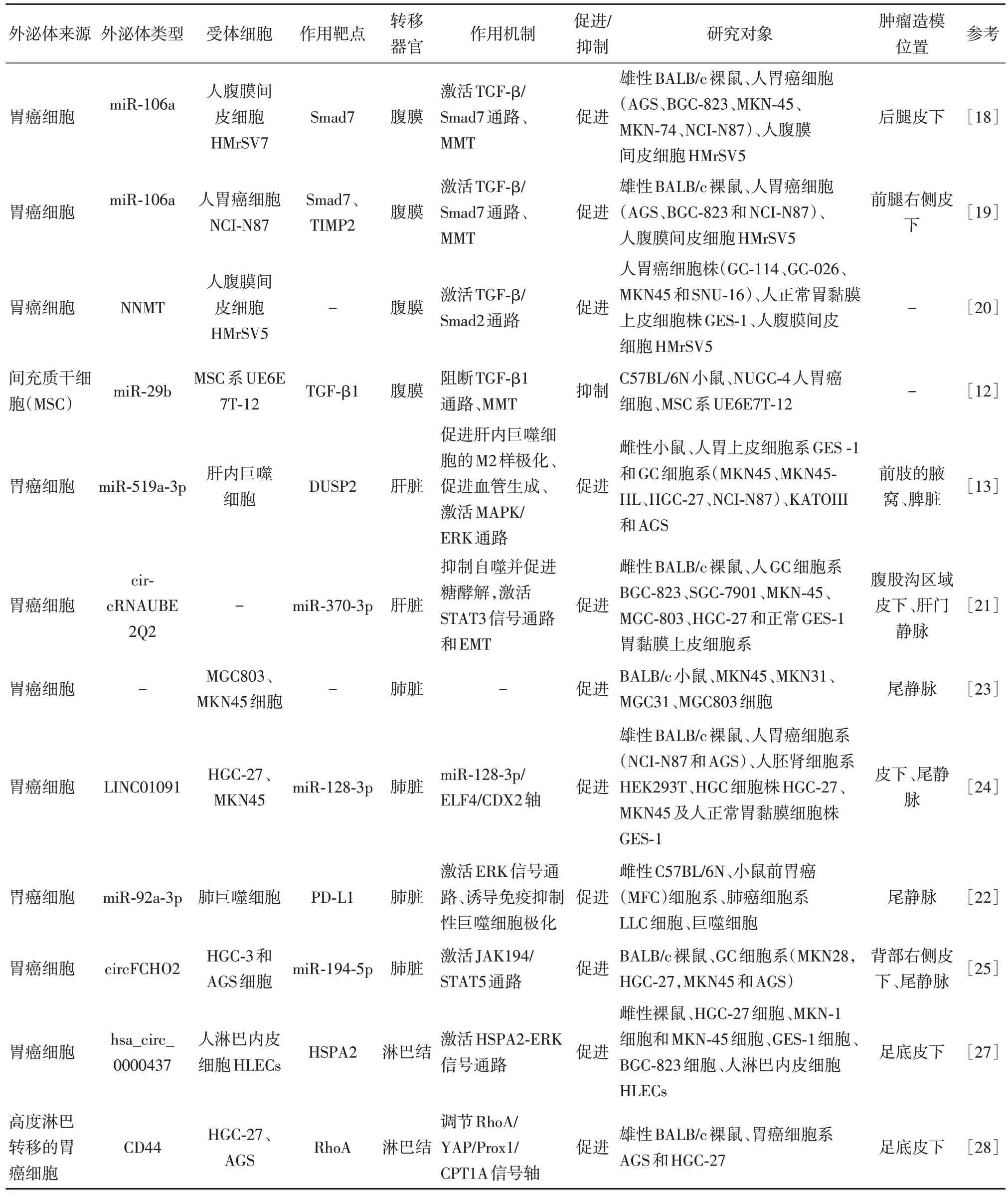
表1 参与胃癌远处转移的外泌体Tab.1 Exosomes involved in distant metastasis of gastric cancer
2.1 胃癌腹膜转移 腹膜转移是胃癌最常见的转移方式,这一过程已被“种子和土壤”理论所描述[17]。外泌体在“种子”和“土壤”之间的细胞间通讯中发挥着关键作用[18]。有研究[18]报道,外泌体miR-106a 通过减轻Smad7 在胃癌腹膜转移期间的抑制作用来激活转化生长因子-β(TGF-β)/Smad通路,并诱导间皮间充质转化(MMT),促进腹膜转移。ZHU 等[19]证实外泌体miR-106a 能够通过靶向Smad7 和金属蛋白酶组织抑制因子2(TIMP2)来激活TGF-β 途径来诱导MMT 促进腹膜转移。研究[20]证明来自GC 细胞的含烟酰胺N-甲基转移酶(NNMT)的外泌体通过TGF-β/Smad2 信号传导促进腹膜转移。KIMURA 等[12]发现来自间充质干细胞(MSC)的外泌体miR-29b 能够阻断TGF-β1 信号抑制MMT,抑制胃癌腹膜转移。
由上发现不同细胞来源的外泌体的作用存在差异:胃癌来源的外泌体在腹膜转移中发挥促进作用,而间充质干细胞则发挥抑制作用。TGF-β信号通路和MMT 在外泌体促进胃癌腹膜转移中充当重要角色:阻断TGF-β信号通路的激活和(或)阻滞MMT 的发生可切断外泌体与胃癌腹膜转移之间的联系,从而发挥抗胃癌腹膜转移的作用。未来开发包裹MMT 阻断药物或TGF-β 抑制剂的外泌体可能在对抗胃癌腹膜转移中具有潜在的治疗价值。
2.2 胃癌肝转移 血液转移是肿瘤细胞扩散到远处的主要途径,来自胃肠道的大部分血液通过门静脉流向肝脏,使肝脏成为胃癌转移最重要的靶器官[13]。QIU 等[13]验证了外泌体miR-519a-3p通过激活肝内巨噬细胞中的双特异性磷酸酶2(DUSP2)-丝裂原活化蛋白激酶(MAPK)/细胞外信号调节激酶(ERK)轴,促进肝转移。YANG 等[21]发现外泌体-环状RNA 泛素接合酶E2Q2(circ UBE2Q2)能够抑制自噬并促进糖酵解,激活信号转导和转录激活因子3(STAT3)信号通路和上皮间质转化(EMT),促进胃癌肝转移。抑制巨噬细胞的M2 极化并削弱肝脏中转移前的生态位可能是治疗胃癌肝转移的新策略。目前外泌体在胃癌肝转移的基础研究较少,还需更深入的研究。
2.3 胃癌肺转移 胃癌细胞通过血液传播导致肺转移瘤的生成,尽管仅有0.5% ~ 16%的胃癌患者在确诊时已发生肺转移,但这些患者的5 年生存率仅为2% ~ 4%[22]。研究[23]显示,脑内RAS 相关蛋白31(RAB31)促进胃癌细胞外泌体释放,从而促进胃癌肺转移的发生。有实验证实[24],长链非编码RNA01091与miR-128-3p结合后会靶向E74样ETS转录因子4(ELF4),ELF4 通过与尾型同源框转录因子-2(CDX2)结合,促进肺转移。GU 等[22]发现GC 衍生的外泌体激活ERK 信号通路,诱导巨噬细胞免疫抑制表型分化,并促进PMN 和肺转移的形成。ZHANG 等[25]验证了外泌体circFCHO2 通过海绵miR-1-3p,激活JANUS 激酶194(JAK194)/STAT5 途径,促进了胃癌肺转移。
胃癌来源的外泌体似乎是通过激活癌症相关信号通路或诱导巨噬细胞的极化和PMN 的形成来促进肺转移的发生。然而,胃癌如何通过重编程巨噬细胞的表型和功能促进肺PMN 的形成尚不清楚。目前只能从外泌体抑制剂、通路抑制剂和抑制巨噬细胞的极化处出手,未来需要更多相关性基础研究来探索胃癌肺转移的相关机制。
2.4 胃癌淋巴结转移 淋巴结转移(LNM)不仅是胃癌较突出的转移途径,也是胃癌患者疾病进展和预后不良最突出标志[26]。阐明LNM 背后的机制才能改善胃癌的预防和治疗效果。研究[27]发现,外泌体hsa_circ_0000437 通过热休克蛋白A2(HSPA2)-ERK 信号通路促进了LNM。WANG 等[28]用淋巴转移性胃癌细胞外泌体通过调节Ras 同源家族成员A(RhoA)/yes 相关蛋白(YAP)/prospero 同源盒蛋白-1(Prox1)/肉碱棕榈酰转移酶1A(CPT1A)信号轴介导外泌体传递,导致腘窝淋巴结的转移。外泌体在胃癌淋巴结转移中的基础研究过少,目前其发生的具体机制尚不明确,因胃癌来源的外泌体可以促进淋巴结转移,或许使用外泌体拮抗剂能达到抗LNM 的效果。
3 外泌体在胃癌化疗耐药中的作用
许多患者在治疗一段时间后,会出现药物的有效性和效力降低,从而导致癌症复发,这是癌症治疗中最关键的障碍之一,也是患者治疗失败的常见原因[29]。作为新型细胞间通信系统的一部分,外泌体携带和传递调节细胞生理状态的信号分子,在胃癌化疗耐药中发挥重要作用[30]。由外泌体介导的胃癌化疗耐药机制总结如下(表2)。
3.1 泛素-蛋白酶体途径参与外泌体促化疗耐药过程 泛素-蛋白酶体途径介导着代谢酶和信号通路的激活和降解,并影响免疫检查点的激活和肿瘤微环境的变化[31],因此是研究和开发癌症治疗新策略的关键靶标。JING 等[32]揭示了顺铂(DDP)耐药的胃癌细胞来源的外泌体miR-769-5p 通过靶向半胱天冬酶9(CASP9)和泛素-蛋白酶体途径的p53 的降解并抑制细胞凋亡,促进耐药性。LIN等[33]发现肿瘤相关巨噬细胞(TAM)来源的外泌体LncRNA 结直肠肿瘤差异表达(CRNDE)促进泛素连接酶NEDD4-1(NEDD4-1)介导的磷酸酶及张力蛋白同源蛋白(PTEN)泛素化,诱导DDP 抗性。研究发现[34]泛素特异性蛋白酶 7(USP7)通过去泛素化稳定癌症相关成纤维细胞(CAF)中的异质核糖核蛋白A1(hnRNPA1),从而增强CAF 分泌miR-522,外泌体miR-522 通过花生四烯酸脂氧合酶15(ALOX15)抑制铁死亡并促进胃癌细胞对DDP 和紫杉醇(PTX)的抵抗。
泛素系统是复杂的,多方面的,并且受到多种酶的严格调节,靶向泛素系统的或许是治疗癌症耐药的一种有前途的方法。由上总结发现外泌体与泛素系统之间有一定的联系,外泌体可通过蛋白酶泛素化和(或)去泛素化达成促胃癌耐药的目的,但泛素系统和外泌体之间的互相调节机制仍有待阐明。未来需要开展临床前实验和临床试验研究外泌体抑制剂的疗效、副作用的大小,以及基础实验研究完善胃癌耐药中的泛素系统机制。
3.2 SOX 家族参与外泌体促化疗耐药过程 性别决定区相关高迁移率族盒蛋白(SOX)是一类含有高度保守的高迁移率族结构域的转录因子家族,其部分家族成员在胃癌中同时充当肿瘤抑制因子和癌基因[35]。LIANG 等[36]发现来源于胃癌耐药细胞的外泌体circ-低密度脂蛋白受体A 类含结构域3(LDLRAD3)通过靶向抑制miR-5 上调SOX5 的表达,促进胃癌耐药及肿瘤生长。有研究报道[37],来自胃癌耐药细胞的外泌体circ_0032821通过负调控miR-515-5p 上调SOX9 的表达,加速了奥沙利铂(L-OHP)敏感胃癌细胞的L-OHP 耐药性。由上可以猜想来源于胃癌耐药细胞的外泌体发挥上调SOX 家族成员的表达,即SOX 家族成员在胃癌耐药中充当癌基因,导致耐药发生。关于SOX 家族在胃癌化疗耐药分子机制中的功能和机制的研究仍处于早期阶段,未来不仅要寻找并识别更多肿瘤耐药与外泌体之间的靶点,还需进一步的科研工作来阐明外泌体、SOX 与胃癌耐药的相互作用,为下一代抗癌耐药疗法提供机会。
3.3 P-糖蛋白参与外泌体在化疗耐药发生的过程 P 糖蛋白(P-gp)是膜中的外排转运蛋白,是ATP结合盒(ABC)转运蛋白的组成部分。P-gp大量存在于癌细胞中,除了阻断化疗药物进入细胞外,还负责产生转运蛋白介导的对肿瘤细胞治疗的耐药性[38]。相关研究[39]报道,来源于耐药细胞的外泌体通过促进P-gp的过表达,致使胃癌化学耐药的发生。研究[40]显示,来源于胃癌细胞的外泌体miR-107 通过靶向高迁移率族蛋白A2(HMGA2)和抑制HMGA2/mTOR/P-gp 途径的激活,从而逆转SGC-7901/5-FU 细胞耐药性。由上发现,来源于耐药细胞的外泌体可以上调受体细胞的P-gp 的表达水平,从而增加化疗药物排泄出细胞,降低受体细胞中化疗药物的浓度,进而促进胃癌细胞的耐药;而胃癌敏感细胞来源的外泌体则下调耐药细胞中P-gp 的水平,可以逆转耐药细胞的耐药性。那么未来可以开发针对P-gp 的拮抗剂,从而达到逆转耐药的效果,并且筛选敏感细胞的外泌体,与P-gp的拮抗剂共同使用,可能会达到事半功倍的疗效。
3.4 信号通路参与外泌体在化疗耐药发生的过程 信号通路在耐药性的发展中起着重要作用,化疗药物靶标的突变或所涉及的信号通路成分的改变会降低药物疗效,使肿瘤对化疗药物产生耐药性[41]。有报道[42]称,CAF的外泌体白细胞介素-8(IL-8)通过激活GC 中的PI3K/AKT 途径诱导奥沙利铂耐药。依旧是胃癌耐药细胞分泌的外泌体阻碍了miR-330-3p 与三重基序蛋白14(TRIM14)的结合,TRIM14 可以引起Wnt/β-连环蛋白信号通路的激活,最终使GC 细胞的L-OHP 抗性得到增强[11]。外泌体通过激活相关信号通路导致耐药性的发生,例如PI3K/Akt、Wnt/β-连环蛋白等通路会在外泌体的作用下被激活,降低CRC 治疗敏感性,促进耐药性。信号通路在癌症发展及耐药中的作用及机制在过去十年中有了显著的发展,靶向肿瘤相关信号通路被认为是抗癌抗耐药的一个关键研究领域。在未来的研究中,通路拮抗剂与协同外泌体抑制剂联合使用可能会提高其化疗敏感性。
4 小结
目前,虽然胃癌的全身治疗,包括化疗,靶向治疗和免疫治疗,在过去几年中取得了显著发展[43],但远处转移和耐药性的出现已成为影响胃癌患者预后的主要问题。本文总结了外泌体及其内容物在治疗胃癌远处转移及化疗耐药方面的潜力,外泌体可促进抗肿瘤药物和RNA 的递送,因此有望应用于胃癌治疗。而且,外泌体在肿瘤进展、远处转移、化疗耐药中的作用也提示其在靶向治疗、抗肿瘤治疗和逆转耐药方面的可能性。外泌体在GC 转移及耐药中的应用的进一步研究应重点关注以下几个方面:(1)获得纯度更高的外泌体以及如何高效地将抗肿瘤药物或基因装载到外泌体中;(2)外泌体拮抗剂在癌症治疗中的最佳剂量、药物分布、治疗常规和生物学安全性;(3)将外泌体相关研究的基础性抗远处转移试验较少,相关机制研究还需更大规模、多中心的研究实验。
【Author contributions】CHEN Shu collected the literature and wrote the article.ZHANG Jinglei,RONG Kang collected and organized the literature.ZHANG Nan,SUN Weiyi formulated the article ideas and reviewed the article.All authors read and approved the final manuscript as submitted.
【Conflict of interest】The authors declare no conflict of interest.

