CYP3A5*3基因多态性对他克莫司治疗膜性肾病血药浓度及临床疗效的影响
许宏磊,徐炳欣*,王申伟,沈志伟,赵 艳,王 琼
(1 河南科技大学附属许昌市中心医院,许昌 461000;2 许昌市分子医学重点实验室,许昌 461000)
膜性肾病(membranous nephropathy,MN)是诱发成人肾病综合征最常见的病理类型。近年来的发病率逐年上升,且发病年龄有年轻化的趋势[1]。该病具体发病机制目前仍不明确,多数学者认为其与免疫性疾病有关[2-3]。目前,他克莫司作为强效免疫抑制剂,常用于MN的治疗。然而,他克莫司治疗指数较低,治疗MN的临床疗效有较大个体差异,在同一治疗方案下不同患者治疗后的有效性和安全性均有所不同[4]。因此,探索影响他克莫司临床疗效的影响因素对于MN患者疾病的治疗具有积极意义。既往研究表明[5-7],CYP3A5*3基因多态性对肾脏、心脏、肝脏移植术后患者应用他克莫司有相关影响,但CYP3A5*3基因多态性是否会影响MN患者应用他克莫司的血药浓度及临床疗效,目前尚缺少临床研究证据。基于此,本研究将探讨CYP3A5*3基因多态性对MN患者应用他克莫司治疗后血药浓度及临床疗效的影响,以期为MN患者的个体化药物治疗提供临床研究证据。
1 资料与方法
1.1 一般资料
将2016年8月~2019年7月许昌市中心医院肾内科收治的105例MN患者为研究对象。其中,6例患者中途退出,1例患者转院治疗,4例患者出院后失访,共计脱落11例,最终共纳入患者94例。记录患者年龄、性别等临床资料,告知患者检测CYP3A5*3基因多态性的临床意义。本研究经本院伦理委员会批准,所有参试者均签署知情同意书。
纳入标准:① 患者年龄在18~70岁,性别不限。② 经病理检查确诊为MN患者。③ 初始治疗时患者血清肌酐水平在正常范围内。④ 自起病以来,未曾使用过糖皮质激素、环磷酰胺、他克莫司、五酯软胶囊等药物者。
排除标准:① 继发性MN患者。② 不能耐受激素及免疫抑制剂治疗者。③ 合并糖尿病者。④ 孕妇、哺乳期妇女。⑤ 对他克莫司药物过敏者。⑥ 依从性差,不能按照要求服药者。⑦ 合并恶性肿瘤、急性冠脉综合征等严重疾病者。
1.2 研究方法
给药方法:患者入组后药物治疗方案为他克莫司联合激素常规治疗。其中他克莫司胶囊(普乐可复,Astellas Pharma Co.Ltd.,注册证号H20150197,规格1 mg)初始给药方案为1粒/次,bid,早餐和晚餐前1 h内给药后,根据血药浓度监测结果调整给药剂量;醋酸泼尼松片(上海上药信谊药厂有限公司,国药准字H31020675,规格5 mg)起始剂量为口服给药0.5 mg/(kg·d),2个月后根据患者复查结果减量,每1~2个月减量5 mg,减至10 mg/d维持给药。患者均给予五酯胶囊、他汀类药物及抗血小板药物等治疗。30天为一个疗程,连续治疗6个疗程。
基因型检测方法与分组:采用荧光染色原位杂交技术检测入组患者CYP3A5*3基因多态性,并依据检测结果将患者分为GG、GA和AA 3组。具体检测过程为:用EDTAK2抗凝的采血管取患者空腹静脉血2 ml,取全血100 μl置于900 μl预处理液中(10×NH4Cl稀释10倍,北京华夏时代基因科技发展有限公司),涡旋震荡10 s,静置5 min后,3000 r/min离心5 min,去除上清液,留取下层白细胞备用。取耀金染试剂(北京华夏时代基因科技发展有限公司)30 μl加入白细胞中得到白细胞悬液。取白细胞悬液2 μl加入到CYP3A5*3基因(rs776746)耀金分试剂(北京华夏时代基因科技发展有限公司),置入TL998A荧光检测仪(西安天隆科技有限公司),其结果由Microseq软件分析和自动判读,给出CYP3A5*3基因多态性检测结果。
他克莫司血药浓度检测采用均相酶免疫分析法测定,于患者规律服药至少7天后检测他克莫司血药浓度谷值(C0,在下一次给药前0.5 h抽血)。他克莫司检测试剂[西门子医学诊断产品(上海)有限公司,国食药监械(进)字2009第2400651号]。他克莫司剂量调整血药浓度以MN患者体重校正他克莫司日剂量(D),并以C0计算剂量调整血药浓度(C0/D)mg/(ml·d)。高密度脂蛋白、低密度脂蛋白、三酰甘油、血糖、总胆固醇、肌酐等生化指标应用,采用Cobas8000型全自动生化免疫分析仪(德国罗氏诊断有限公司)检测,操作严格按照对应试剂盒的使用说明书进行。
1.3 评价标准
有效性评价指标包括:完全缓解、部分缓解和治疗无效[8]。其中,完全缓解:① 患者尿蛋白检测结果转阴。② 患者24 h尿蛋白定量<0.3 g。③ 患者血清白蛋白≥35 g/L。④ 患者血清肌酐<140 μmol/L。部分缓解:① 患者24 h尿蛋白定量比入组时有所降低,降低幅度>50%。② 患者血清白蛋白≥30 g/L。③ 患者血清肌酐<140 μmol/L。治疗无效:① 患者24 h尿蛋白降低幅度<50%或较治疗前升高。② 患者血清白蛋白<30 g/L或较治疗前更低。治疗总有效率(%)=(完全缓解例数+部分缓解例数)/总例数。记录患者在治疗期间所发生的全部药物不良反应,用于评价治疗的安全性。其中药物不良反应发生率的计算方式为:药物不良反应发生率(%)=不良反应发生例数/总例数。
1.4 统计学方法
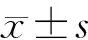
2 结果
2.1 CYP3A5*3基因类型的Hardy-Weinberg遗传平衡
94例患者检出CYP3A5*3基因:GG组45例、GA组32例、AA组17例。CYP3A5*3各基因型的实测值与理论值无统计学差异,符合Hardy-Weinberg遗传平衡(χ2=2.904,P=0.234),说明本研究纳入的样本具有群体代表性。见表1。
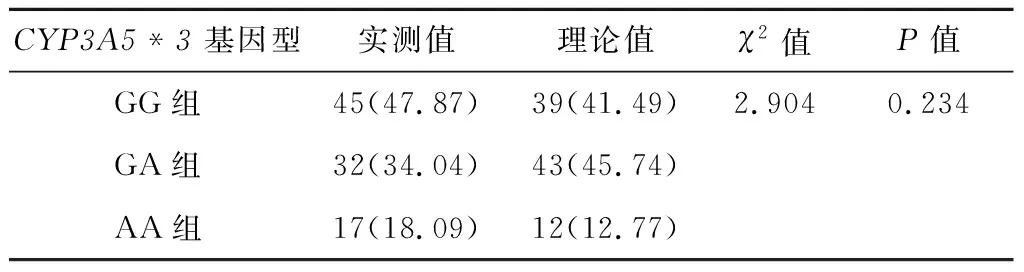
表1 CYP3A5*3基因类型的Hardy-Weinberg遗传平衡 n(%)
2.2 3组一般资料比较
完成研究的94例患者,GG、GA和AA 3组患者例数及所占的比例分别为45例(47.87%)、32例(34.04%)和17例(18.09%)。GG组:男性30例,女性15例;年龄41~68岁,平均年龄(53.21±12.74)岁;GA组:男性23例,女性9例;年龄36~65岁,平均年龄(56.58±14.17)岁;AA组:男性9例,女性8例:年龄38~70岁,平均年龄(51.26±13.58)岁。3组基线资料相比较,无统计学差异(P>0.05)。见表2。
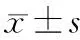
表2 3组一般资料比较
2.3 3组他克莫司C0及C0/D差异
治疗1周后,GG组患者他克莫司C0为(6.42±3.31) ng/ml,高于GA组(5.22±2.76) ng/ml和AA组(4.14±2.57) ng/ml。单因素方差分析显示,不同基因型患者间他克莫司C0比较,具有统计学差异(F=3.924,P=0.022);两两比较经Bonferroni校正,GG组患者他克莫司C0高于AA组,具有统计学差异(P=0.014)。以患者每天他克莫司给药总剂量除以体重,得到D;3组他克莫司D和C0/D数据不符合正态分布,经kruskal-Wallis检验显示,3组他克莫司D无统计学差异(χ2=2.524,P=0.081);3组他克莫司C0/D具有统计学差异(χ2=4.803,P=0.015),两两比较经Bonferroni校正,GG组与AA组C0/D具有统计学差异(P=0.009)。见表3。
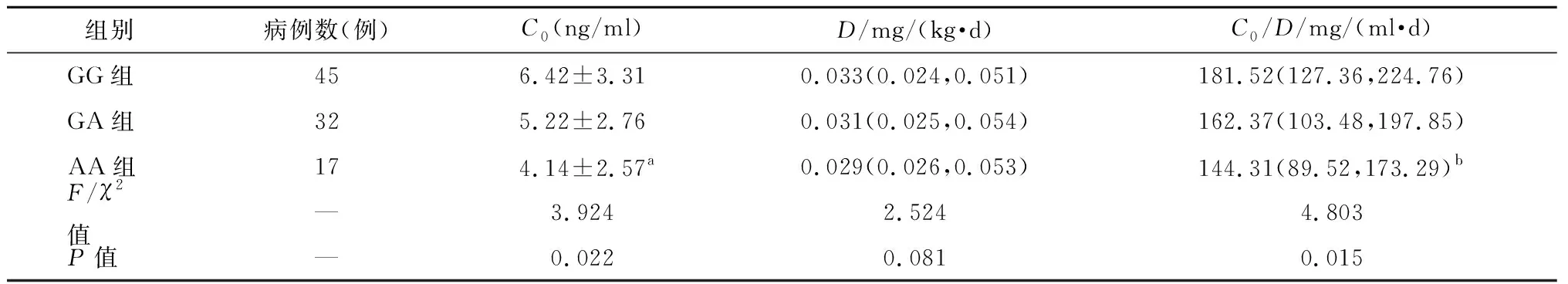
表3 3组他克莫司C0及C0/D的差异
2.4 3组治疗有效率的差异
经过6个月的治疗,GG组患者治疗有效率为34例(75.56%)、GA组治疗有效率为22例(68.75%)、AA组治疗有效率为11例(64.71%)。GG组患者治疗有效率高于GA和AA组,但无统计学差异(χ2=0.861,P=0.650)。见表4。
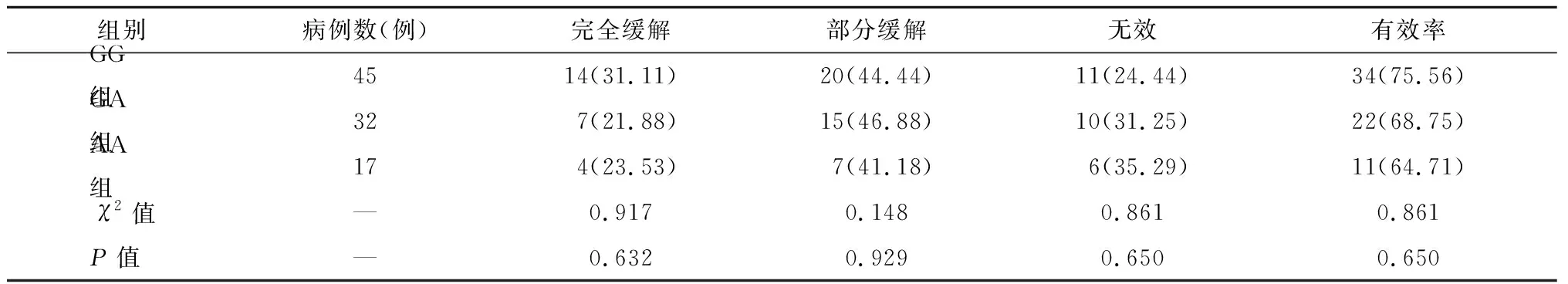
表4 3组治疗有效率比较 n(%)
2.5 3组药品不良反应发生情况
治疗期间,3组患者所发生的药物不良反应主要有胃肠道反应(恶心、腹泻、消化不良等)、空腹血糖受损、血尿酸水平升高、肝酶异常和肌肉震颤。按照国家药物不良反应分级,3组患者所发生的药物不良反应均为一般药物不良反应,经对症处理后均得到缓解或者消失。A组患者肝酶异常发生率和空腹血糖受损发生率均大于B和C组,具有统计学差异(P<0.05);3组其他药物不良反应发生率及药物不良反应总发生率无统计学差异(P>0.05)。见表5。
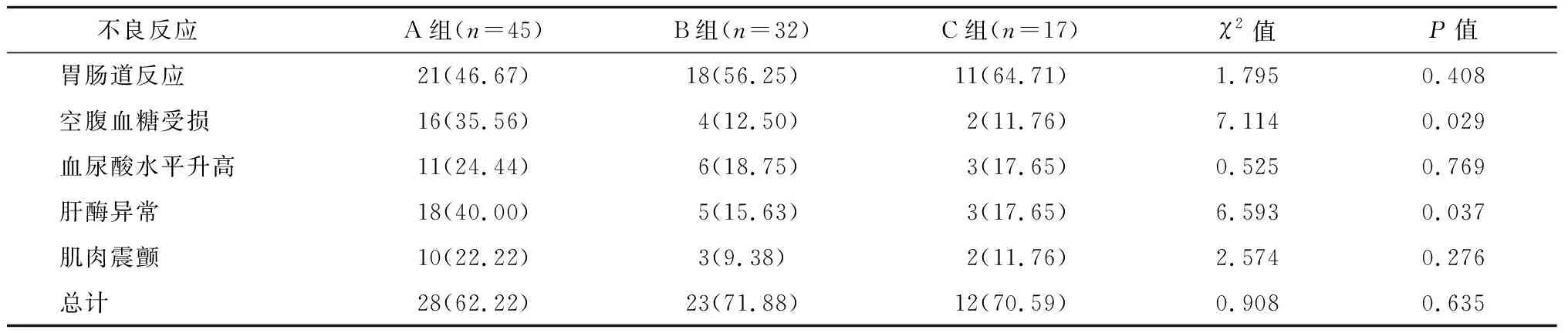
表5 3组药物不良反应发生率比较 n(%)
3 讨论
本研究中患者他克莫司起始给药剂量为每天 2 mg,略低于改善全球肾脏病预后组织推荐的给药剂量[9],主要原因在于所有患者均联合给予五酯胶囊。研究显示[10],五酯胶囊可通过抑制CYP3A5酶的活性提升他克莫司的血药浓度,MN患者联用五酯胶囊后可通过减少他克莫司用药量降低经济负担[11]。
本研究中采用血药浓度监测调整他克莫司的维持给药剂量,主要因为他克莫司治疗指数低且个体差异大[12]。研究考察了CYP3A5*3基因多态性对他克莫司血药浓度的影响,结果显示,在同一给药剂量下不同基因型患者的血药浓度存在差异,且GG组患者血药浓度高于AA组。为排除患者体重、给药剂量对血药浓度的影响,进一步研究考察了3组患者他克莫司调整血药浓度的差异。结果显示,3组他克莫司调整血药浓度也存在差异,且GG组患者高于AA组。这表明CYP3A5*3基因多态性影响他克莫司的血药浓度。研究显示[5,13],他克莫司血药浓度影响因素较多,以遗传因素、患者的疾病状态、饮食结构以及药物相互作用为主,其中以遗传因素的影响更为重要,这与魏传梅等[14]的研究结论相符。
MN的治疗是一个较为长期的过程,在用药前明确不同基因类型患者药物不良反应的发生情况,对于保障患者用药安全有重要的意义。肾毒性是他克莫司常见的药物不良反应,血清肌酐和肾小球滤过率是监测患者肾功能常用的指标。本研究采用血清肌酐监测入组患者治疗过程中肾功能的变化,治疗过程中3组血清肌酐水平在正常范围内。本研究考察了不同CYP3A5*3基因型患者应用他克莫司后药物不良反应发生率的差异。结果显示GG组患者空腹血糖受损和肝酶异常发生率高于GA和AA组患者,表明CYP3A5*3基因多态性对他克莫司不良反应的发生情况有影响。提示临床为了保障治疗安全,在患者应用他克莫司前应检测CYP3A5*3基因型并依据检测结果个体化监测药物不良反应的发生情况。临床应加强GG组患者用药期间的患者教育,患者自身也应加强血糖和肝功能监测。有研究指出[15],他克莫司导致血糖异常的机制在于他克莫司可通过血药浓度依赖的方式抑制胰岛素分泌,进而影响患者血糖水平,且这种抑制程度与血药浓度的高低有关系。GG组患者对他克莫司代谢减慢,可能是空腹血糖发生率高的原因所在。
本研究中3组患者经过6个月的治疗,GG组患者治疗有效率为75.56%,高于GA(68.75%)和AA组(64.71%),但无统计学差异。既往研究显示[16],他克莫司血药浓度是影响他克莫司疗效的关键因素。但本研究中3组有效率无统计学差异,考虑其可能原因为患者在治疗过程中均通过血药浓度监测结果调整他克莫司的给药剂量,同时研究时间相对较短。CYP3A5*3基因多态性对他克莫司治疗MN有效性的影响有待进一步研究。
综上所述,CYP3A5*3基因多态性对MN患者应用他克莫司治疗后的血药浓度和不良反应的发生情况有影响,检测CYP3A5*3基因多态性对提升MN患者治疗的安全性有一定价值。但本研究是单中心研究,纳入样本量较少,这可能会导致研究结论有所偏倚,因此本研究结论有待多中心更大样本量的研究予以证实。

