串联型颈动脉狭窄的血流动力学模拟分析
曹俊杰, 姚志超, 霍桂军, 刘占鳌, 汤 尧, 黄 剑, 周大勇, 沈利明
脑卒中是全球范围内的第二位死亡原因,也是我国居民致残和致死的首要病因, 其中缺血性卒中约占脑卒中发病率的70%, 颈动脉狭窄则占缺血性卒中病因的15%~20%[1-4]。 目前,治疗颈动脉狭窄常用的手术方式为颈动脉支架植入术(carotid artery stenting,CAS) 和颈动脉内膜剥脱术(carotid endarterectomy,CEA),CEA 已被认为是治疗颈动脉狭窄的金标准[5-6]。
串联型颈动脉狭窄(tandem carotid artery stenosis,TCAS)是指在颈动脉不同水平的同时狭窄,发生率为2.1%~5.0%[7-8]。虽然发生率相对较低,但形态学表现复杂,且多伴随复杂的血流动力学状态,既往治疗颈动脉狭窄适用的单纯CEA 或CAS 术往往无法达到令人满意的改善脑灌注、 减少脑卒中的作用[9-10]。 因此,如何有效处理TCAS 的两处不同狭窄,是临床治疗面临的难题与挑战。
近年来, 基于影像学技术与计算流体力学(computational fluid dynamic,CFD)的不断发展,CFD技术在血管病变模拟及手术疗效评价方面取得了诸多进展,已广泛应用于门静脉系统、心血管系统及主动脉系统[11],但尚缺乏关于TCAS 的CFD 模拟研究。 本研究招募了1 例颈内动脉和颈总动脉串联狭窄的患者,通过CTA 数据重建了三维颈动脉分叉模型并进行血流动力学模拟,探讨其发生发展过程及不同手术方式对血流动力学的影响。
1 材料与方法
1.1 数据采集
选取1 例2022 年就诊于南京医科大学姑苏学院/苏州市立医院(本部)且颈动脉CTA 确认存在颈总动脉(common carotid artery,CCA)和颈内动脉(internal carotid artery,ICA)串联狭窄患者。男,76 岁,头晕、乏力1 月余,有吸烟史,无外伤史、手术史,无高血压、糖尿病、冠心病、脑卒中等慢性病史。 本研究经医院伦理委员会批准,并签署知情同意书。
1.2 模型构建
将DICOM 格式CT 数据导入MIMICS 软件(MATERIALISE 公司,比利时)中,使用阈值分割、区域增长、 冗余删除等方法重建颈动脉分叉处模型,输出STL 格式文件后导入3-MATIC(MATERIALISE公司,比利时)进行表面光滑、模型切割等再处理,再以各血管中心线为基准裁剪,得到垂直于中心线的出入口平面[12]。
患者特异性颈动脉分叉的重建几何结构见图1。在CCA 近分叉处存在一个狭窄, 在ICA 存在2 个狭窄并被一个小突起分开。 由于ICA 的2 个狭窄彼此接近,本研究将其合并视为1 个狭窄,建立真实模型即模型1。 狭窄程度使用北美症状性颈动脉内膜剥脱术中的方法进行计算。 建立真实模型后,通过去除CCA 狭窄建立模型2, 去除ICA 狭窄建立模型3,两处狭窄均去除建立模型4,这3 个假定模型用以模拟不同的手术处理方式。 模型4 也可认为是健康者模型。
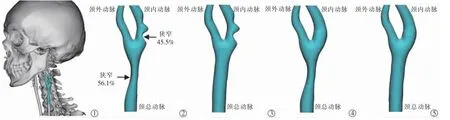
图1 颈动脉模型构建
1.3 CFD 计算
网格划分: 使用3-MATIC 中Remesh 功能画出体表网格并进行质量修整, 将保存的STL 文件导入FLUENT 软件(ANSYS 公司,美国)中进行网格划分,为保证计算精度,边界层采用6 层加密,增长率1.2,网格类型为Poly-Hexcore 网格并进行独立验证,满足精度要求,得出面网格、体网格及边界层网格,见图2。4 个模型生成网格数均为20~30 万。
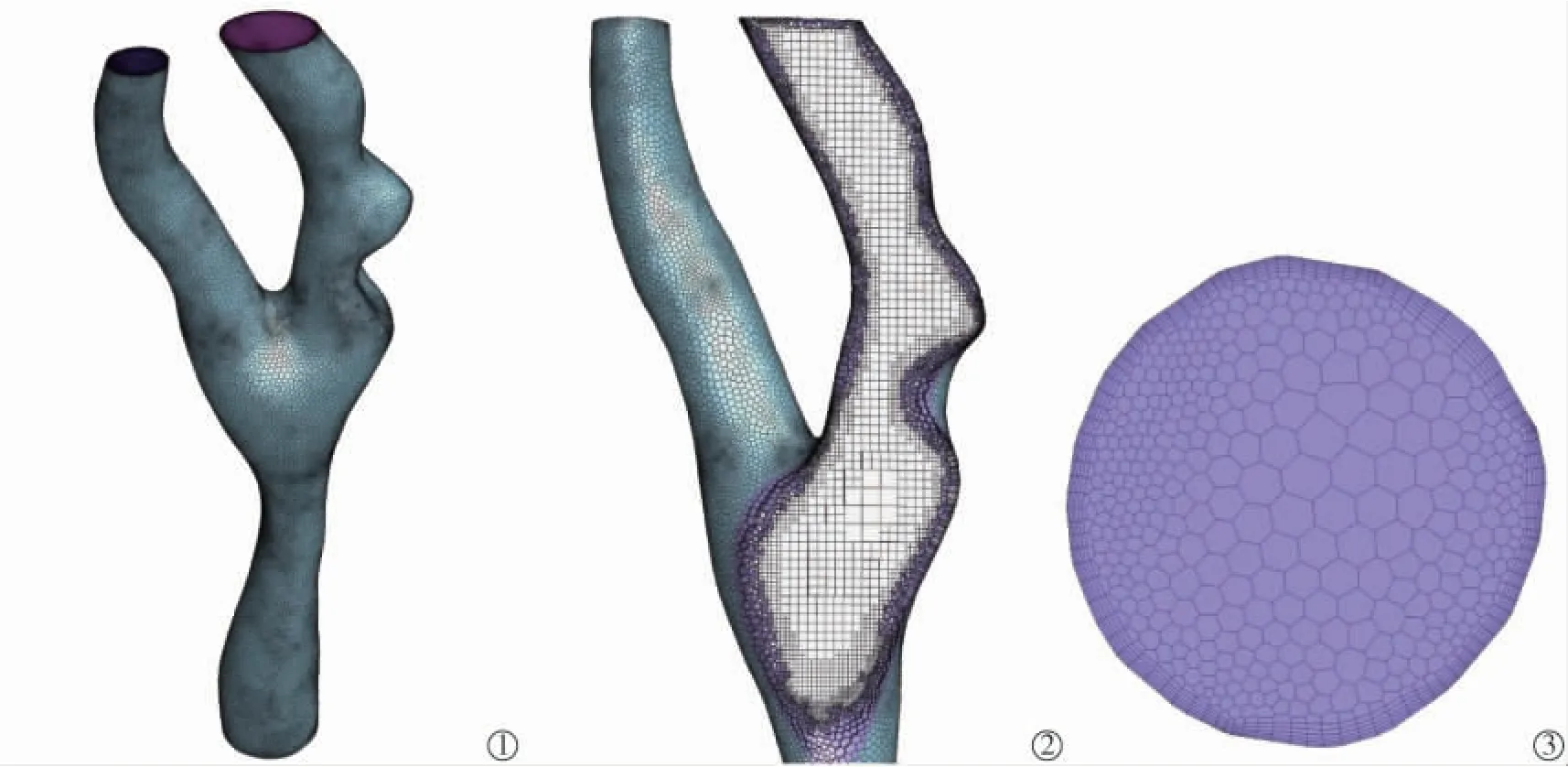
图2 网格化
参数设置:根据相关文献,血液被设定为绝热、均匀、不可压缩的牛顿力学流体,密度设定为1 060 kg/m3、粘度系数设定为0.003 5 Pa·s[13]。 由于血管内压力较小,计算雷诺数均RE<2 300,故流动方式定义为层流[14]。
边界条件:为了真实反映颈动脉内血流情况,采用生理脉动流动条件, 将速度入口和压力出口作为边界条件。CCA 入口处速度曲线及ICA、颈外动脉(external carotid artery,ECA)出口处压力曲线[15-17]见图3。 血管壁为不可压缩的刚性壁,不考虑重力加速度的影响。
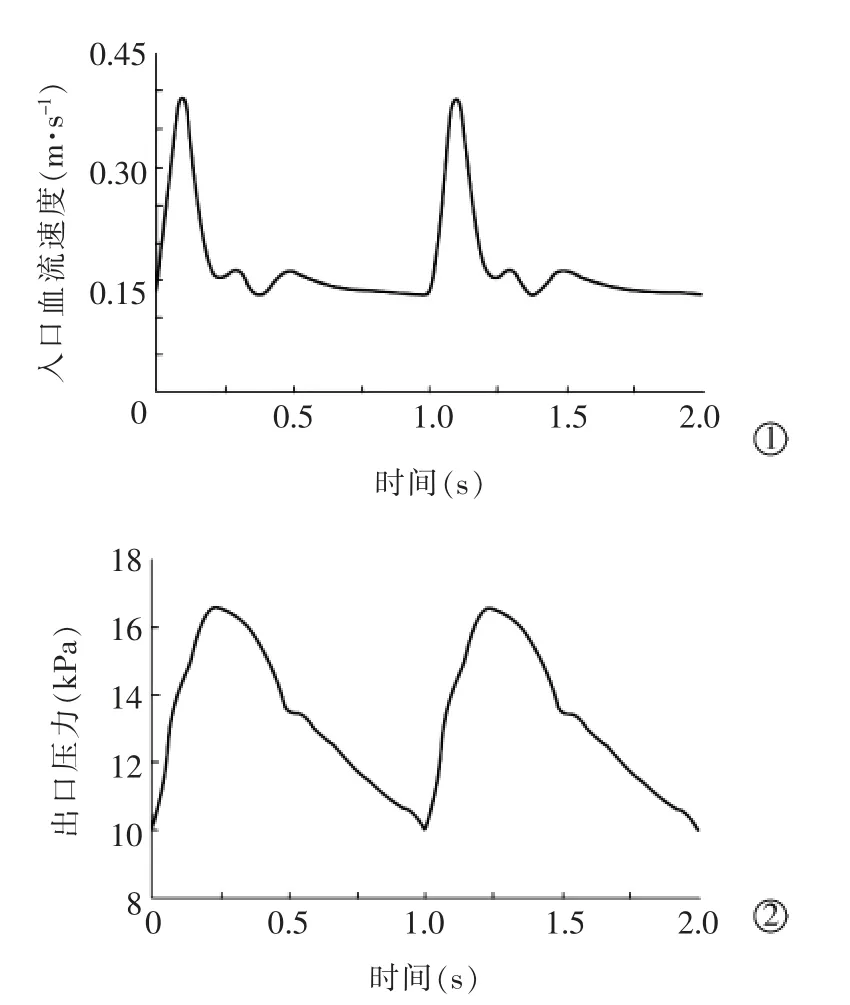
图3 出入口条件
计算设置: 使用FLUENT 求解, 压力-速度耦合采用SIMPLE 算法, 计算收敛条件残差标准设置为10-4。迭代次数设置1 000 次,时间步长0.002 s,总时长2 s(2 个心动周期)。 为减少误差,取第2 个心动周期中计算结果数据用于后处理及分析。
结果分析: 使用后处理软件CFD-post(ANSYS公司,美国)进行结果可视化及分析,除流量、流速、壁面剪切应力(wall shear stress,WSS)等常规参数外,使用了WSS 相关的衍生参数,如时间平均壁面剪切应力(time-average wall shear stress,TaWSS)、剪切振荡系数(oscillatory shear index,OSI)和相对停留时间(relative residence time,RRT)。 TaWSS:为整个心动周期内WSS 的时间加权平均值,反映了单位时间内血流向局部切线平面运动时血管壁产生的摩擦力[18]。OSI:描述了局部WSS 在整个心动周期内方向改变的大小,用于衡量WSS 在流场中震荡水平的强弱[19]。 RRT:结合了TaWSS 及OSI,量化血液处于低剪切、高振荡状态的程度[20]。
为评估整个心动周期过程中4 个颈动脉分叉模型血流动力学改变情况,选取心动周期中T1、T2、T3、T4 共4 个不同时刻及a、b、c、d、e 共5 个不同截面进行分析,见图4。
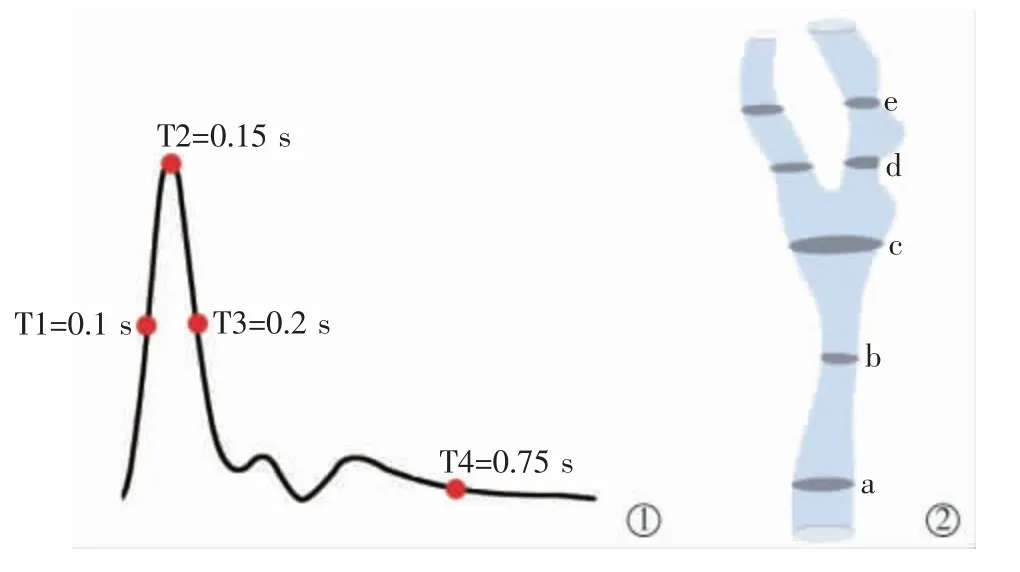
图4 心动周期内时间节点与截面选取
2 结果
2.1 血液流量
真实模型与假定模型的速度入口、压力出口边界条件均相同。 因此,当流体域几何形状基于不同狭窄条件而发生改变时, 分配到ICA 和ECA 的血流质量流率在各模型之间是不同的。 4 个模型中心动周期内从ICA 及ECA 流出的血液质量流率曲线,见图5。可见①在心动周期的大部分时间,通过ICA 流出的血液多于ECA,这是因为ICA 直径大于ECA;②当CCA狭窄时,通过ECA 流出的血液多于ICA,而ICA 血流减少使血管壁的WSS 降低, 可能导致动脉粥样硬化发生;③当ICA 狭窄时,ICA 和ECA 之间的血液分布变得均匀,因为此时ICA丧失了直径大的优势;④当ICA 与CCA 同时狭窄时,ICA 和ECA 之间的血液分布有明显差异,因为有更多的血液自ECA 流出。
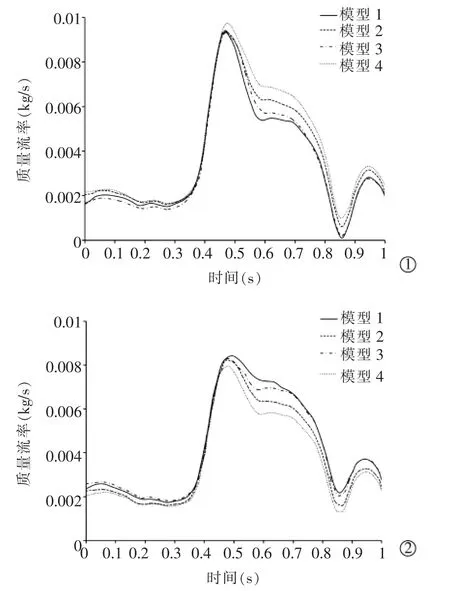
图5 血液质量流率
2.2 血流速度
随着不同模型狭窄情况的改变,血液流动也发生了变化。 流动行为的复杂性导致了后续血管内狭窄的形成与发展。 将4 个模型中T1、T2、T3、T4 4 个不同时刻及a、b、c、d、e 共5 个不同截面的血流速度进行绘制,见图6。 可见各模型在相同时间、相同截面的血流速度有着重大差异, 在ICA 与CCA 狭窄的部位可见明显流速增快,这证明了狭窄更易导致血液湍流的产生。 此外,CCA 狭窄会导致颈动脉分叉部位的流速加快及流动分离,引起ICA 血流流动行为的改变, 而ICA 的狭窄对CCA 血流基本无影响。 另外,串联狭窄的真实模型比其他假定模型具有更为复杂的血流行为改变。
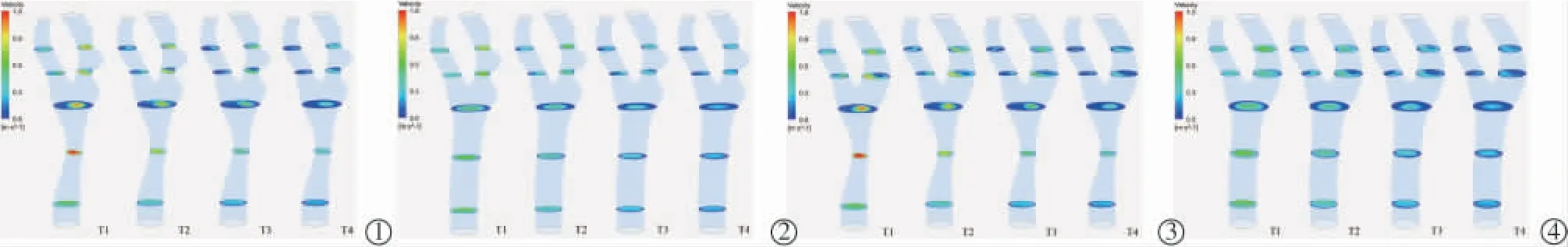
图6 心动周期内各模型血流速度变化情况
2.3 WSS
WSS 与动脉粥样硬化的形成和斑块易损性密切相关。4 个模型心动周期不同时刻WSS 的情况见图7。 可见串联狭窄的模型1 在颈动脉分叉处具有最高的WSS,仅CCA 狭窄的模型3 有较高的WSS,而仅ICA 狭窄的模型2 与无狭窄的模型4 相应位置WSS 明显较低。结果表明,随着无狭窄到CCA 狭窄再发展为串联狭窄,分叉部位WSS 逐步增大。 此外, 还发现ICA 狭窄对分叉处WSS 值的影响较CCA 狭窄所产生的影响小,这可能因为ICA 的狭窄程度较CCA 更轻,且ICA 狭窄位于血流下游,对分叉处血流状态影响有限。

图7 心动周期内各模型剪切应力(WSS) 变化情况
而以无狭窄的健康模型4 为基准,可见WSS 多集中于安全范围(0~7 Pa)内,随着局部狭窄的形成,相对应位置WSS 随之升高;当形成串联狭窄时,WSS 的高值范围(>10 Pa)部分明显扩大,这可能更易导致斑块的脱落。
2.4 TaWSS、OSI、RRT
4 种模型的TaWSS、OSI 和RRT 的情况见图8。与单一狭窄模型相比,串联狭窄模型在ICA 及CCA狭窄部位显示了更多的高TaWSS 值(>10 Pa)区域。而在ICA 狭窄中的突起处可见TaWSS 异常减低的区域,此处可能会导致动脉粥样硬化的发生发展。
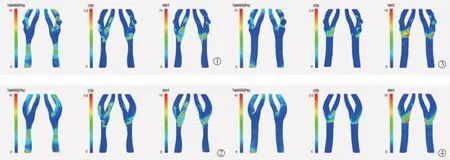
图8 各模型TaWSS、OSI、RRT 情况
此外,在无狭窄的模型4 中,在CCA 分叉处外侧壁可见高OSI 和RRT,表明在这些位置可能已形成斑块。 在仅CCA 狭窄的模型3 中,高OSI 和RRT区域出现在ECA 及ICA 外侧壁, 其中ICA 部分正是在串联狭窄模型中狭窄形成的位置。 然而,在仅ICA 狭窄的模型2 中,CCA 的OSI 和RRT 与无狭窄模型几乎没有差异。 证实在此患者特异性颈动脉分叉模型中,CCA 的狭窄更可能首先形成, 并导致了ICA 狭窄的发生。
3 讨论
血流动力学因素所致内膜损伤在动脉粥样硬化及斑块发生发展过程中起重要作用[21]。 目前,国内外关于颈动脉狭窄的血流动力学研究多为单一CCA 或ICA 狭窄,着重于术前与术后的对比以突出手术的有效性[22-24],鲜有涉及串联狭窄并对术前不同方案进行模拟对比以指导手术的研究。
TCAS 发病率低,但治疗风险高、处理难度大。关于其治疗方案的选择, 目前无大样本的研究报道,也无可靠随机对照试验参考,在近期公布的相关治疗指南及共识中也无针对串联狭窄的具体处理意见。自1953 年CEA 术首次在临床应用以来,现已成为治疗颈动脉狭窄、预防脑卒中的主要手段之一,但对于TCAS 病变尚存在以下局限性:①ICA 远端病变范围有时可超出CEA 所能暴露的最大视野,致使手术失败;②对累及CCA 近端及无名动脉的病变,CEA 需术中开胸,创伤大、风险高[9]。 而CAS 因其创伤小、恢复快,目前在颈动脉狭窄的治疗中被认为也是安全有效的, 但其对于TCAS 病变的治疗尚存在以下局限:①对于过迂曲的颈动脉及2 型、3型主动脉弓患者,CAS 操作难度大、手术失败率高;②对于TCAS 病变, 置入多个支架过程中易导致脑保护装置或支架的剐蹭、移位;③手术费用高[25]。 因此, 通过CFD 技术探索TCAS 的发生发展机制,分析其血流动力学特征, 简化甚至优化TCAS 的手术方案是临床关注的问题。
本研究通过患者CTA 图像成功建立了串联狭窄真实模型, 并通过分别去除CCA 狭窄、ICA 狭窄和两处狭窄均去除共创建了3 个假定模型以模拟不同的手术方案。 通过将假定模型与真实模型的CFD 结果进行对比研究,最终证实:①TCAS 中狭窄病变先发生于血流上游的CCA 区域,而后影响下游的ICA 区域;②串联狭窄比单个狭窄更易引起复杂的血液流动,导致异常高/低的WSS 区域,这也进一步加剧了内皮损伤、促进动脉硬化[26];③CCA 狭窄后高速血流通过颈动脉分叉时产生的涡流及流动分离,也有助于串联狭窄的形成及缺血性脑卒中的发生。对4 个模型心动周期内WSS 衍生参数的计算发现:CCA 狭窄会影响ICA 区域, 使其具有低TaWSS、 高OSI 和RRT, 而TaWSS 的低值及OSI、RRT 的高值被认为是动脉粥样硬化斑块形成的标志,这易导致继发性ICA 狭窄[27]。 相反,ICA 狭窄对CCA 的影响较小。 研究报道,单纯ICA 狭窄约占颈动脉狭窄患者总数的25%[28]。 若TCAS 首先在ICA形成狭窄继而导致CCA 狭窄,则串联狭窄的发生率不应低至所报道的2.1%~5%[7-8]。 该结论提示对于TCAS 病变,若手术仅解除了ICA 狭窄而未处理CCA 狭窄, 则CCA 的狭窄会影响ICA 血流导致狭窄复发; 而若手术仅解除CCA 斑块未处理ICA狭窄,则ICA 狭窄不会对CCA 血流产生影响。 因此,临床医生在规划串联狭窄患者的手术方案时,需考虑手术前后的血流变化, 必要时行假定模型的CFD 模拟,以指导手术方案的选择,避免狭窄复发。
本研究存在以下缺陷:①TCAS 分型多种多样,本研究仅选取了ICA 及CCA 狭窄进行个体化研究,可能使结论缺乏普遍性;②由于TCAS 的低发病率,仅选取了1 例患者,可能使结论缺乏可靠性;③在CFD 血流阈建模时,忽略了血管壁的弹性及血液的可压缩性,可能产生一定误差;④在进行CFD计算时, 对不同的模型均使用了同一速度入口、压力出口边界条件, 可能与现实情况并不完全相符。下一步将针对上述不足,进行多形态、大样本、高精度的CFD 研究,以证实上述结论。

